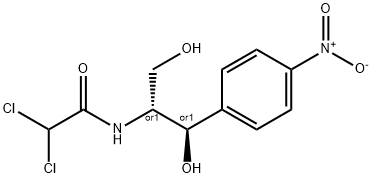
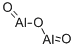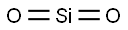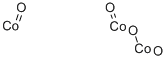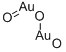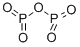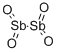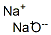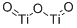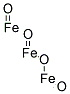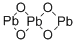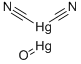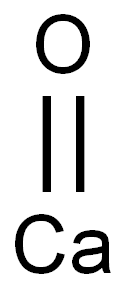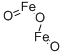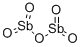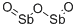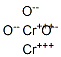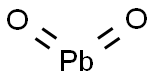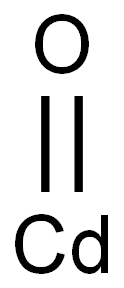酸化物及び過酸化物
酸化物は二つの元素によって構成され,一つは酸素元素の化合物である。酸化物は無機化合物に属する。ヘリウム、ネオン、クリプトン等の希少元素を除き、その他の元素はいずれも酸素と結合して酸化物を生成することができる。酸化物は酸性と塩基性によって一般的に塩基性酸化物、酸性酸化物及び両性酸化物に分けられる。塩基性酸化物は酸性物質と反応して塩基性物質を生成し、酸性酸化物は塩基性溶液と反応して塩基性物質を生成し,それに対して両性酸化物は塩基性物と反応することができ、酸性物質と反応することもできる。さらに一酸化炭素CO、一酸化窒素NO等のような酸化物があり,酸性物質と反応することがなく、塩基性物と反応することもないため,中性酸化物と呼ばされる。酸化物は自然界に広く分布しており,例えば空気中の二酸化炭素であり,石英砂の主な成分は二酸化ケイ素SiO2であり,製鉄用原料はヘマタイトであり,その主な成分は酸化鉄である。酸化物の主な応用は以下のとおりである:○1触媒。②無機顔料。③磁性材料。④光学材料。⑤超伝導材料。⑥化学的分離。
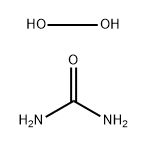
過酸化物は超酸化物とも呼ばされる。ペルオキシ基(-O-O)を含有する化合物である。無機過酸化物と有機過酸化物に分けられる。無機過酸化物は多くが活性金属の過酸化物であり,例えば過酸化ナトリウム(Na2O2)、過硫酸カリウム(K2O2)等であり,それらは水に当たり、又は熱を受ける場合に酸素原子を放出することができ,可燃物の燃焼や爆発を引き起こしやすい。強力な酸化剤である。通常の無機過酸化物は以下のとおりである:過酸化水素、過酸化ナトリウム、過酸化バリウム、過酸化カルシウム、ペルオキシ二硫酸及びペルオキシ二硫酸アンモニウム等。有機過酸化物は通常過酸化水素(H—O—O—H)の誘導体と見なされ,可燃物が酸化された後の初期生成物であり,例えば過酸化ジベンゾイル〔 (C6H5CO)2O2〕、メチルエチルケトンペルオキシド〔C2H5COOCH3〕等であり,それらの性質は非常に不安定であり,受熱、衝撃、摩擦や振動の場合に分解しやすく,酸化-還元反応を行い,自体の燃焼や爆発を引き起こすとともに,それと混合し又は接触する可燃物の燃焼や爆発を引き起こす。貯蔵と輸送の場合に,包装の完全性を保証し,性質に反する物質と離隔して配置し,着火源、熱源から離間し,水、湿気、及び直射日光を防ぎ,摩擦、衝撃、及び転動を禁止すべきである;過酸化ジベンゾイル等の有機過酸化物に対して,さらに安定剤を添加して貯蔵と輸送する必要がある。
過酸化物の主な用途は酸化剤として用いられる。過酸化水素は毒性なしの酸化剤であり,強い殺菌能力を有し,医薬分野において3%の過酸化水素を消毒殺菌剤とする。工業分野において毛、シルク、羽毛等の織物を漂白するために用いられる。実験室及び化学試薬の生産過程において,30%の溶液を酸化剤とし,例えば洗剤に用いられる過ホウ酸ナトリウム及び炭酸ナトリウム等を合成する。純粋な過酸化水素はさらにロケット燃料に用いられる。過酸化ナトリウムはよく用いられる過酸化物(過酸化ナトリウムを参照する)である。ペルオキシ二硫酸塩は重合反応の触媒に用いられる。クロム、チタン、バナジウム等の複雑なペルオキシ酸はそれぞれの色を有するため,一般的にこれらの金属イオンの定性的同定と定量的測定に用いられる。アルカリ土類金属の過酸化物は花火を製造する原料である。
- Structure:
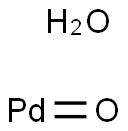
- Chemical Name:酸化パラジウム(II)水和物
- CAS:64109-12-2
- MF:OPd
- Structure:

- Chemical Name:酸化ロジウム
- CAS:12036-35-0
- MF:H2ORh
- Structure:

- Chemical Name:酸化アルミニウム(IV)
- CAS:11092-32-3
- MF:AlO2
- Structure:
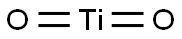
- Chemical Name:酸化チタン(),アナターゼ型
- CAS:1317-70-0
- MF:O2Ti
- Structure:
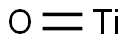
- Chemical Name:チタン(II)オキシド
- CAS:12137-20-1
- MF:OTi
- Structure:
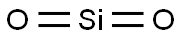
- Chemical Name:石英
- CAS:14808-60-7
- MF:O2Si
- Structure:
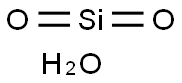
- Chemical Name:Silica glass
- CAS:10279-57-9
- MF:H2O3Si
- Structure:
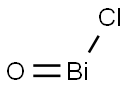
- Chemical Name:ビスマスオキシドクロリド
- CAS:7787-59-9
- MF:BiClO
- Structure:
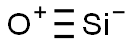
- Chemical Name:一酸化ケイ素(一酸化珪素)
- CAS:10097-28-6
- MF:OSi
- Structure:
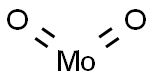
- Chemical Name:モリブデン(IV)ジオキシド
- CAS:18868-43-4
- MF:MoO2
- Structure:
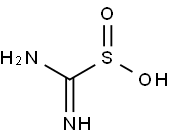
- Chemical Name:ホルムアミジンスルフィン酸
- CAS:1758-73-2
- MF:CH4N2O2S
- Chemical Name:Microsilica gel
- CAS:
- MF:
- Structure:
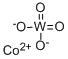
- Chemical Name:タングステン酸コバルト(II)
- CAS:10101-58-3
- MF:CoO4W
- Structure:
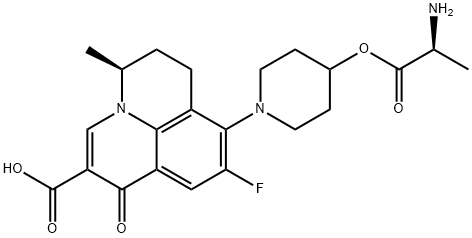
- Chemical Name:Alalevonadifloxacin
- CAS:706809-20-3
- MF:C22H26FN3O5
- Structure:
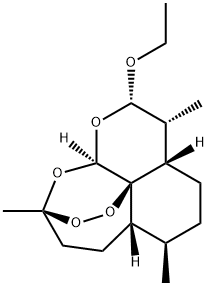
- Chemical Name:アルテモチル
- CAS:75887-54-6
- MF:C17H28O5
- Structure:
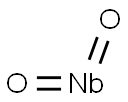
- Chemical Name:ニオブ(IV)ジオキシド
- CAS:12034-59-2
- MF:NbO2
- Structure:
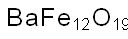
- Chemical Name:バリウム鉄オキシド
- CAS:12047-11-9
- MF:BaFeH4O
- Structure:
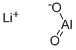
- Chemical Name:(リチオオキシ)アルミニウムオキシド
- CAS:12003-67-7
- MF:AlLiO2
- Structure:
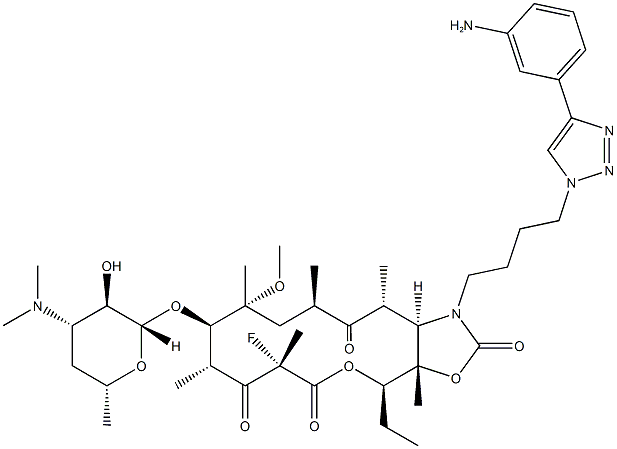
- Chemical Name:ソリスロマイシン
- CAS:760981-83-7
- MF:C43H65FN6O10
- Structure:

- Chemical Name:オルトバナジン酸ビスマス
- CAS:14059-33-7
- MF:BiO4V
- Structure:
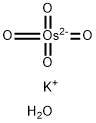
- Chemical Name:オスミウム(VI)酸カリウム二水和物
- CAS:10022-66-9
- MF:H2KO5Os-
- Structure:
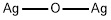
- Chemical Name:酸化銀(Ⅰ)
- CAS:20667-12-3
- MF:Ag2O
- Structure:
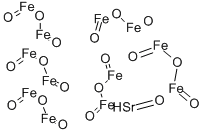
- Chemical Name:STRONTIUM FERRITE
- CAS:12023-91-5
- MF:Fe12O19Sr
- Structure:
- Chemical Name:タングステン酸銅()
- CAS:13587-35-4
- MF:CuH2OW
- Structure:
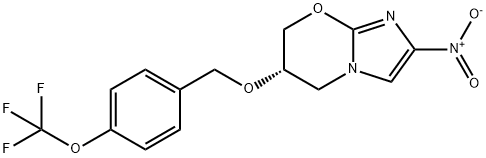
- Chemical Name:プレトマニド
- CAS:187235-37-6
- MF:C14H12F3N3O5
- Structure:
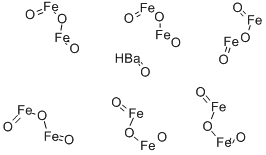
- Chemical Name:バリウムフェライト
- CAS:11138-11-7
- MF:BaO.6Fe2O3
- Structure:
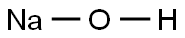
- Chemical Name:(2H)ナトリウムヒドロキシド
- CAS:14014-06-3
- MF:HNaO
- Chemical Name:酸化鉄
- CAS:12227-89-3
- MF:Fe3O4
- Structure:
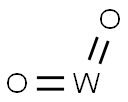
- Chemical Name:タングステン(IV)ジオキシド
- CAS:12036-22-5
- MF:O2W
- Chemical Name:Cobalt green
- CAS:
- MF:
- Structure:
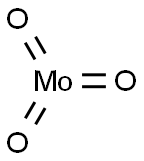
- Chemical Name:モリブデン(VI)トリオキシド
- CAS:1313-27-5
- MF:MoO3
- Structure:
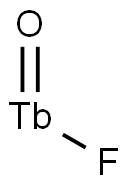
- Chemical Name:TERBIUM FLUORIDE
- CAS:21031-92-5
- MF:F3Tb
- Structure:
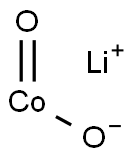
- Chemical Name:コバルト酸リチウム
- CAS:12190-79-3
- MF:CoLiO2
- Structure:
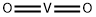
- Chemical Name:バナジウム(IV)ジオキシド
- CAS:12036-21-4
- MF:O2V
- Structure:
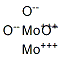
- Chemical Name:molybdenum(III) oxide
- CAS:1313-29-7
- MF:Mo2O3
- Structure:
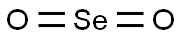
- Chemical Name:セレン(IV)ジオキシド
- CAS:7446-08-4
- MF:O2Se
- Structure:
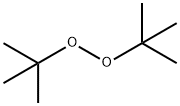
- Chemical Name:ジ-tert-ブチルペルオキシド
- CAS:110-05-4
- MF:C8H18O2
- Structure:
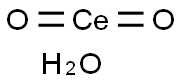
- Chemical Name:水酸化セリウム(IV) N水和物
- CAS:23322-64-7
- MF:CeH2O3
- Structure:
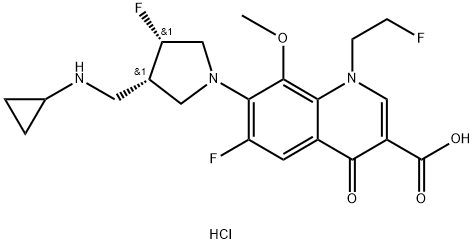
- Chemical Name:ラスクフロキサシン塩酸塩
- CAS:1433857-09-0
- MF:C21H25ClF3N3O4
- Structure:
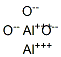
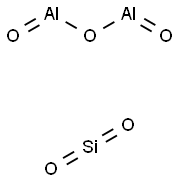
- Chemical Name:アルミニウム オキシド
- CAS:1344-28-1
- MF:Al2O3
- Structure:
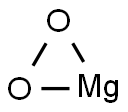
- Chemical Name:過酸化マグネシウム
- CAS:14452-57-4
- MF:MgO2
- Structure:

- Chemical Name:Lithium nickel manganese cobalt oxide
- CAS:346417-97-8
- MF:CoH3LiMnNiO
- Structure:
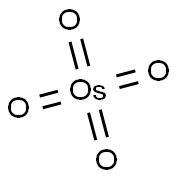
- Chemical Name:四酸化オスミウム (4%水溶液)
- CAS:20816-12-0
- MF:O4Os
- Structure:
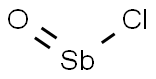
- Chemical Name:アンチモンオキシドクロリド
- CAS:7791-08-4
- MF:ClOSb
- Chemical Name:Epilancin 15X
- CAS:
- MF:
- Structure:
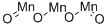
- Chemical Name:MANGANESE OXIDE
- CAS:1309-55-3
- MF:Mn3O4
- Structure:
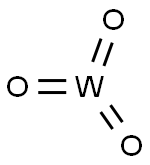
- Chemical Name:タングステン(VI)トリオキシド
- CAS:1314-35-8
- MF:O3W
- Structure:
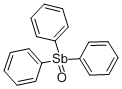
- Chemical Name:トリフェニルアンチモンオキシド
- CAS:4756-75-6
- MF:C18H15OSb
- Structure:
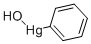
- Chemical Name:フェニル水銀(II)ヒドロキシド
- CAS:100-57-2
- MF:C6H6HgO
- Structure:
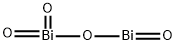
- Chemical Name:過酸化ビスマス(IV)
- CAS:12048-50-9
- MF:Bi2O4
- Structure:
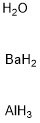
- Chemical Name:バリウム アルミニウム オキシド
- CAS:12004-04-5
- MF:AlBaH7O
- Structure:
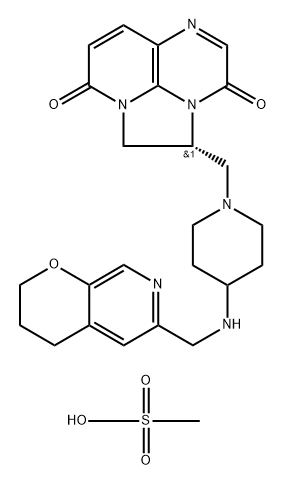
- Chemical Name:Gepotidacin mesylate
- CAS:1624306-20-2
- MF:C25H32N6O6S
- Structure:

- Chemical Name:メルサシジン
- CAS:128104-18-7
- MF:C80H120N20O21S4
- Structure:
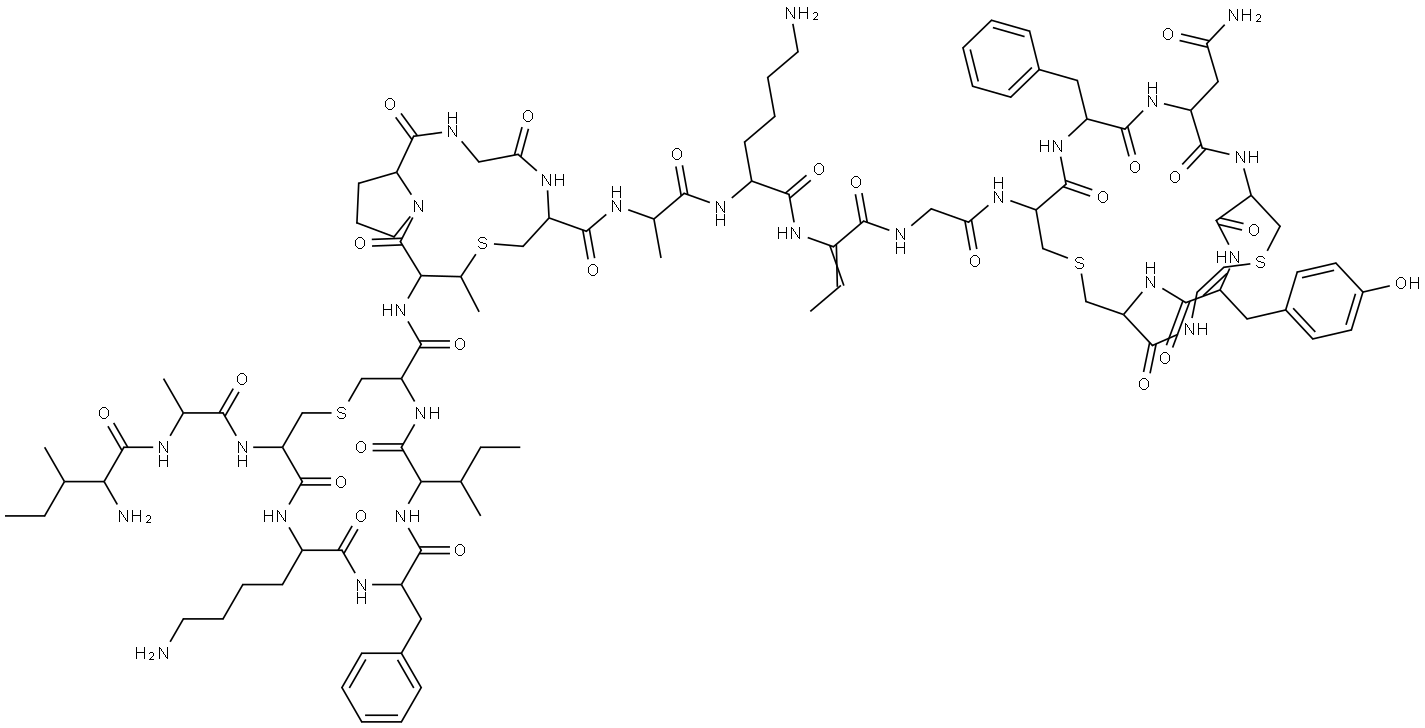
- Chemical Name:epidermin
- CAS:99165-17-0
- MF:C98H141N25O23S4
- Structure:
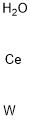
- Chemical Name:タングステン酸セリウム(III)
- CAS:13454-74-5
- MF:CeH2OW
- Structure:
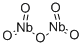
- Chemical Name:酸化ニオブ(V),3N5
- CAS:1313-96-8
- MF:Nb2O5
- Structure:
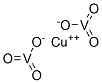
- Chemical Name:メタバナジン酸銅(II)
- CAS:14958-34-0
- MF:CuO6V2
- Structure:
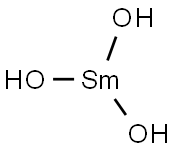
- Chemical Name:トリヒドロキシサマリウム(III)
- CAS:20403-06-9
- MF:H5O4Sm
- Structure:
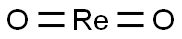
- Chemical Name:レニウム(IV)ジオキシド
- CAS:12036-09-8
- MF:O2Re
- Chemical Name:Carbapenems
- CAS:
- MF:
- Chemical Name:ラクチシン-481
- CAS:136959-47-2
- MF:
- Structure:
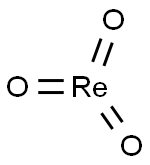
- Chemical Name:レニウム(VI)トリオキシド
- CAS:1314-28-9
- MF:O3Re
- Structure:
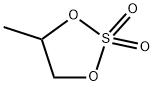
- Chemical Name:(4S)-Methyl-[1,3,2]dioxathiolane 2,2-dioxide
- CAS:174953-30-1
- MF:C3H6O4S
- Structure:
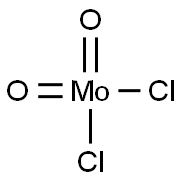
- Chemical Name:モリブデン(VI)ジクロリドジオキシド
- CAS:13637-68-8
- MF:Cl2MoO2
- Structure:
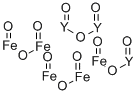
- Chemical Name:酸化鉄イットリウム
- CAS:12063-56-8
- MF:Fe5O12Y3
- Structure:
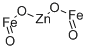
- Chemical Name:黄色酸化鉄
- CAS:12063-19-3
- MF:Fe2O4Zn
- Structure:

- Chemical Name:酸化チタン
- CAS:12065-65-5
- MF:H2OTi
- Structure:
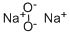
- Chemical Name:ペルオキシジナトリウム
- CAS:1313-60-6
- MF:Na2O2
- Structure:
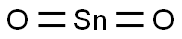
- Chemical Name:さんかすず
- CAS:18282-10-5
- MF:O2Sn
- Chemical Name:lactocin S
- CAS:125387-34-0
- MF:
- Structure:
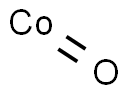
- Chemical Name:コバルト(II)オキシド
- CAS:1307-96-6
- MF:CoO
- Structure:
- Chemical Name:酸化セリウムジルコニウム
- CAS:53169-24-7
- MF:CeH2OZr
- Structure:

- Chemical Name:タングステン酸アンモニウム
- CAS:11140-77-5
- MF:H6NOW+
- Structure:
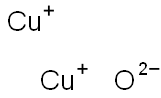
- Chemical Name:ビスクプリオ(I)オキシド
- CAS:1317-39-1
- MF:Cu2O