Azilsartan(RAAS拮抗剂)
发布日期:2020/2/18 7:59:45
背景[1-6]
Azilsartan(RAAS拮抗剂)是angiotensin II type 1(AT1)(血管紧张素II 1型)受体拮抗剂,IC50为2.6nM。Azilsartan抑制125I-Sar1-Ile8-AII对人血管紧张素1型受体的特异性结合。细胞试验中,Azilsartan也会抑制AII诱导的肌醇1磷酸盐(IP1)的积累,IC50值为9.2nM。在离体的兔子动脉条中,Azilsartan减少对AII的收缩响应,pD'2值为9.9。带状材料洗掉后,Azilsartan对AII诱导的收缩响应的抑制作用依然存在。口服葡萄糖耐量测试中(OGTT),Azilsartan抑制血浆葡萄糖水平的增加,而不会显著改变胰岛素浓度或提高胰岛素敏感性。
在骨骼肌中,0.001%剂量的Azilsartan减少TNF-α的表达。在脂肪组织中,Azilsartan减少TNF-α表达,但是增加脂联素、PPARγ、C/EBα和aP2的表达。在培养的3T3-L1脂肪前体细胞中,Azilsartan增强脂肪形成,作用于编码基因过氧化物酶体增生物激活的受体-α(PPARα)、PPARδ、瘦素、脂肪酶和脂联素的表达,比valsartan有效。外源性增补的血管紧张素II不存在下,Azilsartan也会有效抑制血管细胞增生。
在Koletsky大鼠体内,口服葡萄糖耐量测试中,Azilsartan治疗降低血压,基础血浆胰岛素浓度和胰岛素耐受指数的稳态模式评估,并抑制血糖和胰岛素浓度的过度增加。Azilsartan下调11β-羟化类固醇脱氢酶1型的表达。Azilsartan medoxomil是一种前药,在肠道和血浆中通过酯水解能够迅速转化为活性部分,azilsartan(TAK-536)。
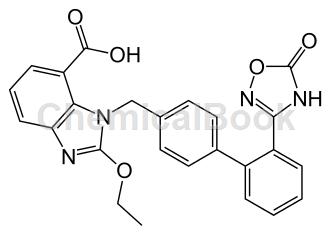
在血管平滑肌和肾上腺中,Azilsartan选择性阻断血管紧张素II与AT1(1型血管紧张素II)受体的结合,从而促进血管舒张并降低醛固酮的效果。Azilsartan是AT1受体的高选择性拮抗剂,IC50为2.6 nM,对AT1受体的亲和力是AT2受体的10,000多倍,并且对其它心脏受体或离子通道没有亲和力。Azilsartan的抑制作用在游离化合物冲洗后仍然存在(IC50值为7.4 nM)。Azilsartan也会抑制血管紧张素II诱导的肌醇-1-磷酸(IP1)在细胞水平测定中的积累,IC50值为9.2 nM,并且这种作用耐冲洗(IC50值为81.3 nM)。
应用[7][8]
Azilsartan(RAAS拮抗剂)可用于研究血管紧张素Ⅱ对多巴胺能神经元凋亡的影响:
帕金森病(Parkinson’s disease,PD)深深影响着全球范围内老年人的生活质量,同时也造成了巨大的社会经济负担。PD最主要的临床表现是运动迟缓、静止性震颤、肌强直和姿势平衡障碍,主要的病理学特点是黑质区多巴胺能神经元的进行性缺失。
研究发现,PD患者及PD动物模型的脑中,肾素-血管紧张素系统(Renin-angiotensin-system,RAS)的主要组成部分血管紧张素Ⅱ(AngiotensinⅡ,AngⅡ)的含量明显增高,提示PD的发病机制与脑内RAS的过度激活密切相关。因此,从生物学层面研究AngⅡ与PD病理进程的关联,成为了本领域的一个研究热点。RAS主要负责调节机体的血压和水、盐平衡,维持内环境的稳定。
脑中及体内多个组织和器官均存在独立的RAS系统,称为局部RAS系统。且与循环系统RAS的主要成分相似,局部RAS也可见AngⅡ及其1型受体(AT1R)和2型受体(AT2R)的稳定表达。包括我课题组在内的不少先前实验已经发现,AngⅡ与帕金森病多巴胺能神经元的损伤紧密相关,且利用血管紧张素转换酶抑制剂(ACE inhibitors,ACEI)或AngⅡ受体拮抗剂(AngiotensinⅡreceptor blockers,ARB)阻断AngⅡ介导的信号通路可减少基底节区多巴胺能神经元的凋亡。
此外,在诸如心脏、肾脏等组织或器官中,AngⅡ均可通过增强自噬活动以加剧心肌细胞和肾脏足细胞的凋亡,从而加强对心肌和肾脏的损伤,这提示细胞凋亡可能与自噬密不可分。利用可以稳定表达AT1R和AT2R的Cath.a多巴胺能细胞株作为研究对象,分别观察AngⅡ对神经元凋亡和自噬的影响以及神经元凋亡和自噬之间的关联,并进一步观察何种受体参与了AngⅡ引起前述效应的过程,从而阐明AngⅡ对离体多巴胺能神经元的影响及相关机制。ARB类药物已被部分实验证明对多巴胺能神经元具有保护作用。
参考文献
[1]Simultaneous determination of azilsartan and chlorthalidone in rat and human plasma by liquid chromatography-electrospray tandem mass spectrometry[J].Rachumallu Ramakrishna,Santosh kumar Puttrevu,Manisha Bhateria,Veenu Bala,Vishnu L.Sharma,Rabi Sankar Bhatta.Journal of Chromatography B.2015
[2]Angiotensin AT 2 receptor stimulation inhibits activation of NADPH oxidase and ameliorates oxidative stress in rotenone model of Parkinson’s disease in CATH.a cells[J].Jie Lu,Liang Wu,Teng Jiang,Yao Wang,Hongrui Zhao,Qing Gao,Yang Pan,Youyong Tian,Yingdong Zhang.Neurotoxicology and Teratology.2015
[3]In vivo gastric detection ofα‐synuclein inclusions in Parkinson’s disease[J].álvaro Sánchez‐Ferro,Alberto Rábano,María JoséCatalán,Fernando Canga Rodríguez‐Valcárcel,Servando Fernández Díez,Jaime Herreros‐Rodríguez,Elvira García‐Cobos,Marina Mataálvarez‐Santullano,Lydia López‐Manzanares,Antonio J.Mosqueira,Lydia Vela Desojo,Juan JoséLópez‐Lozano,Eva López‐Valdés,Rafael Sánchez‐Sánchez,JoséAntonio Molina‐Arjona.Mov Disord..2015(4)
[4]Ischemic Preconditioning Provides Neuroprotection by Induction of AMP-Activated Protein Kinase-Dependent Autophagy in a Rat Model of Ischemic Stroke[J].Teng Jiang,Jin-Tai Yu,Xi-Chen Zhu,Qiao-Quan Zhang,Meng-Shan Tan,Lei Cao,Hui-Fu Wang,Jian-Quan Shi,Li Gao,Hao Qin,Ying-Dong Zhang,Lan Tan.Molecular Neurobiology.2015(1)
[5]Caspase crosstalk:integration of apoptotic and innate immune signalling pathways[J].Emma M.Creagh.Trends in Immunology.2014(12)
[6]Angiotensin‐(1–7)induces cerebral ischaemic tolerance by promoting brain angiogenesis in a M as/eNOS‐dependent pathway[J].Teng Jiang,Jin‐Tai Yu,Xi‐Chen Zhu,Qiao‐Quan Zhang,Meng‐Shan Tan,Lei Cao,Hui‐Fu Wang,Jie Lu,Qing Gao,Ying‐Dong Zhang,Lan Tan.Br J Pharmacol.2014(18)
[7]Alpha‐synuclein in peripheral tissues and body fluids as a biomarker for P arkinson’s disease–a systematic review[J].N.Malek,D.Swallow,K.A.Grosset,O.Anichtchik,M.Spillantini,D.G.Grosset.Acta Neurol Scand.2014(2)
[8]高擎.血管紧张素Ⅱ对多巴胺能神经元凋亡的影响及机制研究[D].南京医科大学,2017.
欢迎您浏览更多关于AZILSARTAN (RAAS拮抗剂)的相关新闻资讯信息
