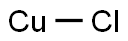
Медь I хлористая
- английское имяCopper(I) chloride
- CAS №7758-89-6
- CBNumberCB7341838
- ФормулаClCu
- мольный вес99
- EINECS231-842-9
- номер MDLMFCD00010971
- файл Mol7758-89-6.mol
| Температура плавления | 430 °C (lit.) | ||||||||||||||
| Температура кипения | 1490 °C (lit.) | ||||||||||||||
| плотность | 1.15 g/mL at 20 °C | ||||||||||||||
| Плотность накопления | 1600-1800kg/m3 | ||||||||||||||
| давление пара | 1.3 mm Hg ( 546 °C) | ||||||||||||||
| показатель преломления | 1.93 | ||||||||||||||
| Fp | 1490°C | ||||||||||||||
| температура хранения | Store at +5°C to +30°C. | ||||||||||||||
| растворимость | 0.06 g/L (25°C) | ||||||||||||||
| форма | beads | ||||||||||||||
| цвет | Slightly greenish-gray | ||||||||||||||
| Удельный вес | 4.14 | ||||||||||||||
| РН | 5 (50g/l, H2O, 20℃)(slurry) | ||||||||||||||
| Flame Color | Bluish-green | ||||||||||||||
| Растворимость в воде | 0.06 g/L (25 ºC) | ||||||||||||||
| Чувствительный | Air & Moisture Sensitive | ||||||||||||||
| Кристальная структура | Hexagonal, Wurtzite (Zincite) Structure - Space Group P 63mc | ||||||||||||||
| crystal system | Cube | ||||||||||||||
| Мерк | 14,2660 | ||||||||||||||
| Константа произведения растворимости (Ksp) | pKsp: 6.76 | ||||||||||||||
| Space group | F43m | ||||||||||||||
| Lattice constant |
|
||||||||||||||
| Пределы воздействия | ACGIH: TWA 1 mg/m3 NIOSH: IDLH 100 mg/m3; TWA 1 mg/m3 |
||||||||||||||
| Стабильность | Stable. Incompatible with oxidizing agents, potassium, water. Air, light and moisture sensitive. | ||||||||||||||
| Справочник по базе данных CAS | 7758-89-6(CAS DataBase Reference) | ||||||||||||||
| FDA 21 CFR | 582.80 | ||||||||||||||
| Рейтинг продуктов питания EWG | 2 | ||||||||||||||
| FDA UNII | C955P95064 | ||||||||||||||
| Справочник по химии NIST | Cuprous monochloride(7758-89-6) | ||||||||||||||
| Система регистрации веществ EPA | Cuprous chloride (7758-89-6) | ||||||||||||||
| UNSPSC Code | 12352302 | ||||||||||||||
| NACRES | NB.24 |
| Коды опасности | Xn,N | |||||||||
| Заявления о рисках | 22-50/53-51/53-36/37/38-41-37/38-38 | |||||||||
| Заявления о безопасности | 26-61-60-22-39 | |||||||||
| РИДАДР | UN 3082 9/PG 3 | |||||||||
| WGK Германия | 2 | |||||||||
| RTECS | GL6990000 | |||||||||
| F | 1-8-10 | |||||||||
| TSCA | Yes | |||||||||
| кода HS | 2827 39 85 | |||||||||
| Класс опасности | 8 | |||||||||
| Группа упаковки | III | |||||||||
| Токсичность | LD50 orally in Rabbit: 336 mg/kg | |||||||||
| NFPA 704: |
|
рисовальное письмо(GHS)
-
рисовальное письмо(GHS)



-
сигнальный язык
опасность
-
вредная бумага
H315:При попадании на кожу вызывает раздражение.
H302:Вредно при проглатывании.
H318:При попадании в глаза вызывает необратимые последствия.
H410:Чрезвычайно токсично для водных организмов с долгосрочными последствиями.
-
оператор предупредительных мер
P264:После работы тщательно вымыть кожу.
P273:Избегать попадания в окружающую среду.
P280:Использовать перчатки/ средства защиты глаз/ лица.
P301+P312:ПРИ ПРОГЛАТЫВАНИИ: Обратиться за медицинской помощью при плохом самочувствии.
P302+P352:ПРИ ПОПАДАНИИ НА КОЖУ: Промыть большим количеством воды.
P305+P351+P338:ПРИ ПОПАДАНИИ В ГЛАЗА: Осторожно промыть глаза водой в течение нескольких минут. Снять контактные линзы, если Вы ими пользуетесь и если это легко сделать. Продолжить промывание глаз.
Медь I хлористая химические свойства, назначение, производство
Химические свойства
white or pale grey powderФизические свойства
White cubic crystal which turns blue when heated at 178°C; density 4.14 g/cm3; the mineral nantokite (CuCl) has density 4.14 g/cm3, hardness 2.5 (Mohs), refractive index 1.930; melts at 430°C becoming a deep, green liquid; vaporizes around 1,400°C; vapor pressure 5 torr at 645°C and 400 torr at 1250°C; low solubility in water (decomposes partially); Ksp 1.72x10-7; insoluble in ethanol and acetone; soluble in concentrated HCl and ammonium hydroxide.The space lattice of CuCl belongs to the cubic system, and its zinc-blende structure has a lattice constant of a=0.541 nm and Cu–Cl=0.235 nm below 407°C, and it belongs to the hexagonal system and has a wurtzite structure at 407°C–422°C.The reflection peaks at room temperature are positioned at λ: 58 and 65.4 mm. The transmission peak is located at λ: 18.5 mm. The absorption spectrum near the absorption edge λ: 370.0 nm at liquid He temperature shows many structures because of exciton absorption.
Использование
Copper(I) chloride (CuCl) or cuprous chloride is a white powder used as an absorbing agent for carbon dioxide gas in enclosed breathing areas such as space vehicles.Определение
ChEBI: An inorganic chloride of copper in which the metal is in the +1 oxidation state.Подготовка
Copper(I) chloride is prepared by reduction of copper(II) chloride in solution: 2CuCl2 + H2 2CuCl + 2HCl Alternatively, it can be prepared by boiling an acidic solution of copper(II) chloride with copper metal, which on dilution yields white CuCl: Cu + CuCl2 2CuCl Copper(I) chloride dissolved in concentrated HCl absorbs carbon monoxide under pressure forming an adduct, CuCl(CO). The complex decomposes on heating releasing CO. Copper(I) chloride is slightly soluble in water. However, in the presence of Cl- ion, it forms soluble complexes of discrete halogeno anions such as, CuCl2-, CuCl3 2-, and CuCl4 3-. Formation of complexes and organocopper derivatives as outlined below are not confined only to copper(I) chloride, but typify Cu+ in general. Reaction with ethylenediamine (en) in aqueous potassium chloride solution forms Cu(II)-ethylenediamine complex, while Cu+ ion is reduced to its metallic state: 2CuCl + 2en → [Cuen2]2+ + 2Cl- + Cu° It dissolves in acetonitrile, CH3CN forming tetrahedral complex ion [Cu(CH3CN)4]+ which can be precipitated with large anions such as ClO4 - or PF6- . Reactions with alkoxides of alkali metals produce yellow copper(I) alkoxides. For example, reaction with sodium ethoxide yield copper(I) ethoxide, a yellow compound that can be sublimed from the product mixture: CuCl + NaOC2H5 → CuOC2H5 + NaCl Copper(I) chloride forms complexes with ethylene and other alkenes in solutions that may have compositions such as [Cu(C2H4)(H2O)2]+ or [Cu(C2H4)(bipy)]+. (bipy = bipyridyl) Reactions with lithium or Grignard reagent yield alkyl or aryl copper(I) derivatives, respectively. Such organocopper compounds containing Cu-Cu bonds are formed only by Cu+ and not Cu2+ ions.Общее описание
The structure of copper(I) chloride is similar to zinc-blende crystal at room temperature; the structure is wurtzite at 407 °C and at higher temperatures it forms copper(I) chloride vapor as per mass spectroscopy.Опасность
Copper(I) chloride is moderately toxic by ingestion and possibly other routes of entry into the body. The oral LD50 in mouse is reported to be 347 mg/kg; and subcutaneous LD50 in guinea pigs is 100 mg/kg.Перевозки
UN2802 Copper chloride, Hazard class: 8; Labels: 8-Corrosive material.Методы очистки
Wash the solid with ethanol and diethyl ether, then dry it and store it in a vacuum desiccator [.sterl.f Acta Chem Scand 4 375 1950]. Alternatively, to an aqueous solution of CuCl2.2H2O is added, with stirring, an aqueous solution of anhydrous sodium sulfite. The colourless product is dried at 80o for 30minutes and stored under N2. Cu2Cl2 can be purified by zone-refining [Hall et al. J Chem Soc, Faraday Trans 1 79 343 1983]. [Glemser & Sauer in Handbook of Preparative Inorganic Chemistry (Ed. Brauer) Academic Press Vol II p 1005 1965.]Несовместимости
Contact with strong acids forms monovalent copper salts and toxic hydrogen chloride gas. Forms shock-sensitive and explosive compounds with potassium, sodium, sodium hypobromite, nitromethane, acetylene. Keep away from moisture and alkali metals. Attacks metals in the presence of moisture. Reacts with moist air to form cupric chloride dihydrate. May attack some metals, paints, and coatings. May be able to ignite combustible materials.Медь I хлористая запасные части и сырье
сырьё
1of3
запасной предмет
- 5-[4-ФТОР-3-(ТРИФТОРМЕТИЛ)ФЕНИЛ]-2-ФУРАЛЬДЕГИД
- Acid Blue 129
- 5-[2-хлор-4-(трифторметил)фенил]-2-фуральдегид
- Клоназепам
- 2-бромхлорбензол
- 4-Хлор-3-нитротолуола
- 2-Хлор-1 ,3-динитробензол
- 3,5-дихлор-1H-индазол
- Di-t-butylmethylphosphine
- 7-хлорхинолин
- 3-хлортолуол
- Дихлорметилсилана
- 4-Хлор-N-метиланилина
- Бис (триметилсилил) ацетилен
- 2 - (4-хлорбензил) пиридин
- 5-[2,6-ДИХЛОР-4-(ТРИФТОРМЕТИЛ)ФЕНИЛ]-2-ФУРАЛЬДЕГИД
- Акрилоилхлорида
- 3-(П-ХЛОРФЕНИЛ)-3-(2-ПИРИДИЛ)ПРОПИЛАЛЬДЕГИД ДИЭТИЛ АЦЕТАЛЬ
- Ремазол бриллиантовый синий R
- 3-Phenoxytoluene
- 2,4,5-Trifluorophenylacetic кислота
- 3-ХЛОРТИОФЕН-2-КАРБОКСАМИД
- disodium 4,4'-[methylenebis(4,1-phenyleneimino)]bis[1-amino-9,10-dihydro-9,10-dioxoanthracene-2-sulphonate]
- 5- [4- (трифторметокси) фенил] -2-фуральдегида
- 3-Хлор-2-метилбензонитрил
- N,N,N',N'-тетраметил-p-фенилендиамин дигидрохлорид
- 1,4-дихлорнафталин
- 5-бром-2-хлор-3-пиколин
- 2,3-дихлорбензальдегид
- Direct Blue 86
1of8
Медь I хлористая поставщик
| поставщик | телефон | страна | номенклатура продукции | благоприятные условия |
|---|---|---|---|---|
| +8615531157085 | China | 8804 | 58 | |
| +86 13288715578 +8613288715578 |
China | 12825 | 58 | |
| +8617531153977 | China | 5855 | 58 | |
| +8617732866630 | China | 18147 | 58 | |
| +8613343047651 | China | 3692 | 58 | |
| +86-18186686046 +86-18186686046 |
China | 5861 | 58 | |
| +86-0371-55170693 +86-19937530512 |
China | 21632 | 55 | |
| +86-0551-65418679 +8618949832763 |
China | 2986 | 55 | |
| 18017610038 | CHINA | 3619 | 58 | |
| +86-0371-86658258 +8613203830695 |
China | 29871 | 58 |