人淋巴毒素α(LTA)Elisa试剂盒的应用
发布日期:2024/6/3 8:59:27
背景[1-3]
人淋巴毒素α(LTA)Elisa试剂盒是一种用于体外定量检测人体样本中淋巴毒素α(LTA)浓度的免疫分析工具。它主要被应用在医学和生物学研究领域,通过酶联免疫吸附测定法(ELISA),该试剂盒能够准确、灵敏地检测血清、血浆、组织匀浆、细胞裂解液或细胞培养上清液等样本中的LTA水平。
人淋巴毒素α(LTA)Elisa试剂盒的主要组成包括:
酶标包被板:用于承载固相抗体,通常是微孔板,每个孔都预先包被了抗胰蛋白酶的抗体。
标准品:用于绘制标准曲线,帮助计算样本中AT的浓度。
酶标试剂:即HRP标记的抗体,与样本中的AT结合后形成复合物。
洗涤液:用于洗涤酶标板,去除未结合的成分。
显色剂:与酶标抗体反应后产生颜色变化,用于定量检测AT的浓度。
终止液:用于停止显色反应,以便进行OD值的测定。
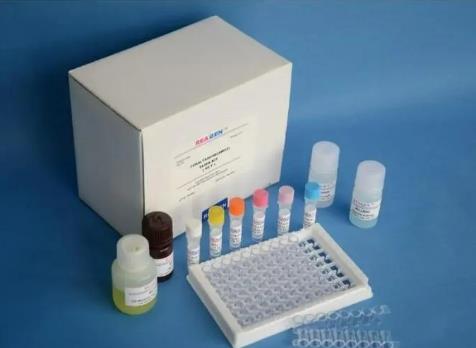
人淋巴毒素α(LTA)Elisa试剂盒
使用人淋巴毒素α(LTA)Elisa试剂盒进行实验时,需要按照以下步骤进行:
实验开始前,各试剂均应平衡至室温(试剂不能直接在37℃溶解);试剂或样品稀释时,均需混匀,混匀时尽量避免起泡。实验前应预测样品含量,如样品浓度过高时,应对样品进行稀释,以使稀释后的样品符合试剂盒的检测范围,计算时再乘以相应的稀释倍数。
1.加样:分别设空白孔、标准孔、待测样品孔。空白孔加样品稀释液100μl,余孔分别加标准品或待测样品100μl,注意不要有气泡,加样将样品加于酶标板孔底部,尽量不触及孔壁,轻轻晃动混匀,酶标板加上盖或覆膜,37℃反应120分钟。为保证实验结果有效性,每次实验请使用新的标准品溶液。
2.弃去液体,甩干,不用洗涤。每孔加检测溶液A工作液100μl(在使用前一小时内配制),酶标板加上覆膜,37℃反应60分钟。
3.温育60分钟后,弃去孔内液体,甩干,洗板3次,每次浸泡1-2分钟,大约400μl/每孔,甩干(也可轻拍将孔内液体拍干)。
4.每孔加检测溶液B工作液(同检测A工作液)100μl,酶标板加上覆膜37℃反应60分钟。
5.温育60分钟后,弃去孔内液体,甩干,洗板5次,每次浸泡1-2分钟,350μl/每孔,甩干(也可轻拍将孔内液体拍干)。
6.依序每孔加底物溶液90μl,酶标板加上覆膜37℃避光显色(30分钟内,此时肉眼可见标准品的前3-4孔有明显的梯度兰色,后3-4孔梯度不明显,即可终止)。
7.依序每孔加终止溶液50μl,终止反应,此时蓝色立转黄色。终止液的加入顺序应尽量与底物液的加入顺序相同。为了保证实验结果的准确性,底物反应时间到后应尽快加入终止液。
8.用酶联仪在450nm波长依序测量各孔的光密度(OD值)。在加终止液后立即进行检测。
人淋巴毒素α(LTA)Elisa试剂盒具有灵敏度高、特异性强、操作简便等优点,在生物医学研究、临床诊断等领域中得到了广泛应用。需要注意的是,在使用该试剂盒时,应仔细按照说明书进行操作,并注意样本的采集、保存和处理等细节问题,以保证实验结果的准确性和可靠性。
应用[4][5]
人淋巴毒素α(LTA)Elisa试剂盒可以用于淋巴毒素α与急性冠脉综合征发病关系的研究
检测急性冠脉综合征患者及对照组淋巴毒素α(LTA)C804A、A252G基因多态性,并测定LTA、髓过氧化物酶(MPO)、肿瘤坏死因子(TNFα)、细胞间黏附因子(ICAM-1)水平,分析LTA804位点、LTA252位点基因突变与冠状动脉病变范围及炎症因子表达的相关性,进而探讨遗传因素、炎症反应与急性冠脉综合征发病关系。
方法:选择2007年9月至2008年12月,天津市第一中心医院心内科收治的急性冠脉综合征组病人106例,对照组80例,入选的所有病人入院后均接受冠状动脉造影检查,不稳定心绞痛或急性心肌梗塞病人的诊断均依据ACC/AHA指南。记录患者下列临床资料:年龄、性别、吸烟史、饮酒史、高血压史、冠心病家族史、甘油三脂、总胆固醇、低密度脂蛋白、高密度脂蛋白、尿酸、空腹血糖水平等。根据冠状动脉造影结果分为急性冠脉综合征(ACS)组106例和对照组80例,ACS组根据其类型又分为不稳定型心绞痛(UAP)组和急性心肌梗塞(AMI)组。用人淋巴毒素α(LTA)Elisa试剂盒测定淋巴毒素α(LTA)、肿瘤坏死因子-α(TNF-α)、髓过氧化物酶(MPO)、细胞间黏附因子(ICAM-1)水平,用DNA试剂盒提取DNA,利用多聚酶链反应(PCR)及琼脂糖凝胶电泳分析淋巴细胞毒素-α(LTA-α)基因C804A、A252G的基因多态性并进行测序。应用SPSS13.0数据统计软件对实验数据进行统计学分析。两组间定量资料进行正态性检验,正态分布资料采用均数±标准差((?)±s)表示,两样本均数比较采用t检验,多样本均数比较应用方差分析,组间比较采用q检验。计数资料以百分数表示,例数及率的比较采用x2检验。以P<0.05为差异有统计学意义。
人淋巴毒素α(LTA)Elisa试剂盒结果:急性冠脉综合征组测定的TNF-α、MPO、LTA、ICAM-1水平高于对照组,其中AMI组TNF-α、ICAM-1水平高于UAP组(P<0.05)。急性冠脉综合征组不同病变程度的TNF-α水平差异有统计学意义,多支病变高于单支病变(P<0.01)。UAP组与AMI组测定的MPO、LTA无差异。急性冠脉综合征组不同病变范围测得的MPO、LTA、ICAM-1水平无显著性差异(P>0.05)。LTA804位点存在CC、CA、AA3种基因型。急性冠脉综合征组与对照组LTA804位点基因型、等位基因频率比较无统计学差异(P>0.05)。
参考文献
[1]Plasma levels of myeloperoxidase are not elevated in patients with stable coronary artery disease[J].Lukas Kubala;;Guijing Lu;;Stephan Baldus;;Lars Berglund;;Jason P.Eiserich.Clinica Chimica Acta,2008(1)
[2]Lymphotoxin-alpha C804A polymorphism is a risk factor for stroke.The PROSPER study[J].S.Trompet;;A.J.M.de Craen;;P.Slagboom;;J.Shepherd;;G.J.Blauw;;M.B.Murphy;;E.L.E.M.Bollen;;B.M.Buckley;;I.Ford;;A.Gaw;;P.W.Macfarlane;;C.J.Packard;;D.J.Stott;;R.G.J.Westendorp;;J.W.Jukema.Experimental Gerontology,2008(8)
[3]Symptomatic Peripheral Arterial Disease in Women:Nontraditional Biomarkers of Elevated Risk[J].Aruna D.Pradhan;;Sanjay Shrivastava;;Nancy R.Cook;;Nader Rifai;;Mark A.Creager;;Paul M Ridker.Circulation,2008(6)
[4]Plasma myeloperoxidase is related to the severity of coronary artery disease[J].Düzgün?inar;;Yavuz;;Hazirolan;;Deniz;;Tokg?zoglu;;Akata;;Demirpen?e.Acta Cardiologica,2008(2)
[5]陈欣.淋巴毒素α与急性冠脉综合征发病关系的研究[D].天津医科大学,2009.
欢迎您浏览更多关于人淋巴毒素α(LTA)Elisa试剂盒的相关新闻资讯信息


