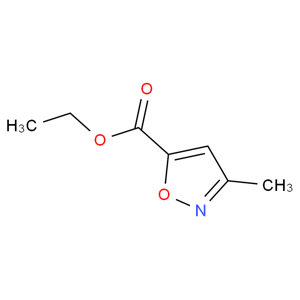
3-甲基-5-异噁唑羧酸甲酯的应用
发布日期:2020/1/8 8:29:48
背景及概述[1][2]
3-甲基-5-异噁唑羧酸甲酯为羧酸酯类化合物,可用做有机合成原料。
制备[1]
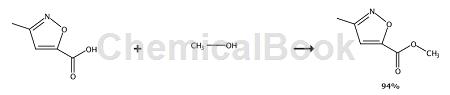
在室温下向1.0g(8mmol)3-甲基-5-异噁唑甲酸的DCM(20mL)溶液中加入2mL(23mmol)草酰氯。将反应在室温下搅拌2小时,并在减压下除去溶剂。 将残余物溶于DCM中,加入甲醇(0.62mL,15mmol)。将反应在室温下搅拌0.5小时。 减压除去溶剂,得到1.1g棕色固体状的3-甲基-5-异噁唑羧酸甲酯,产率:90%。1H NMR(500MHz,氯仿-d)δppm2.39(3H,s),3.97(3H,s),6.79(1H,s);m/z [M + H]:142。
应用[2]
US20110071196A1报道了3-甲基-5-异噁唑羧酸甲酯可用于合成CB2受体调价剂如下所示,即专利报道的实施例9:
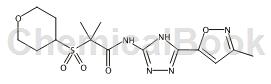
合成路线如下,3-甲基-5-异噁唑羧酸甲酯用于合成Amine V:
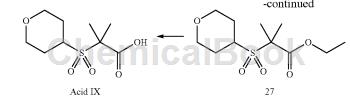
在20分钟内向166g(0.63mol)化合物27的THF /水(4 / 1,1.66L)溶液中分批加入50.5g(1.26mol)NaOH颗粒。将反应在室温下搅拌2.5天。减压除去有机溶剂,将含水残余物用水(2L)稀释,并用DCM(2L)洗涤。用浓HCl将水层酸化至pH 1-2,然后用DCM(3×2L)萃取。 酸性水溶液进一步用NaCl饱和并再次用DCM(6×2L)萃取。 减压浓缩合并的有机萃取物,得到123g酸IX,为白色固体。 收率:83%。 收率83%。1H-NMR(250MHz,氯仿-d)δppm1.71(6H,s),1.94-2.12(4H,m),3.47(2H,td,J = 11.41,2.98Hz),3.73-3.86( 1 H,m),4.07-4.15(2H,m),6.82(1H,br.s。); ES-MS:m / z 235 [M-H]。
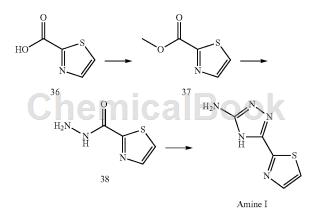

化合物38的合成:向1.00g(7mmol)化合物37的乙醇(10mL)溶液中加入1.27mL(14mmol)水合肼(35%水溶液)。将反应在室温下搅拌2小时。过滤分离所得沉淀物,用乙醇(1mL)冲洗,得到0.73g化合物38,为灰色固体。收率:73%。收率76%。 1H NMR(500MHz,氯仿-d)δppm2.37(3H,s),4.10(2H,br.s。),6.78(1H,s),8.00(1H,br.s。); m / z [M + H]:142。
胺1的合成:向0.73g(5mmol)化合物38的水(30mL)溶液中加入1.41g(5mmol)S-甲基假硫脲和0.20g(5mmol)氢氧化钠颗粒。将反应在50℃下搅拌。 3小时过滤反应混合物并用水(5mL)洗涤。将固体在减压下在40℃下干燥。将固体在220℃下熔化。得到0.48g胺1,为灰色固体。收率57%。收率72%。 1H NMR(500MHz,MeOD)δppm2.34(3H,s),6.65(1H,s); m / z [M + H]:166。
实施例9的合成:通过在50℃下用亚硫酰氯(3mL)处理,实现0.54g(2.28mmol)酸IX作为相应的酰氯的活化。 3小时将反应冷却至室温,减压除去过量的亚硫酰氯。将粗酰氯溶解在无水THF(5mL)中,加入N,N-二异丙基乙胺(0.53mL,3.03mmol),然后加入0.25g(1.52mmol)胺V.加完后,将反应加热至70℃。持续17个小时将反应冷却至室温,减压除去溶剂。将残余物溶于DCM(10mL)中并用饱和NaHCO3水溶液(10mL)洗涤。用DCM(2×10mL)反萃取水层。将合并的有机层用Na2SO4干燥,过滤,并将滤液减压浓缩。将残余物用DCM /乙醚(1 / 1,2mL)洗涤,得到0.22g实施例9产率:38%。
主要参考资料
[1] U.S. Pat. Appl. Publ., 20110071196, 24 Mar 2011
[2] US20110071196A1
欢迎您浏览更多关于3-甲基-5-异噁唑羧酸甲酯的相关新闻资讯信息