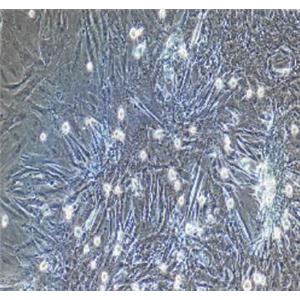
大鼠小肠隐窝上皮细胞的应用
发布日期:2021/11/24 13:23:38
背景[1-3]
大鼠小肠隐窝上皮细胞采用先机械分离法、后胶原酶消化法并通过上皮细胞专用培养基培养筛选制备而来,细胞总量约为5×10⁵cells/瓶。
大鼠小肠隐窝上皮细胞分离自小肠组织;小肠位于腹中,上端接幽门与胃相通,下端通过阑门与大肠相连,是食物消化吸收的主要场所。
小肠盘曲于腹腔内,上连胃幽门,下接盲肠,分为十二指肠、空肠和回肠三部分。小肠内消化是至关重要的,因为食物经过小肠内胰液、胆汁和小肠液的化学性消化及小肠运动的机械性消化后,基本上完成了消化过程,同时营养物质被小肠粘膜吸收了。小肠管壁由粘膜、粘膜下层、肌层和浆膜构成。
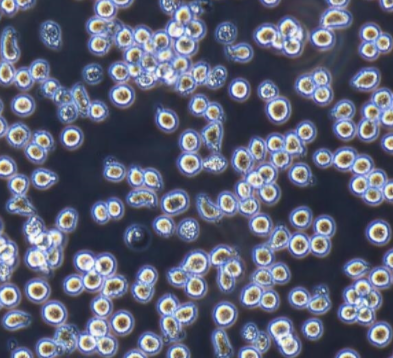
大鼠小肠隐窝上皮细胞
其结构特点是管壁有环形皱襞,粘膜有许多绒毛,绒毛根部的上皮下陷至固有层,形成管状的肠腺,其开口位于绒毛根部之间。绒毛和肠腺与小肠的消化和吸收功能关系密切;构成肠腺的细胞有柱状细胞、杯状细胞、潘氏细胞和未分化细胞。柱状细胞和内分泌细胞与绒毛上皮相似,接近绒毛的柱状细胞与吸收细胞相似,绒毛深部的柱状细胞微绒毛少而短,不形成纹状缘。小肠有三种功能即消化、吸收和分泌及运动功能,其中以吸收和分泌功能为主。
小肠腔面的环行皱襞从幽门附近开始出现,在十二指肠末段和空肠头段极发达,向下逐渐减少和变矮,至肠中段以下基本消失。粘膜表面还有许多细小的肠绒毛,是由上皮和固有层向肠腔突起而成,形状不一,以十二指肠和空肠头段最发达。绒毛于十二指肠呈叶状,于空肠呈指状,于回肠则细而短。
环行皱襞和绒毛使小肠表面积扩大20-30倍,绒毛根部的上皮下隐至固有层形成管状的小肠腺,又称肠隐窝,故小肠腺与绒毛的上皮是连续的,小肠腺直接开口于肠腔。
应用[4][5]
用于人参多糖对IEC-6细胞迁移钙离子调控相关指标影响的研究
观察人参多糖对吲哚美辛致小肠粘膜损伤的防治作用,细胞实验则观察人参多糖对IEC-6细胞迁移过程Ca2+调控相关机制的影响,以探讨人参促进小肠粘膜损伤修复的作用机制,为其治疗胃肠粘膜损伤的疗效机制提供参考。
方法1.人参多糖的提取、分离和纯化:人参经水提醇沉、Sevag法去蛋白和DEAE-52纤维素层析纯化,分别得到人参多糖1、2、3样品;苯酚-硫酸法检测人参多糖三种样品的多糖含量;Folin-酚法检测“人参多糖2”样品的蛋白含量;高效液相凝胶色谱法对“人参多糖3”样品进行纯度分析。
2. 细胞迁移实验与受试药筛选:在划痕法细胞迁移模型,观察人参多糖三种样品对细胞迁移的影响,并筛选出促进细胞迁移药效的样品作为后续实验的受试药。
3. 人参多糖防治大鼠小肠粘膜损伤的实验:吲哚美辛5mg/kg/d皮下注射,造模4d,每日造模前1h予人参多糖(5g/kg、15g/kg)灌胃治疗;5d时处死动物,大体观察小肠粘膜损伤情况,并刮取小肠粘膜用于Ca2+含量检测。
4. 比色法测定大鼠小肠粘膜Ca2+含量。
5. Ca2+相关调控指标检测:①Western-blot检测RhoA、Cav-1、TRPC1、Rac1和PLC-γ1蛋白表达;②免疫共沉淀法检测RhoA/TRPC1、Cav-1/TRPC1和Racl/PLC-γ1蛋白复合体表达;③观察Rac1活性抑制剂NSC-23766对细胞迁移的影响,并以Western-blot或免疫共沉淀法观察人参多糖对NSC-23766负荷下Rac1、PLC-γ1及其蛋白复合体表达的影响。研究结果1.人参多糖提取、分离和纯化:①人参多糖1、2、3样品得率分别为6.50%、5.06%和2.70%。②人参多糖1、2、3样品多糖含量分别为65.25%、77.38%和97.21%,其中以“人参多糖3”多糖含量最高。
6. 细胞迁移实验与受试药筛选:人参多糖三种样品均能促进细胞迁移,在动物实验中,选择“人参多糖2”样品作为受试药,设置5g/kg和15g/kg(按照生药量计算)两个剂量组。在后续细胞实验中,选择“人参多糖3”样品作为受试药,设置20、40、80和160mg/L四个剂量组,部分实验设置80mg/L和160mg/L两个剂量组。
7. 人参多糖对吲哚美辛所致大鼠小肠粘膜损伤的影响:①能减轻大鼠小肠粘膜溃疡损伤;②提高造模大鼠小肠粘膜Ca2+含量。提示人参多糖对小肠粘膜损伤的防治作用,可能与提高粘膜Ca2+含量有关,也为从细胞水平探讨其小肠粘膜保护作用提供了研究基础。
参考文献
[1]Rho GTPases and related signaling complexes in cell migration and invasion[J].Xiaoying Guan,Xiaoli Guan,Chi Dong,Zuoyi Jiao.Experimental Cell Research.2020(1)
[2]The Role of Immune Cells and Cytokines in Intestinal Wound Healing[J].Xiang Xue,Daniel M.Falcon.International Journal of Molecular Sciences.2019(23)
[3]Alcohol or Gut Microbiota:Who Is the Guilty?[J].Marica Meroni,Miriam Longo,Paola Dongiovanni.International Journal of Molecular Sciences.2019(18)
[4]Gastrointestinal Barrier Breakdown and Adipose Tissue Inflammation.[J].Cheru Lediya,Saylor Charles F,Lo Janet.Current obesity reports.2019(2)
[5]朱惠彬.人参多糖对IEC-6细胞迁移钙离子调控相关指标影响的研究[D].广州中医药大学,2020.
欢迎您浏览更多关于Rat Small Intestinal Crypt Epithelial Cells的相关新闻资讯信息