人双功能嘌呤生物合成蛋白PURH的应用研究
发布日期:2020/3/9 18:10:37
背景[1-3]
人双功能嘌呤生物合成蛋白PURH是双功能蛋白,其催化从头嘌呤生物合成途径的最后两个步骤。N-末端结构域具有磷酸核糖基氨基咪唑甲酰胺甲Chemicalbook酰基转移酶活性,并且C-末端结构域具有IMP环化水解酶活性。该基因中的突变导致AICA-核糖核苷酸。嘌呤生物合成purine biosynthesis指核酸碱基成分的腺嘌呤和鸟嘌呤的生物合成。
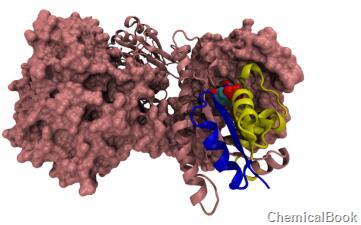
嘌呤生物合成是鸟类和爬虫类排泄物尿酸的重要代谢过程,是通过许多细胞进行的。它是以与核糖磷酸相结合的形态由氨(通过天冬氨酸,谷酰胺)、甘氨酸、甲酸和二氧化碳所合成。具有先合成肌苷酸,然后氧化成为尿酸的途径,并有AMP、GMP的合成支路。AMP可抑制PRPP向磷酸核糖胺的转化反应及肌苷酸和天冬氨酸的结合反应,而GMP前者反应和肌苷酸向黄嘌呤核苷酸的转化反应的抑制。人双功能嘌呤生物合成蛋白PURH蛋白质参与子途径的步骤1,该步骤从5-氨基-1-(5-磷酸-D-核糖基)咪唑-合成5-甲酰胺基-1-(5-磷酸-D-核糖基)咪唑-4-羧酰胺4-羧酰胺(10-甲酰基THF途径)。该途径是通过从头途径进行的IMP生物合成途径的一部分,其本身是嘌呤代谢的一部分。
应用[4][5]
用于突触结合蛋白C2结构域和甘露糖酸脱水酶的结构生物学研究突触结合蛋白(synaptotagmin,SYT)家族是一个多功能跨膜蛋白家族,主要存在于神经和内分泌系统的囊泡中。迄今已在哺乳动物中发现并鉴定了17种SYT家族的亚型,已知其中的7种亚型能通过它们的C2结构域与Ca2+结合。我们解析了结合有Ca2+和醋酸根离子的人SYT5C2A结构域的晶体结构。醋酸根离子的结合位点可能模拟了SYT5C2A结构域与磷脂磷酸基的结合位点。Ca2+结合口袋的开闭程度可能会影响与磷脂双分子层解离时SYT与磷脂荷电头部间的静电排斥势能。SYT5C2A结构域与其它SYT的C2结构域的折叠模式相似,而其Ca2+结合口袋的开闭程度在具有Ca2+结合能力的SYT中居中,这与先前所测的SYT5的胞质部分与磷脂脂质体复合物依赖Ca2+的解离速率常数在具有Ca2+结合能力的SYT中居中这一实验结果一致。甘露糖酸脱水酶(Mannonate dehydratase,ManD;EC4.2.1.8)催化一分子D-甘露糖酸脱去一分子水生成2-酮-3-脱氧-D-葡萄糖酸。该酶存在于多种细菌和古细菌中,催化Entner-Doudoroff途径中D-葡糖醛酸分解过程的第三步反应。序列比对结果表明Gram阴性菌的ManD比Gram阳性菌的ManD多了一段插入序列。为阐明该插入序列对酶的催化效率的影响,我们解析了大肠杆菌K12菌株的ManD及其与底物复合物的晶体结构。结果显示,此插入序列形成2段位于催化活性位点上方的α螺旋。这两个插入的α螺旋导致与它们相连的一个loop覆盖于底物结合口袋之上,这使得底物进入与产物离开催化活性位点的通道受限。定点突变及酶活实验证实酶的催化速率因此loop而降低。这些特征在Gram阴性菌中是保守的,因此,与Gram阳性菌相比,Gram阴性菌的ManD中的这段插入序列能够导致酶的催化速率下降,从而降低葡糖醛酸的代谢速率。为阐明TRM6-TRM61的催化机制以及这两个亚基间的相互作用方式奠定了基础。在细菌和真核生物中,嘌呤从头合成的最后两步由一个双功能嘌呤生物合成蛋白(PurH)所催化。该酶由两个以柔性区域相连的功能独立的结构域组成。其中,N端结构域具有次黄嘌呤核苷酸单磷酸环水解酶的活性,而C端结构域具有5-氨基咪唑-4-氨甲酰核苷酸甲酰基转移酶的活性。与真核生物和古细菌的PurH相比,细菌的PurH有许多插入和缺失序列,这些序列差异可能导致细菌的PurH的结构域间的相对取向与其他物种的不同。表达并纯化了大肠杆菌K12菌株的PurH(EcPurH),并获得了其晶体,收集了一套分辨率为3.05A的衍射数据。这为探究细菌PurH的两个催化结构域间的相对取向对催化效率的影响奠定了基础。
参考文献
[1]Synaptotagmin-Mediated Bending of the Target Membrane Is a Critical Step in Ca 2+-Regulated Fusion[J].Enfu Hui,Colin P.Johnson,Jun Yao,F.Mark Dunning,Edwin R.Chapman.Cell.2009(4)
[2]Structural biology of the purine biosynthetic pathway[J].Y.Zhang,M.Morar,S.E.Ealick.Cellular and Molecular Life Sciences.2009(23)
[3]Identification and characterization of the bacterial d-gluconate dehydratase in Achromobacter xylosoxidans[J].Seonghun Kim,Sun Bok Lee.Biotechnology and Bioprocess Engineering.2008(4)
[4]Crystal Structure of Thermus thermophilus tRNA m 1 A 58 Methyltransferase and Biophysical Characterization of Its Interaction with tRNA[J].Pierre Barraud,Béatrice Golinelli-Pimpaneau,Cédric Atmanene,Sarah Sanglier,Alain Van Dorsselaer,Louis Droogmans,Frédéric Dardel,Carine Tisné.Journal of Molecular Biology.2008(2)
[5]邱晓挺.突触结合蛋白C2结构域和甘露糖酸脱水酶的结构生物学研究[D].中国科学技术大学,2012.
欢迎您浏览更多关于人双功能嘌呤生物合成蛋白PURH的相关新闻资讯信息
