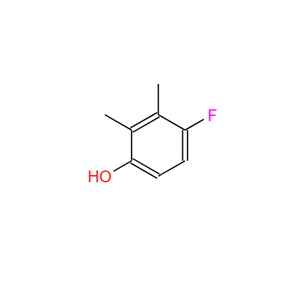
一种合成2,3-二甲基-4-氟苯酚的方法
发布日期:2022/8/3 11:18:58
背景技术
近年来,含氟化合物在制药和农业等行业方面的作用日益突出,含氟化合物变得 越来越重要,其市场范围亦正在日益扩大。含氟有机中间体主要用于制药行业的原料药生 产,发展趋势表明,医药化合物在生产过程中,对脂肪族或芳香族含氟有机中间体的市场需 求越来越普遍,在药物品种中所占的比例越来越高。有机氟中间体化合物具有较强的稳定性、生理活性、脂溶性和疏水性,可以调节电子、亲脂性等参数,所以很多含氟药物在性能上 相对具有用量少、毒性低、药效高、代谢能力强等优点,对药物的药效学和药物动力学性质 产生重大的影响。由于含氟药物的性能表现优越,因此,对含氟药物的研究和开发推动了含 氟有机中间体国内外市场的扩大。与此同时,对于含氟有机中间体的合成也成为了研究的 热点。在含氟有机中间体的合成中,可选择的合成路线和起始原料都非常多,且合成路线中 步骤通常也较多,操作比较复杂,而且,大多数起始原料也比较昂贵,因此,寻求优化的合成 路线,以降低成本并适用于扩大化生产,是当前含氟有机中间体合成中需要解决的首要问 题。
2,3-二甲基-4-氟苯酚是一种比较重要的含氟化合物,广泛用于医药中间体的合成,是制备含氟药物化合物必备的原料。但是,目前尚未见有文献报道合成2,3-二甲基-4-氟苯酚的方法。
发明内容
有鉴于此,本发明的目的在于提供一种合成2,3-二甲基-4-氟苯酚的方法,操作简单,成本低廉,收率高,纯度高,反应扩大化生产方便,可靠,能够满足市场需要。
为了实现上述目的,本发明采用以下技术方案:
—种合成2,3-二甲基-4-氟苯酚的方法,包括以下步骤:
2,3-二甲基氟苯经溴代反应得到3-溴-6-氟邻二甲苯,3-溴-6-氟邻二甲苯经甲氧 基化得到3-甲氧基-6-氟邻二甲苯,3-甲氧基-6-氟邻二甲苯水解得到2,3-二甲基-4-氟苯酚。
其制备路径如下:
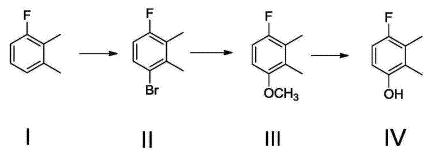
其中,式I所示化合物为2,3-二甲基氟苯,式Π所示化合物为3-溴-6-氟邻二甲苯, 式m所示化合物为3-甲氧基-6-氟邻二甲苯,式IV所示化合物为2,3-二甲基-4-氟苯酚。
在本发明的一些具体实例中,一种合成2,3-二甲基-4-氟苯酚的方法,包括以下步 骤:
(1)将二氯甲烷、2,3-二甲基氟苯和三氯化铝依次加入到反应容器中,在20〜 25°C搅拌;从装有全部溴素的滴液器中一次放出部分溴素加入到反应容器,在20〜35 °C搅拌,引发反应并使得反应液为红色后,再将滴液器中的剩余溴素滴加到反应容器 中,在20〜25°C搅拌,滴加完毕后反应0.5〜1小时,结束反应,反应液经后处理得到3-溴-6-氟邻二甲苯(如式Π所示);
其中,三氯化铝与2,3-二甲基氟苯的质量比为0.01〜0.05:1,所述全部溴素与2, 3-二甲基氟苯的摩尔比为1: (0.95〜1.0),所述部分溴素占全部溴素质量的10〜20%;
(2)在N2保护下,向第二反应容器中加入3-溴-6-氟邻二甲苯、N,N-二甲基甲酰胺 (DMF)和甲醇,再向其中分批缓慢加入甲醇钠,控制温度在10〜30°C,加料完毕后,加热使体 系升温至回流,反应4〜6小时,结束反应后降至室温,反应液经后处理得到3-甲氧基-6-氟 邻二甲苯(如式m所示);
其中,每克3-溴-6-氟邻二甲苯对应3.9〜4. ImL由N,N-二甲基甲酰胺和甲醇构成 的溶剂,N,N-二甲基甲酰胺与甲醇的体积比为7: 3,甲醇钠与3-溴-6-氟邻二甲苯的摩尔比 为2.0〜2.2;
(3)将装有N,N-二甲基苯胺的第三反应容器置于10〜30°C水浴中,再向第三反应 容器中缓慢加入三氯化铝;然后,将由3-甲氧基-6-氟邻二甲苯溶解在甲苯中得到的混合溶 液缓慢滴加到第三反应容器中,滴加完毕后,加热使体系升温至回流,反应4〜8小时,结束 反应后降至室温,反应液经后处理得到2,3_二甲基-4-氟苯酚(如式IV所示);
其中,三氯化铝与3-甲氧基-6-氟邻二甲苯的摩尔比为1.9〜2.1:1,N,N-二甲基苯 胺与3-甲氧基-6-氟邻二甲苯的摩尔比为1.9〜2.1:1,每克3-甲氧基-6-氟邻二甲苯对应3 〜3 · 2mL甲苯。
优选的技术方案中,步骤⑴中,所述滴液器为恒压滴液漏斗。
优选的技术方案中,步骤⑴中,所述全部溴素与2,3_二甲基氟苯的摩尔比为1。
优选的技术方案中,步骤(1)中,所述后处理过程为:将饱和亚硫酸钠水溶液滴加 到反应容器的反应液中,反应液逐渐变为无色后,将反应容器内液体静置,分层为 水相和有机相,取有机相用无水硫酸钠干燥,然后过滤得到滤液和滤饼,将所述滤饼用二氯 甲烷洗涤,洗涤所得液相与所述滤液合并得到有机相,所得有机相经减压浓缩得到产物3-溴-6-氟邻二甲苯。
进一步优选的技术方案中,步骤(1)所述后处理过程中,亚硫酸钠与2,3-二甲基氟 苯的摩尔比为0.1〜0.2:1。
进一步优选的技术方案中,步骤(1)所述后处理过程中,所述减压浓缩是在50〜55 ℃进行,至基本无液体出来结束。
本发明步骤⑴中,二氯甲烷作为溶剂使用,其用量可选择为2,3-二甲基氟苯重量 的1〜10倍。
优选的技术方案中,步骤⑵中,甲醇钠与3-溴-6-氟邻二甲苯的摩尔比为2。
优选的技术方案中,步骤(2)中,所述后处理过程为:将反应液加入质量百分比浓 度为16%〜20%的稀盐酸中,分层为有机相和水相,保留有机相,水相继续用乙酸乙酯萃取 若干次,合并所有的有机相;将所得有机相用饱和食盐水洗涤,洗涤后分层,取有机相再用 无水硫酸钠干燥,然后过滤得到滤液和滤饼,将所述滤饼用乙酸乙酯洗涤得到液相,所述液 相与所述滤液合并得到有机相,所得有机相经减压浓缩得到产物3-甲氧基-6-氟邻二甲苯。
进一步优选的技术方案中,步骤(2)所述后处理过程中,质量百分比浓度为16%〜 20%的稀盐酸与3-溴-6-氟邻二甲苯的摩尔比为3.9〜4.4。
进一步优选的技术方案中,步骤(2)所述后处理过程中,所述乙酸乙酯萃取的次数 为2〜3次。
进一步优选的技术方案中,步骤(2)所述后处理过程中,所述减压浓缩是在50〜55 °C进行,至基本无液体出来结束。
优选的技术方案中,步骤(3)中,所述后处理过程为:将反应液加入质量百分比浓 度为16%〜20%的稀盐酸中,分层为有机相和水相,保留有机相,水相继续用甲苯萃取若干 次,合并所有的有机相;向所得有机相加水后,缓慢加入氢氧化钠,体系pH值在10以上,再次 分层为有机相和水相,取水相用二氯甲烷萃取若干次,萃取后分离所得的水相用质量百分 比浓度为36 %〜38 %的盐酸处理至pH值为1〜2,过滤后弃去滤液,滤饼用水洗涤后,50〜55 °C干燥滤饼,得到产物2,3-二甲基-4-氟苯酚。
进一步优选的技术方案中,步骤(3)所述后处理过程中,所述甲苯萃取的次数为2 〜3次。
进一步优选的技术方案中,步骤⑶所述后处理过程中,所述二氯甲烷萃取的次数 为2〜3次。
进一步优选的技术方案中,步骤⑶所述后处理过程中,所述干燥为鼓风干燥。
进一步优选的技术方案中,步骤(3)所述后处理过程中,氢氧化钠与3-甲氧基-6-氟邻二甲苯的摩尔比为1.0〜1.2:1,质量百分比浓度为16%〜20%的稀盐酸与3-甲氧基-6-氟邻二甲苯的摩尔比为1.9〜2.4:1。
本发明还提供了由上述合成方法制得的2,3-二甲基-4-氟苯酚。
本发明中,所述室温,通常是指10〜30°C。
本发明的合成方法中,通过三氯化铝的加入,使得溴素与2,3_二甲基氟苯高选择 性反应生成3-溴-6-氟邻二甲苯,有效避免了邻位取代副反应发生,所合成的3-溴-6-氟邻 二甲苯纯度大于93%,大大高于通常情况下溴代反应得到的产物的纯度;进一步,将高纯度 的3-溴-6-氟邻二甲苯在N,N-二甲基甲酰胺和甲醇钠作用下甲氧基化得到3-甲氧基-6-氟 邻二甲苯,通过反应参数的控制,使得甲氧基化的转化率大于90%;最后,3-甲氧基-6-氟邻 二甲苯水解并经酸碱提纯处理和二氯甲烷萃取,得到纯度大于98 %的2,3-二甲基-4-氟苯 酚。该合成方法以来源广泛、价格低廉的2,3_二甲基氟苯为反应原料,每一步反应都能 化得到纯度较高的中间体,使得整个反应的总收率高,而最终产物的纯度更是高达98%以 上,经济效益非常明显,特别适合工业化大规模应用和推广。
与现有技术相比,本发明具有以下有益的技术效果:
1、本发明反应步骤较少,且反应的高选择性减少了反应过程中的副产物,简化了 反应过程,缩短反应时间,更加适应目前工业化的需要。
2、本发明原料低廉易得,使用的溶剂试剂比较常规,大大降低了生产的成本。
3、本发明反应条件温和安全,工艺操作简单易实现,方法稳定可靠易控制,适合进 行扩大化生产。
4、本发明产品的收率和纯度高,经济效益好,适合工业化生产。
具体实施方式
为了更好地说明本发明,便于理解本发明的技术方案,下面结合附图和具体实施 例,对本发明作进一步详细说明。应理解,下述的实施实例仅用于说明本发明,并不代表或 限制本发明的权利保护范围,本发明的保护范围以权利要求书为准。
(一)3-溴-6-氟邻二甲苯的制备
将400g二氯甲烷,124g的2,3-二甲基氟苯、5g三氯化铝依次加入IL的三口反应瓶 中,在20°C搅拌;从装有160g溴素的恒压滴液漏斗中一次放出16〜32g溴素加入到三口反应 瓶,在30°C搅拌,引发反应并产生大量溴化氢使得反应液为红色;此时,再将恒压滴液漏斗 中的剩余溴素滴加到三口反应瓶中,在20°C搅拌,滴加完毕后反应0.5小时结束。
反应结束后,对反应液进行后处理:将50ml饱和亚硫酸钠水溶液滴加到三口瓶的 反应液中,以去除少量未反应的溴素,室温条件下,等到反应液逐渐变为无色,意味着溴素 处理完全,将三口瓶内液体静置,分层为水相和有机相,水相另外保留,有机相用无水硫酸 钠干燥,然后过滤得到滤液和滤饼,将滤饼用少许二氯甲烷洗涤,洗涤所得液相与滤液合并 得到有机相,有机相在50〜55 °C减压浓缩至基本无液体,得到产品189g。
反应过程中产生的溴化氢气体,通过接在三口反应瓶上的导管导出到尾气吸收处 理系统中通过氢氧化钠水溶液进行吸收处理。产品3-溴-6-氟邻二甲苯,8.9min为邻位取代副反应产物,数据计算结果显示:产品纯度达88.4%以上, 副反应产物极少(约3.3%),剩余的主要为原料,计算收率为87%。
(二)3-甲氧基-6-氟邻二甲苯的制备
N2保护下,向IL反应瓶中加入102g的3-溴-6-氟邻二甲苯和285ml N,N-二甲基甲 酰胺(DMF)以及122ml甲醇,再向其中分四批缓慢加入54g甲醇钠,控制温度在10〜30 °C,加 料完毕,油浴加热使得体系升高至回流,维持回流状态下反应4小时即可,降温至室温。
反应结束后,对反应液进行后处理:将反应液倒入400g质量百分比浓度为18%的 稀盐酸中处理,分层为有机相和水相,保留有机相,水相继续加入500ml乙酸乙酯萃取三次, 合并所有的有机相,用IOOml饱和食盐水洗涤,洗涤后分层,取有机相再用无水硫酸钠干燥, 然后过滤得到滤液和滤饼,滤饼用少量乙酸乙酯洗涤得到液相,该液相与滤液合并得到有 机相,有机相在50〜55 °C减压浓缩至基本无液体,得到产品79.3g。目标产品3-甲氧基-6-氟邻二甲苯,8.6min为 邻位取代副产物的反应产品,数据计算结果显示:产品纯度为88.4%,副反应产物极少(约 2%),剩余的主要是原料及溶剂残留,计算收率为90%。
(三)2,3-二甲基-4-氟苯酚的制备
在IL三口瓶中加入121g N,N-二甲基苯胺后,将该三口瓶置于常温(10〜30°C)水 浴中,再向三口瓶中缓慢加入133g三氯化铝;然后,将由77g的3-甲氧基-6-氟邻二甲苯溶解 在240ml甲苯中得到的混合溶液,缓慢滴加到三口瓶中,滴加完毕,油浴加热使体系升温至 回流,维持回流状态下反应4小时后结束,自然降温至室温。
反应结束后,对反应液进行后处理:将反应液倒入200g质量百分比浓度为18%的 稀盐酸中,分层为有机相和水相,保留有机相,水相用100ml甲苯萃取两次,合并所有的有机 相,向所得有机相中加入200〜300ml水,再缓慢加入20g氢氧化钠,体系pH值在10以上,再次 分层为有机相和水相,取水相用二氯甲烷萃取两次,萃取后分离所得的水相用100g质量百 分比浓度为36.5%的盐酸处理至pH值为1,过滤后弃去滤液,滤饼用少许水洗涤后,50°C鼓 风烘干滤饼,得到目的产物59.5g。确定所得产品为2,3-二甲基-4-氟苯酚。
欢迎您浏览更多关于2,3-二甲基-4-氟苯酚的相关新闻资讯信息