4,7-双(2-溴-5-噻吩基)-2,1,3-苯并噻二唑的合成与有关研究
发布日期:2025/3/27 10:34:30
简述
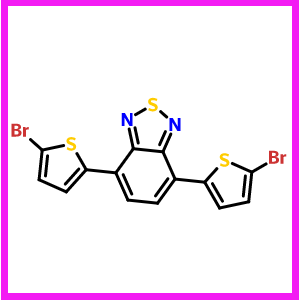
4,7-双(2-溴-5-噻吩基)-2,1,3-苯并噻二唑(4,7-Bis(2-bromo-5-thienyl)-2,1,3-benzothiadiazole)又名4,7-双(5-溴-2-噻吩基)-2,1,3-苯并噻二唑,分子式为C14H6Br2N2S3,分子量为458.21384。常温常压下,4,7-双(2-溴-5-噻吩基)-2,1,3-苯并噻二唑表现为淡黄色粉末,有关该物质的部分物性数据包括:密度:1.898g/cm3;沸点:527.304℃ at 760 mmHg;闪点:272.704℃。

合成工艺
2,1,3-苯并噻二唑(BT)由苯环和噻唑环构成,具有较强大的共面性,吸电子能力,较好的空气稳定性和高载流子迁移率,可作为受体材料。另外,噻吩基为含有S原子的五元环结构,也具有强的供电子能力,两者通常被作为受体单元广泛应用于有机合成中。因此,对同时具有上述结构的4,7-双(2-溴-5-噻吩基)-2,1,3-苯并噻二唑进行合成工艺研究具有重要意义。以2,1,3-苯并噻二唑为基体,引入噻吩基团以及溴原子进行改性即可合成4,7-双(2-溴-5-噻吩基)-2,1,3-苯并噻二唑[1]。
将合成探索扩大范围至4,7-双(5-卤代噻吩-2-基)-2,1,3-苯并噻二唑,研究表明,在钯催化剂和溶剂存在下,将4,7-二卤代-2,1,3-苯并噻二唑和噻吩基加成试剂接触,该噻吩基加成试剂可以是2-噻吩基卤化锌,2-噻吩基卤化镁或2-噻吩硼酸,在这样的条件下形成4,7-双(噻吩-2-基)-2,1,3-苯并噻二唑。然后将该前体卤化,优选溴化,形成所需的二溴化产物4,7-双(2-溴-5-噻吩基)-2,1,3-苯并噻二唑。溴原子的引入,使得4,7-双(2-溴-5-噻吩基)-2,1,3-苯并噻二唑的UV-Vis光谱产生相应的红移,其薄膜的UV-Vis光谱覆盖至700nm,且其荧光发射发生猝灭,表明其具有优良的光吸收性能。以其为原料单体制备9,9-二取代芴共聚物可用于聚合物发光二极管(pLED)应用领域[2]。
有关研究
采用周期性密度泛函理论,在PW91/DNP水平上研究4,7-双(2-溴-5-噻吩基)-2,1,3-苯并噻二唑(简称DBrTBT)在CdSe(100)和CdSe(111)表面的吸附。吸附前后DBrTBT的Mulliken电荷和前线轨道分析表明:当DBrTBT分别吸附在CdSe(100)和CdSe(111)表面时,DBrTBT向CdSe(100)和CdSe(111)表面的电荷转移量分别为0.220和0.058e。吸附能,能隙和态密度分析表明:DBrTBT吸附于CdSe(100)表面的吸附能(-15.37 eV)强于吸附于CdSe(111)表面的吸附能(-2.50 eV),有更强的表面驰豫现象。DBrTBT吸附于CdSe(100)表面的能隙小于吸附于CdSe(111)表面的能隙。DBrTBT与CdSe(100)表面形成的共混膜是具有更好光伏性能的太阳能电池材料[3]。
参考文献
[1]蓝国森,李海财,余嘉裕,等.2,1,3-苯并噻二唑类溴化物的合成及其性质研究[J].广东化工, 2018, 45(8):3.DOI:CNKI:SUN:GDHG.0.2018-08-022.
[2]张春明.制备4,7-双(5-卤代噻吩-2-基)-2,1,3-苯并噻二唑及其前体的方法:CN200480013233.X[P].CN1791584.DOI:CN1791584 A.
[3]张福兰,罗臣.4,7-二(5-溴噻吩-2-基)-2,1,3-苯并噻二唑在CdSe表面吸附的理论研究[J].分子科学学报:中英文版, 2020.DOI:10.13563/j.cnki.jmolsci.2020.06.006.
欢迎您浏览更多关于4,7-双(2-溴-5-噻吩基)-2,1,3-苯并噻二唑的相关新闻资讯信息