
5YR企业会员
发布人:上海优宁维生物科技股份有限公司
发布日期:2026/2/26 17:13:06
蛋白翻译后修饰(Post-translational modification, PTM)是指在蛋白质合成完成后,蛋白质分子经历的各种化学修饰过程。这些修饰可以影响蛋白质的功能、活性、稳定性、定位和相互作用等特性。小优为您整理了10种经典和前沿热门的翻译后修饰的机制和功能,方便小伙伴们查看。由于篇幅有限,本篇先介绍5种翻译后修饰,剩下5种将下篇介绍。
1、磷酸化
- 磷酸化机制:
在蛋白激酶(protein kinase,PK)的催化下,ATP的磷酸基团被转移到蛋白的氨基酸上,从而发生磷酸化修饰;在磷酸酯酶的催化下,磷酸基团可以从蛋白质氨基酸上脱落。蛋白磷酸化普遍存在于生物体蛋白中,其中以丝氨酸(S)、苏氨酸(T)和酪氨酸(Y)残基磷酸化修饰为主。
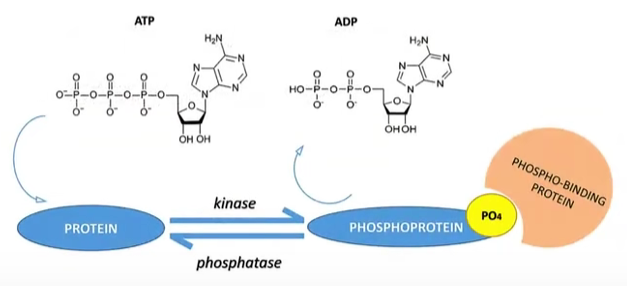
- 生物学功能:
通过蛋白激酶和磷酸酯酶可逆的蛋白磷酸化过程,实现复杂而精准的调控。
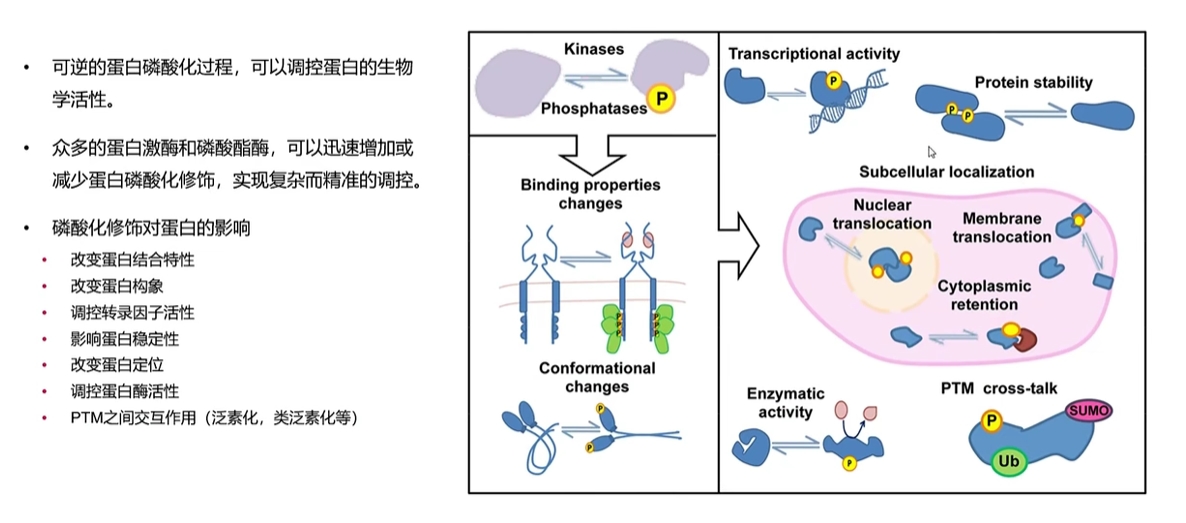
如下图所示,蛋白发生磷酸化后会引起蛋白的结合能力的改变和蛋白构象的改变,进而发挥更多的生物学功能。
左上:调控转录因子的活性。例如细胞受细胞因子(如 IL-6)刺激时,JAK 激酶直接磷酸化 STAT3 的酪氨酸 705 位点,磷酸化的 STAT3 形成同源二聚体入核,与靶基因启动子结合并激活转录。
右上:影响蛋白的稳定性。例如DNA 损伤信号激活 ATM/ATR 激酶,磷酸化 p53 的 Ser15、Ser20 位点,直接破坏 p53 与泛素连接酶 MDM2 的结合,阻断 MDM2 介导的泛素化降解途径,使 p53 在细胞内大量累积并发挥转录调控功能。
中间:改变蛋白的亚细胞定位:
(1)影响蛋白核定位。例如静息状态下,NF-κB 在细胞质里被 IκB 蛋白抑制。当细胞受到炎症信号刺激时,IκB 会被磷酸化并降解,NF-κB 随之被释放并磷酸化,然后进入细胞核,激活炎症相关基因的表达。
(2)影响蛋白膜定位。例如当生长因子(如胰岛素)与细胞膜上的受体结合后,会激活 PI3K,使细胞膜上的 PIP2 转化为 PIP3。Akt 的 PH 结构域会结合 PIP3,从而被招募到细胞膜上,然后被 PDK1 和 mTORC2 磷酸化激活,进而传递增殖和存活信号。
(3)影响蛋白的细胞质滞留。例如胰岛素或胰岛素样生长因子(IGF)信号激活 PI3K/Akt 通路,Akt 激酶磷酸化 FoxO1 的 Thr24、Ser256、Ser319 位点,磷酸化后的 FoxO1 会与 14-3-3 蛋白结合,被锚定在细胞质中无法入核;当该信号通路被抑制时,FoxO1 去磷酸化,随即进入细胞核结合靶基因启动子,调控糖脂代谢、细胞凋亡相关基因的转录。
下左:调控蛋白酶活性。例如细胞受肾上腺素、胰高血糖素刺激时,依赖 cAMP 的蛋白激酶 A(PKA)催化糖原磷酸化酶的 Ser14 位点 磷酸化,引发酶蛋白构象从无活性的 T 态(紧张态) 转变为有活性的 R 态(松弛态),暴露出与糖原底物的结合位点。
下右:影响和其他PTM之间的交互。例如细胞发生 DNA 损伤时,ATM 激酶催化组蛋白 H3 的Ser10 位点磷酸化,该修饰会直接招募组蛋白甲基转移酶Dot1L,促使邻近的H3K79 位点发生甲基化;而 H3K79 甲基化又会进一步募集 DNA 损伤修复相关蛋白(如 53BP1),启动损伤修复通路。
类别
产品
货号
Phospho-Tyrosine Mouse mAb (P-Tyr-100)
Phosphotyrosine Recombinant Rabbit mAb (S-R207)
Phospho-NF-kappaB p65 (Ser536) (93H1) Rabbit Monoclonal Antibody
Tau (phospho T181) Recombinant Rabbit mAb (SDT-R045)
CREB (phospho S133) Recombinant Rabbit mAb (S-1100-102)
2、泛素化
- 泛素化机制:
泛素化是将 76 个氨基酸组成的泛素分子(Ubiquitin)通过共价键连接到靶蛋白赖氨酸残基的翻译后修饰,可形成单泛素化或多聚泛素链(K48、K63 等链接方式),是调控蛋白质命运的关键机制。
泛素化主要包括3个阶段:
(1)激活阶段:泛素激活酶(E1)消耗 ATP,使泛素 C 端羧基与 E1 的半胱氨酸残基形成硫酯键,激活泛素。
(2)结合阶段:激活的泛素被转移至泛素结合酶(E2)的半胱氨酸残基,形成 E2 - 泛素复合物。
(3)连接阶段:泛素连接酶(E3)识别靶蛋白,介导泛素从 E2 转移至靶蛋白,完成单泛素化或多聚泛素链组装,E3 的底物特异性决定修饰的特异性。
(4)DUB是去泛素化酶,在底物被送入蛋白酶体核心降解之前,DUB 会先把泛素链从底物上完整地切割下来,避免泛素被一同降解,实现修饰的动态调控和泛素分子的重复使用。
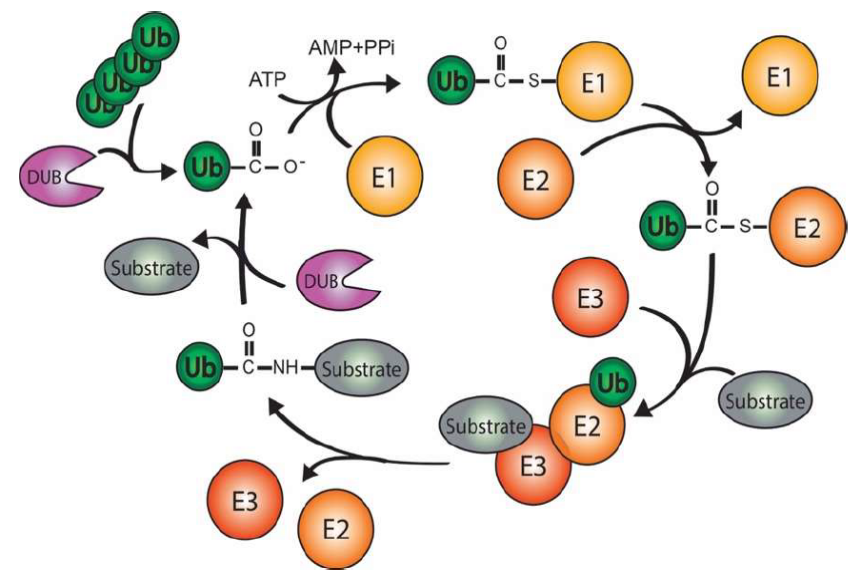
- 生物学功能:
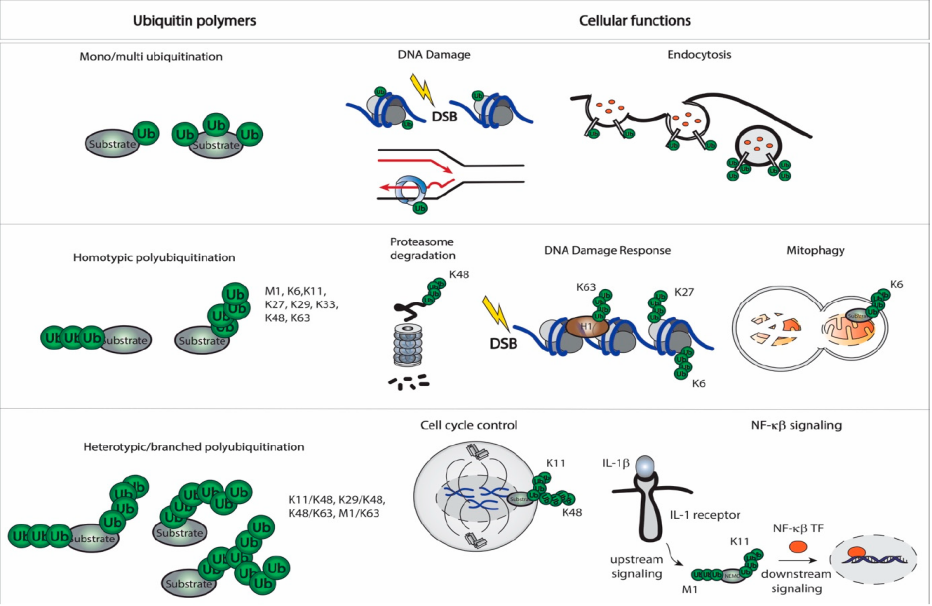
泛素化最经典和最为熟知的功能是介导蛋白降解,但这并不是泛素化唯一的功能。如下图所示,根据泛素分子的结合形式,泛素化可以分为单泛素化,同型多泛素化和异型多泛素化几类,分别介导不同的生物学功能。
(1)单泛素化 / 多单泛素化(Mono/multi ubiquitination)
定义:靶蛋白上的 1 个或多个赖氨酸残基分别被 1 个泛素分子标记(不是形成一条链)。
功能:通常不介导降解,而是调控蛋白的定位或活性。
左图:DNA 损伤修复。单泛素化可以招募修复蛋白到 DNA 双链断裂(DSB)位点,启动修复过程。当 DSB 发生时,染色质上的组蛋白 H2AX 会被磷酸化(γ-H2AX),随后一系列修复蛋白会被招募到损伤位点。其中,单泛素化修饰可以作为 “招募信号”,把下游的修复因子(如 RPA、Rad51)带到断裂处,启动修复过程。
右图:内吞作用(Endocytosis)介导受体调控。细胞膜上的受体(如 EGF 受体)被单泛素化后,会被识别并招募到内吞小体,最终进入溶酶体降解或循环到膜表面。这是调控细胞表面受体数量的重要方式。
(2)同型多泛素化(Homotypic polyubiquitination)
定义:多个泛素分子通过自身特定的赖氨酸残基(如 K48、K63)连接成一条线性或分支链,再连接到靶蛋白上。
功能:连接位点不同,功能完全不同。
左图:介导蛋白降解。K48 连接的泛素链是最经典的降解信号。靶蛋白被 K48 链标记后,会被 26S 蛋白酶体识别并降解。比如细胞周期蛋白(Cyclin)在周期结束时被 K48 泛素化降解,推动细胞周期前进。
中间:DNA损伤修复。在 DNA 双链断裂时,K63 泛素链会招募修复蛋白(如 RPA、Rad51)到损伤位点,促进同源重组修复;
右图:介导线粒体自噬。当线粒体功能受损或细胞处于饥饿等应激状态时,细胞会通过这个机制清除 “不合格” 的线粒体,以维持能量代谢和细胞稳态。
(3)异型 / 分支多泛素化(Heterotypic/branched polyubiquitination)
定义:泛素链中包含多种连接方式(如 K11 和 K48 混合,或 K48 和 K63 混合),形成更复杂的分支结构。
功能:这种 “组合标签” 可以传递更精细的信号,常参与细胞周期调控等复杂过程。
左图:调控细胞周期。在有丝分裂后期,周期蛋白 Cyclin B 的降解需要 K11 和 K48 混合连接的泛素链。这种分支结构比单一 K48 链更高效地触发降解,确保细胞周期精准推进。
右图:调控信号传递。例如在 IL-1β 受体激活的下游,K11 和 M1 混合的泛素链可以同时调控信号传递和蛋白降解,让炎症反应既被激活又能被及时终止。
除了泛素化以外,还有几种翻译后修饰也和泛素化的机制类似,只是通过不同的E1,E2,E3酶介导,并使用了不同的小分子。例如接下来为大家介绍的SUMO化和犹素化。
类别
产品
货号
K-ε-GG Rabbit Polyclonal Antibody
Premium Anti-K-ε-GG agarose Beads
3、SUMO化
- SUMO化机制:SUMO 化是类泛素修饰(Small Ubiquitin-like Modifier),将 SUMO 蛋白(主要有 SUMO1-4)共价连接到靶蛋白赖氨酸残基,修饰过程与泛素化类似但使用专属酶系,以单修饰或多聚修饰为主。
和泛素化类似,SUMO化也包括以下几个阶段:
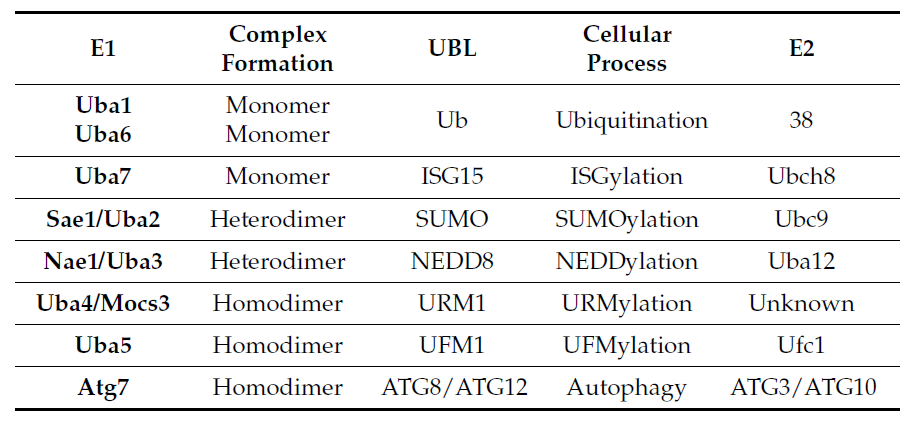
(1)激活:SUMO 激活酶(SAE1/SAE2 异二聚体,类似 E1)激活 SUMO 分子。
(2)结合:激活的 SUMO 转移至 SUMO 结合酶(Ubc9,唯一已知 E2)。
(3)连接:SUMO 连接酶(E3,如 PIAS 家族、RanBP2 等)介导 SUMO 与靶蛋白结合,部分靶蛋白可在 Ubc9 介导下直接发生 SUMO 化(无 E3 参与)。
(4)去修饰:SUMO 特异性蛋白酶(SENPs)可移除靶蛋白上的 SUMO,实现修饰的动态调控。
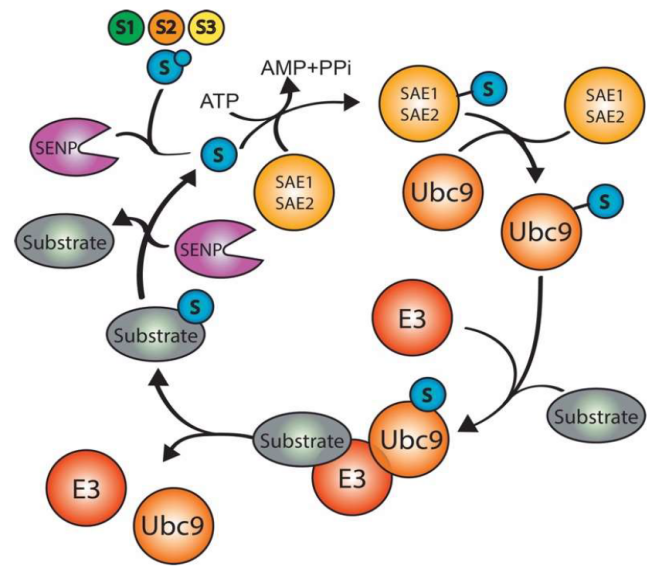
- 生物学功能:
根据E3连接酶特异性识别的底物不同,SUMO化介导不同的细胞功能,例如转录调控,细胞应急应答,亚细胞定位,信号通路调控等。具体见下图:
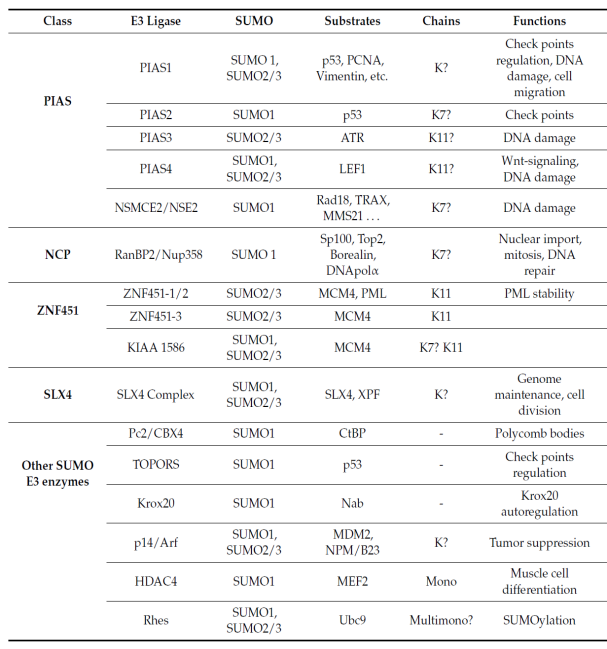
4、犹素化
- 犹素化机制:
犹素化是类泛素修饰(UFMylation),将犹素分子(UFM1,Ubiquitin-fold modifier 1,含 85 个氨基酸的保守小分子蛋白)共价连接到靶蛋白赖氨酸残基,修饰以单修饰或多聚修饰(主要通过 K69 位点形成多聚链)为主。
和泛素化类似,犹素化也包括以下几个阶段:
(1)成熟:UFM1 前体(Pro-UFM1)经犹素特异性蛋白酶(UFSP1/UFSP2)切割 C 端氨基酸,暴露 C 端甘氨酸,形成成熟 UFM1。
(2)激活:犹素激活酶(E1,UBA5)利用 ATP 能量激活 UFM1,形成高能硫酯键(UBA5‑UFM1 复合物)。
(3)结合:激活的 UFM1 转移至犹素结合酶(E2,UFC1,唯一已知 E2),形成 UFC1‑UFM1 硫酯复合物。
(4)连接:犹素连接酶(E3,UFL1,常与 UFBP1/DDRGK1、CDK5RAP3 形成复合物)介导 UFM1 与靶蛋白赖氨酸残基形成异肽键;目前未发现无 E3 参与的直接连接案例。
(5)去修饰:犹素特异性蛋白酶(UFSP1/UFSP2)移除靶蛋白上的 UFM1,实现修饰的动态可逆调控
- 生物学功能:
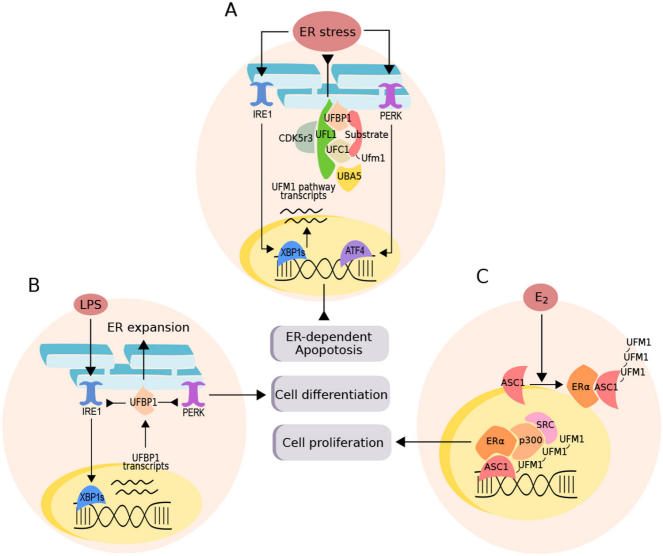
如下图所示,犹素化主要介导内质网应激,细胞分化和细胞增殖等生物学功能。
A图:介导内质网应激。这是犹素化最经典的生物学功能。内质网应激(ER stress)激活内质网膜上的 IRE1 和 PERK 两条信号通路,并引发犹素化级联反应:UFM1 经过 UBA5(E1 激活酶)、UFC1(E2 结合酶)和 UFL1(E3 连接酶)的催化,最终结合到底物蛋白上。UFBP1作为核心底物和支架蛋白,它的犹素化是整个通路的关键节点。CDK5R3与 UFL1 形成复合物,辅助完成修饰过程。最终激活下游XBP1s 和 ATF4 等转录因子,启动内质网应激应答(UPR),并最终调控内质网依赖的凋亡、细胞分化和增殖。
B图:介导细胞分化。脂多糖(LPS,革兰氏阴性菌的细胞壁成分)诱导内质网扩张(ER expansion)。LPS 激活 IRE1 通路,促进 UFBP1 的转录和表达,进而增强犹素化水平。通过下游 XBP1s 调控基因表达,参与免疫细胞的分化与增殖,从而调控炎症反应。
C图:介导细胞增殖。雌激素(E₂)结合其受体 ERα。ERα 招募 ASC1、p300 和 SRC 等共激活因子,ASC1 随后发生犹素化修饰。犹素化修饰增强了 ERα 的转录激活活性,调控雌激素靶基因的表达,影响细胞增殖等生理过程。
5、DNA甲基化
- DNA甲基化机制:
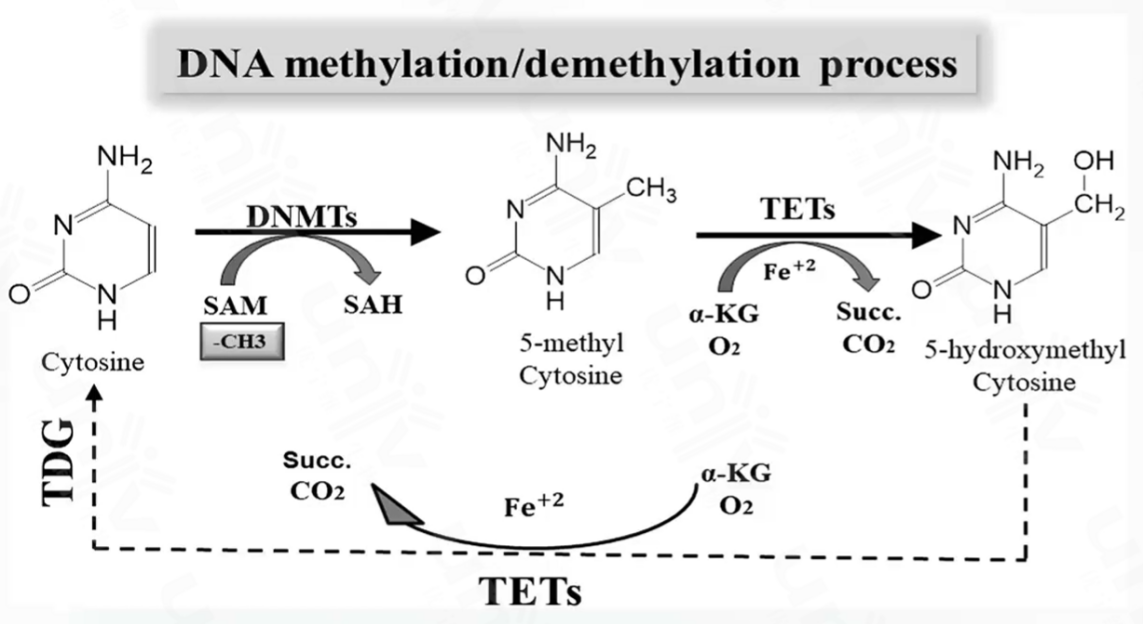
DNA甲基化是指在DNA甲基转移酶的催化作用下,将SAM上的甲基共价连接到CpG位点上的胞嘧啶(C)上的过程。
主要包括以下几个阶段:
· 第一步氧化:TET 酶(需要 Fe²⁺、α- 酮戊二酸(α-KG)和 O₂作为辅助因子)将 5 - 甲基胞嘧啶氧化为5 - 羟甲基胞嘧啶(5-hydroxymethyl Cytosine)。
· 后续氧化:TET 酶可以继续催化 5 - 羟甲基胞嘧啶,生成 5 - 甲酰基胞嘧啶和 5 - 羧基胞嘧啶。
· 碱基切除修复(BER):TDG(胸腺嘧啶 DNA 糖苷酶)识别并切除这些氧化后的胞嘧啶衍生物,再通过 DNA 修复机制替换为未修饰的胞嘧啶,完成去甲基化。
- 生物学功能
哺乳动物DNA甲基化主要发生在CpG位点的胞嘧啶(C)上,CpG位点以两种形式存在:
(1)分散于基因组序列中,70%-80%被甲基化。(2)呈现高度聚集状态,即CpG岛。甲基化主要具有抑制基因转录,抑制转座子活性,参与DNA损伤修复,介导细胞衰老与分化,参与代谢调控等过程。
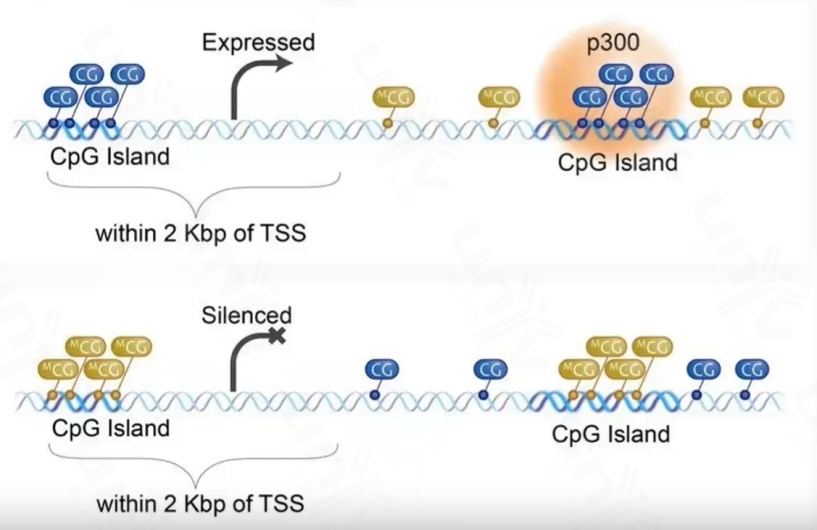
下图展示了CpG岛甲基化调控过程。 CpG 岛(CpG island)是指在基因的启动子区域,常常存在一段富含 CpG 序列的区域,称为 CpG 岛。如果这些 CpG 岛被高度甲基化,就会抑制基因的转录,导致基因沉默;反之,去甲基化则会激活基因表达。
上图:介导基因表达。启动子区域的 CpG 岛未甲基化(蓝色标记的 CpG 位点),此时转录因子和辅助激活因子(如 p300)可以结合到这些位点上,启动基因的转录。
下图:介导基因沉默。启动子区域的 CpG 岛高度甲基化(黄色标记的 mCG),甲基化会阻止转录因子和激活因子的结合,同时招募甲基化结合蛋白(如 MeCP2),进一步压缩染色质结构。
类别
产品
货号
Methacryllysine Recombiant Mouse mAb (S-3455)
Histone H3 (di methyl K14) Recombinant Rabbit mAb (S-R414)
Di-Methyl-Histone H3 (Lys9) (D85B4) Rabbit Monoclonal Antibody
Mono-Methyl-Histone H3 (Lys4) (D1A9) Rabbit Monoclonal Antibody
相关新闻资讯