
2YR企业会员
发布人:普健生物(武汉)科技有限公司
发布日期:2026/2/4 10:26:22
FMDV 的病毒粒子呈二十面体对称,直径约 25-30nm,核心为单股正链 RNA 基因组,全长约 8.5kb,编码P1、P2、P3 三大前体蛋白。其中 P1 前体经 3C 蛋白酶切割形成 VP1-VP4 四种结构蛋白,共同组装成病毒衣壳,而 VP1 表面的 G-H 环是主要抗原位点,也是中和抗体的关键靶点。FMDV存在7种主要血清型(O、A、C、Asia 1、SAT1-3)及众多亚型,不同血清型间无交叉免疫保护,且病毒RNA复制过程易发生突变,导致新变异株持续出现,这也是传统疫苗防控的主要障碍。
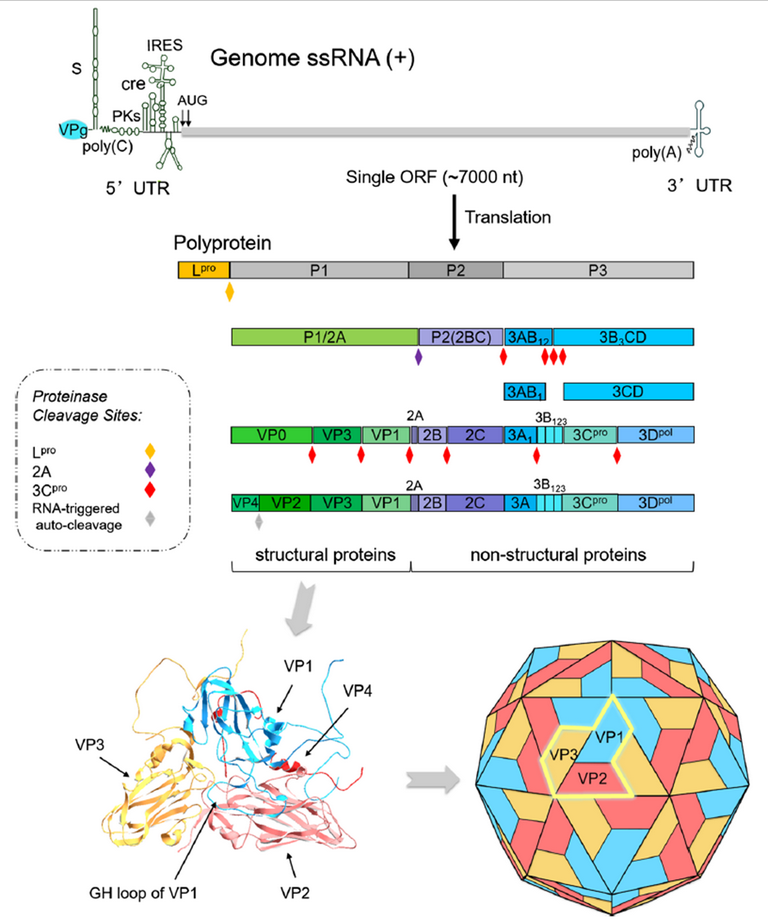
Figure 1. 口蹄疫病毒(FMDV)基因组、病毒多肽加工及结构蛋白构象
借助Diamond 同步加速器的X射线晶体学与冷冻电镜技术,研究团队成功解析了 FMDV 衣壳的三维结构,发现其稳定性依赖于亚基间的疏水作用与二硫键。这一发现为 VLP 疫苗设计提供了关键依据——通过在VP2蛋白的 H2093 位点引入半胱氨酸突变,可形成额外二硫键,显著增强衣壳稳定性,解决了传统VLP易解离的技术瓶颈。
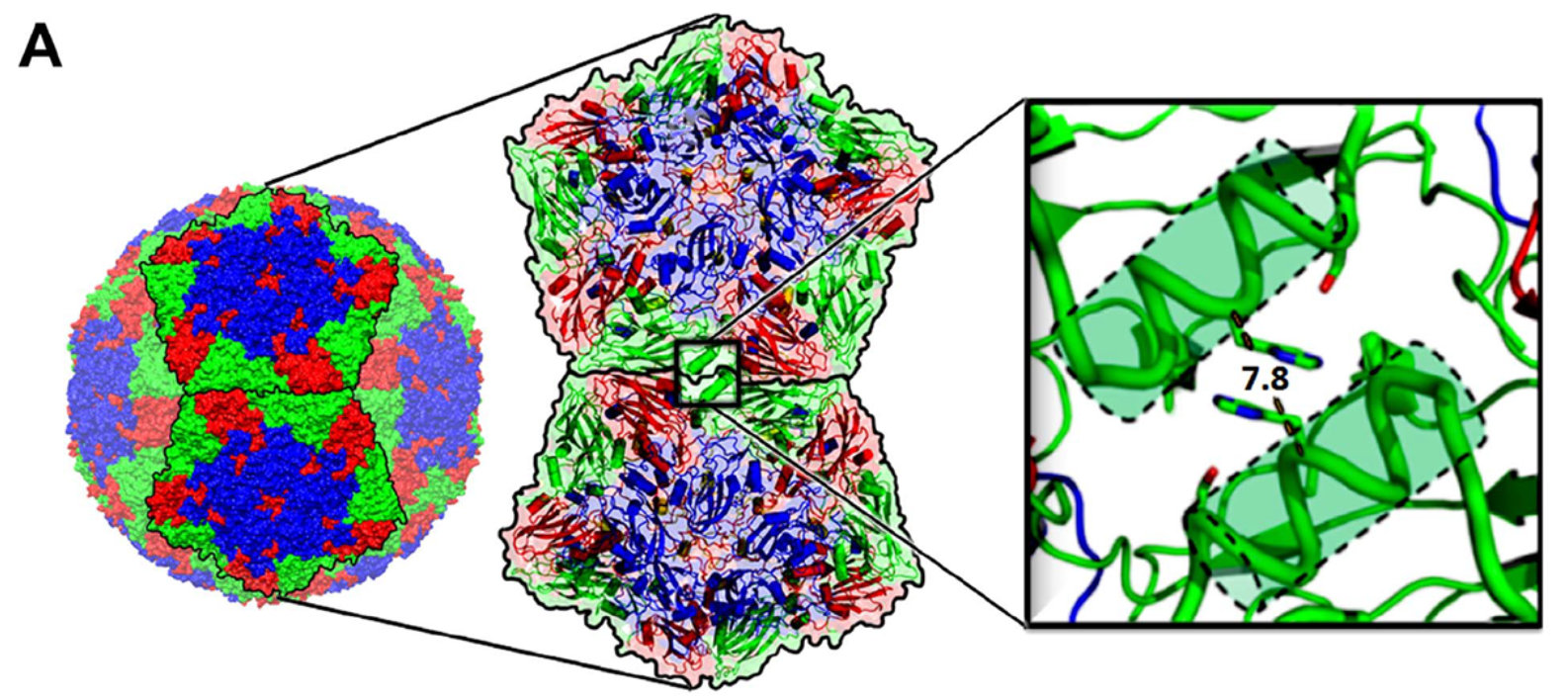
Figure 2. 用于生产稳定空衣壳的FMDV A22的合理设计
FMDV 是已知传染性最强的动物病毒之一,其基本再生数(R₀)在牛群中可达 2.52-14,小型实验中甚至出现无限传播的极端情况。病毒主要通过直接接触、呼吸道飞沫及污染物传播,侵入宿主后首先在口腔黏膜、蹄部上皮细胞中复制,随后通过血液循环扩散至全身。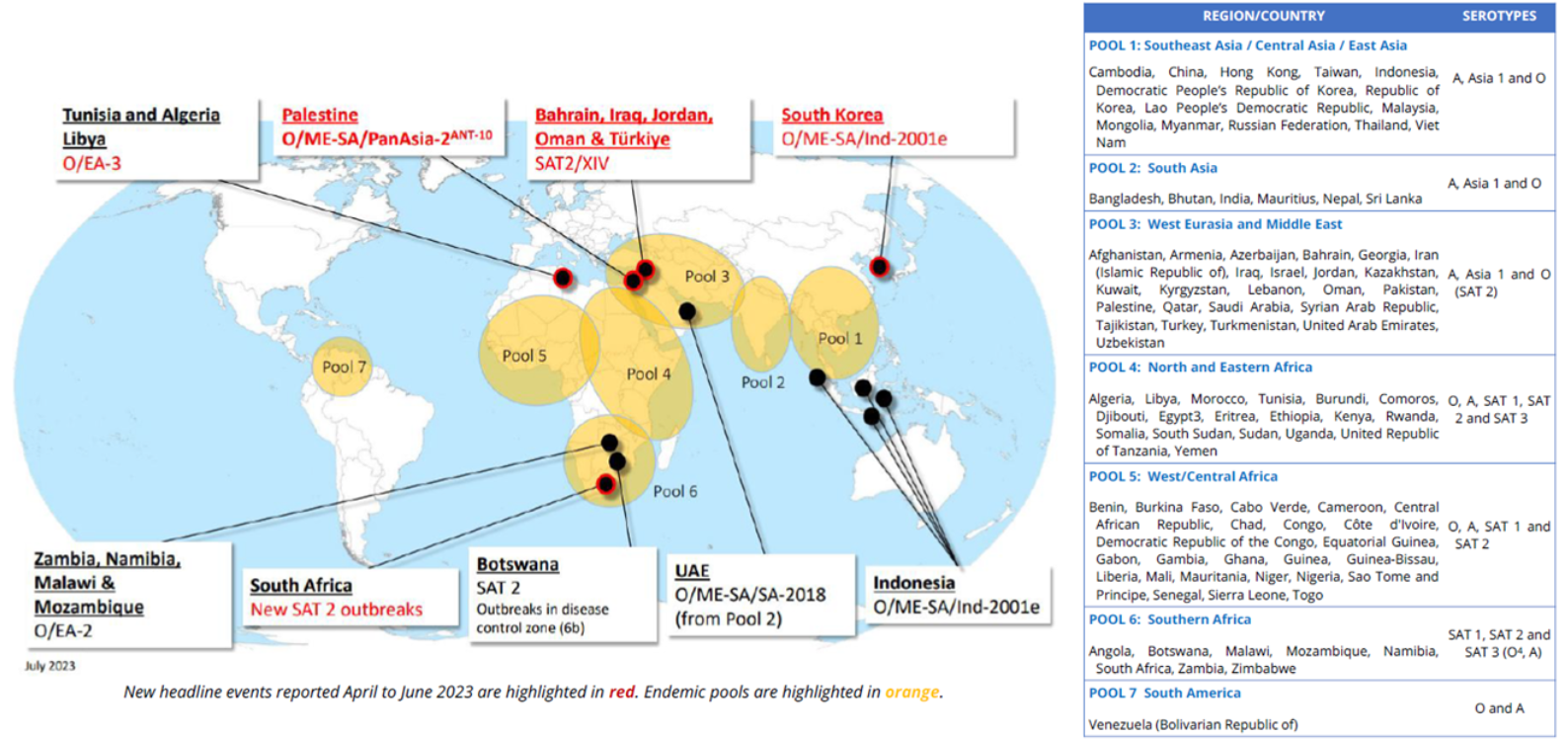
Figure 3. FMD的地理分布和最近全球爆发情况
致病过程中,FMDV 的 VP1 蛋白与宿主细胞表面的整合素αvβ6结合,介导病毒内化,其复制会导致上皮细胞坏死脱落,形成特征性的口腔水疱、蹄部溃烂症状。虽然成年动物死亡率较低,但会引发严重的生产损失:泌乳奶牛产奶量下降 20%-80%,育肥动物体重减轻 10%-25%,繁殖动物流产率升高至 28.8%,且感染动物的牵引能力丧失可持续 20 天以上。更严重的是,病毒可在非洲水牛等野生动物中持续存在,形成自然疫源地,给疫病根除带来巨大挑战。
Figure 4. FMDV非结构蛋白在细胞调控中的已知功能
Diamond Light Source支持的FMD-VLP 疫苗项目:根据CSIL 2023年影响报告,由Diamond Light Source、Pirbright研究所、牛津大学、雷丁大学与MSD Animal Health合作开发的病毒样颗粒(VLP)疫苗,目前正处于监管审批阶段。生产预计在未来几年内启动。该疫苗基于之前文献的理性工程设计(引入H2093C等突变增强稳定性),并通过Diamond 的X 射线晶体学和冷冻电镜技术优化,已证明在动物试验中安全有效,提供热稳定性、DIVA 兼容性和无需活病毒生产的优势。2026年1月Diamond 新闻强调,该疫苗若实现20%市场渗透,可每年带来超过13亿美元全球畜牧收益,并显著提升粮食安全。
E. coli表达系统:2025年韩国研究报道,使用E. coli 生产的O型FMDV VLP 疫苗,在小鼠和猪模型中显示高存活率(1/10和1/160剂量下100%保护),并计划推进到目标牲畜种的大规模试验和监管审批。该平台强调安全性与可扩展性。
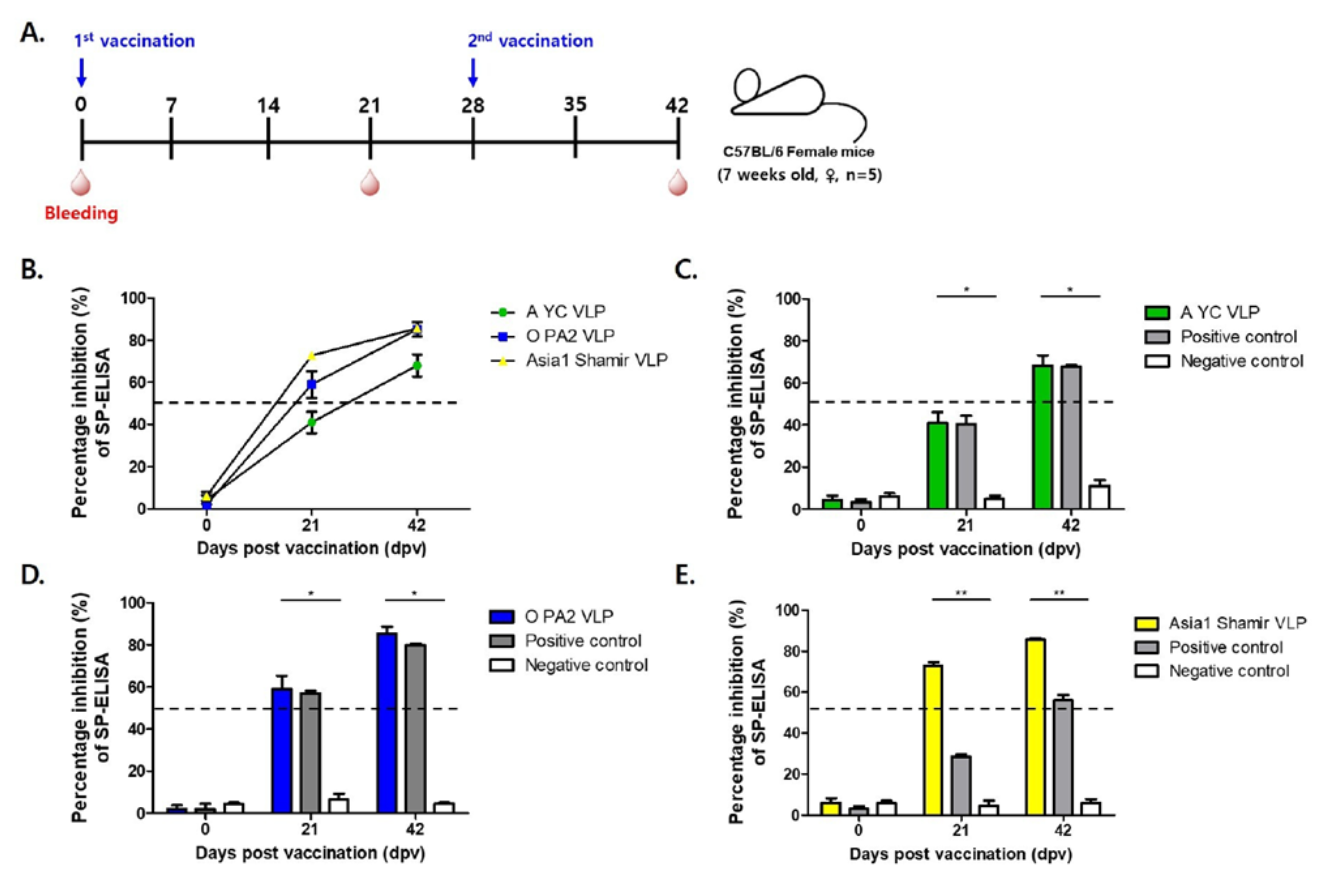
Figure 5. 接种重组FMDVLP抗原的小鼠的免疫原性
腺病毒载体增强型:2025年多项研究开发了腺病毒表达的FMDV VLP 疫苗,融入CD154分子佐剂或Fc融合,提升猪模型中的免疫应答和交叉中和能力。Ad5-FMDV VLP-sFc 变体显示出更强的体液和细胞免疫。
Figure 6. FMDV VLP表达载体的确认
SAT型和多血清型优化:2025年Veterinary Research 综述聚焦SAT 型FMDV VP1 表位演化,强调VLP 疫苗在小鼠和牛模型中的潜力(如SAT2 VLP 达4.33 PD50/剂,超过OIE标准)。结合结构洞见(如cryo-EM验证),支持候选疫苗选择和抗原优化。
新兴平台:2025年研究探索植物基、纳米颗粒和肽疫苗作为补充,但尚未达到监管审批阶段。整体趋势是向无活病毒、热稳定、多血清型覆盖的下一代疫苗转型。
口蹄疫病毒(FMDV)研究热点持续聚焦于病毒-宿主交互的核心机制,以推动更有效的疫苗、抗病毒策略和全球控制。当前研究的热门靶点包括:
VP1蛋白及其表位:作为病毒附着和主要免疫原的关键结构蛋白,VP1的G-H环(GH loop,含RGD基序)是经典中和表位靶点,但其高变异性导致抗原漂移和疫苗匹配挑战。近期研究强调VP1的B/T细胞表位映射、重组表达和多价设计,以实现广谱保护。
非结构蛋白(NSPs):特别是Lpro、3Cpro、3Dpol和3A蛋白,作为免疫逃逸和病毒复制的核心调控者。Lpro和3Cpro通过切割宿主因子(如eIF4G、RIG-I/MDA5)抑制IFN途径;3Dpol靶向STAT2抑制IFN信号;3A干扰宿主膜重排和宿主范围决定。这些靶点是开发广谱抗病毒药物或增强型疫苗(如DIVA兼容VLP)的优先方向。
免疫逃逸与持久感染机制:病毒通过干扰JAK-STAT、NF-κB和IRF3途径逃避免疫监视,促进载体状态(尤其是牛)。野生动物宿主(如非洲水牛)和病毒-宿主交互决定毒力,是跨界传播研究热点。
这些靶点研究正从基础结构生物学(如Diamond同步辐射解析)向转化应用转型,强调“One Health”框架下多血清型、热稳定、无活病毒疫苗的开发,以应对全球流行和经济损失。
以下为 abinScience 针对FMDV相关的重组蛋白与抗体新产品,目录号可直接点击进入产品页。
1、Dong H, Liu P, Bai M, et al. Structural and molecular basis for foot-and-mouth disease virus neutralization by two potent protective antibodies. Protein Cell. 2022;13(6):446-453. doi:10.1007/s13238-021-00828-9
2、Park JY, Lee HM, Kang KJ, et al. Development and immunogenicity of adenoviral Fc-fused FMDV virus-like particle vaccine in swine. Vet Q. 2025;45(1):2564443. doi:10.1080/01652176.2025.2564443
3、Kotecha A, Seago J, Scott K, et al. Structure-based energetics of protein interfaces guides foot-and-mouth disease virus vaccine design. Nat Struct Mol Biol. 2015;22(10):788-794. doi:10.1038/nsmb.3096
4、Porta C, Kotecha A, Burman A, et al. Rational engineering of recombinant picornavirus capsids to produce safe, protective vaccine antigen. PLoS Pathog. 2013;9(3):e1003255. doi:10.1371/journal.ppat.1003255
5、Sultanov AA, Tyulegenov S, Yessembekova GN, et al. The progressive control of foot-and-mouth disease (FMD) in the Republic of Kazakhstan: Successes and challenges. Front Vet Sci. 2023;10:1036121. Published 2023 Apr 17. doi:10.3389/fvets.2023.1036121
6、Li Y, Zeng W, Niu X, et al. Foot-and-mouth disease virus-like particle vaccine incorporating dominant T and B cell epitopes: enhanced immune response in piglets with CD154 molecules. Front Vet Sci. 2025;12:1540102. Published 2025 Feb 19. doi:10.3389/fvets.2025.1540102
7、Gao Y, Sun SQ, Guo HC. Biological function of Foot-and-mouth disease virus non-structural proteins and non-coding elements. Virol J. 2016;13:107. Published 2016 Jun 22. doi:10.1186/s12985-016-0561-z
8、Stenfeldt C, Eschbaumer M, Humphreys J, Medina GN, Arzt J. The pathogenesis of foot-and-mouth disease virus: current understandings and knowledge gaps. Vet Res. 2025;56(1):119. Published 2025 Jun 16. doi:10.1186/s13567-025-01545-5
9、Jiang S, Yang S, Zhang X, et al. Evolutionary and structural insights into VP1 epitopes of representative SAT-type FMDV strains: implications for candidate vaccine selection. Vet Res. 2025;56(1):227. Published 2025 Dec 15. doi:10.1186/s13567-025-01643-4
10、Elrashedy A, Mousa W, Nayel M, et al. Systematic review and meta-analysis of the effectiveness of polypeptide, virus-like particles, and viral vector vaccines for foot-and-mouth disease (2020-2025). Sci Rep. 2025;15(1):39370. Published 2025 Nov 10. doi:10.1038/s41598-025-24078-5
11、Yu SC, Lee IK, Kong HS, et al. Foot-and-Mouth Disease Virus-like Particles Produced in E. coli as Potential Antigens for a Novel Vaccine. Vet Sci. 2025;12(6):539. Published 2025 Jun 2. doi:10.3390/vetsci12060539
相关新闻资讯