
5YR企业会员
发布人:广州优南科技有限公司
发布日期:2024/10/18 10:19:19
上半年,FDA批准多款具有里程碑意义药物,看点颇多:
40年来首款非酒精性脂肪性肝炎药物Rezdiffra获批上市;时隔32年,又一款应用于肿瘤免疫治疗的细胞因子药物Anktiva获批上市等等。
截至目前,2024年上半年CDER批准了18个新分子实体,其中包括13款化药新药和5款生物药新药。值得一提的是,今年上半年的新药获批数量明显少于去年,2023年同期已有20多款新分子实体获批,主要是化药新药上市数量减少(去年同期有17款化药新药上市)。
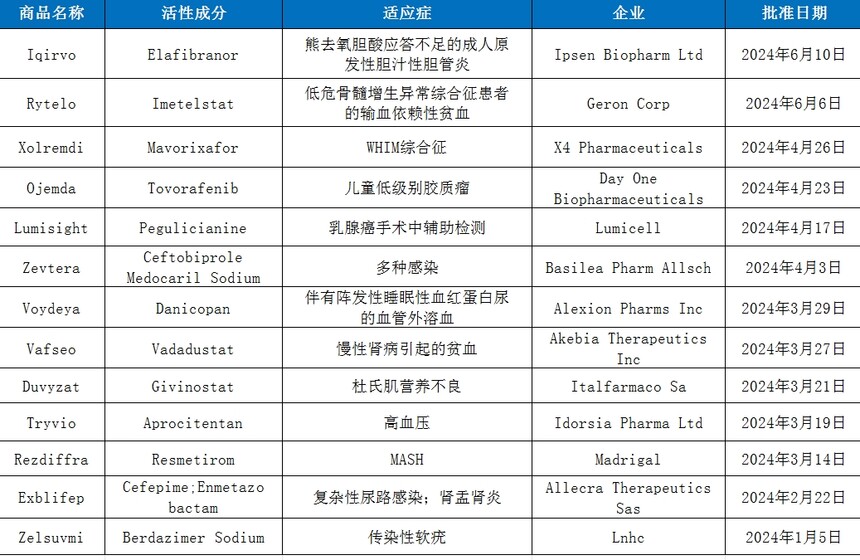
数据来源:FDA、药智数据
从审批方式看,获批的13款新化药中Iqirvo、Xolremdi、Ojemda等8款药物是通过优先审评上市,与NDA标准审批需要10个月相比,优先审评需在6个月内完成,节省了企业的时间成本,同时优先审评的药物具有更高的治疗价值。
从适应症上来看,代谢类疾病治疗领域有4款,肿瘤领域有3款,免疫治疗领域有2款,抗感染领域有2款,神经系统和其他领域各1款。在获批的化药新药中孤儿药有6款,占比接近一半,可见罕见病研发领域依旧火热。
下面简要介绍几款获批上市的新化药。
Iqirvo(Elafibranor)
6月10日,益普生宣布美国FDA已加速批准Iqirvo,Iqirvo是同类首创的口服、每日一次的过氧化物酶体增殖激活受体(PPAR)激动剂,用于治疗对UDCA应答不足的成人原发性胆汁性胆管炎(PBC),或作为单药疗法治疗对UDCA不耐受的患者。这是近十年来首个获批治疗罕见肝病原发性胆汁性胆管炎的新药。
PBC是因为胆管的慢性损伤,导致清除毒素的能力下降,引发肝硬化和肝功能衰竭。根据关键性3期试验ELATIVE结果显示只有接受elafibranor治疗的患者在第52周碱性磷酸酶(ALP)达到正常值,与对照组相比降低幅度达到41%。目前治疗罕见自身免疫性PBC患者、治疗PBC的炎症、胆汁淤积和纤维化等研究正在进行。值得一提,同靶点药物Seladelpar,已获得FDA优先审评资格,预计8月份公布审评结果。
Rytelo(Imetelstat)
6月6日,Geron Corporation的Rytelo被FDA获批上市,用于治疗低危骨髓增生异常综合征(LR-MDS)患者的输血性依赖性贫血。MDS指阻碍血液(造血)干细胞成熟为健康血细胞的一组癌症,是一种罕见的血癌。如果患者体内没有足够的健康血细胞,可能会出现贫血、频繁感染和失控出血等严重疾病。
Rytelo是一款first in class端粒酶抑制剂,Imetelstat通过结合并抑制端粒酶,从而调控恶性造血干细胞的凋亡。1990年Geron成立,从开始研发端粒酶抑制剂到Rytelo上市,Geron花了30多年,在经历一系列的失败之后,Imetelstat终于在MDS上有了用武之地;3期IMerge研究显示Imetelstat治疗后无需输血的比例显著高于安慰剂组。
Xolremdi(Mavorixafor)
4月26日,X4 Pharmaceuticals公司宣布美国FDA批准Xolremdi(mavorixafor)胶囊上市,用于治疗12岁及以上患有WHIM综合征的患者,以增加血液循环中成熟中性粒细胞和淋巴细胞的数量。这是首款获批针对WHIM综合征患者的小分子疗法。WHIM综合征是一种罕见的原发性免疫缺陷和慢性中性粒细胞减少症,由CXC趋化因子受体4(CXCR4)信号通路障碍引起。
Xolremdi是一种选择性CXCR4拮抗剂,关键3期临床4WHIM研究结果显示,与安慰剂相比,Xolremdi治疗显著增加了中性粒细胞计数(ANC)水平超过阈值(≥500细胞/微升)和绝对淋巴细胞计数(ALC)水平超过阈值(≥1000细胞/微升)的持续时间,安全性良好。此前,Xolremdi已经被FDA授予突破性疗法认定。
Ojemda(Tovorafenib)
4月23日,FDA加速批准Day One Biopharmaceuticals开发的泛RAF激酶抑制剂Ojemda(tovorafenib)上市,用于治疗6个月及以上的复发或难治性儿童低级别胶质瘤(pLGG)患者,这些患者存在BRAF融合或重排,或BRAF V600突变。Ojemda是用于治疗该疾病的全身疗法,它能够抑制携带BRAF融合或BRAF V600突变的肿瘤的生长,并且具有大脑渗透性。先前被FDA授予突破性疗法和罕见儿科疾病资格,这也是基于FIREFLY-1临床2期试验数据获批的原因之一。
儿科低级别胶质瘤是儿童中最常见的脑瘤,在美国,儿童LGG年发病率为每十万人1.3~2.1例,预计每年有1000-1600例新发病例。2023年3月16日,FDA批准了诺华的BRAF/MEK组合即Tafinlar(dabrafenib,达拉非尼)联合Mekinist(trametinib,曲美替尼),这是pLGG的首个靶向疗法。
Rezdiffra(Resmetirom)
3月14日,MASH治疗领域迎来重大进展,FDA批准Madrigal的口服小分子药物Rezdiffra用于治疗伴有中度至晚期肝瘢痕形成(纤维化)的代谢功能障碍相关脂肪性肝炎成人患者,配合饮食、运动一起使用。这是40年来首款获批上市的MASH药物。
Resmetirom是一款甲状腺激素受体(THR)-β口服选择性激动剂。THR-β在人体肝脏中高表达,能够调节脂代谢,降低LDL-C、甘油三酯和致动脉粥样硬化性脂蛋白,THR-β还可以通过促进脂肪酸的分解和刺激线粒体的生物发生来减少脂肪毒性并改善肝功能,进而减少肝脏脂肪。
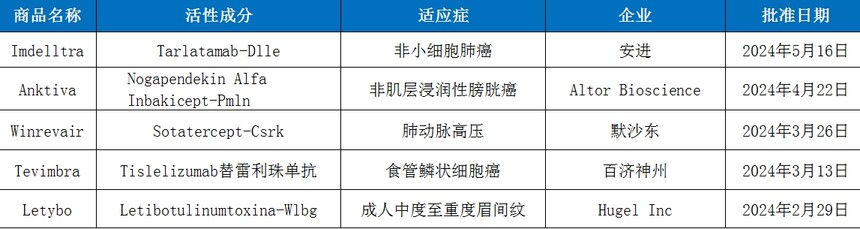
数据来源:FDA、药智数据
截至目前,2024年上半年CDER共批准了5款生物药新药,1款双抗(Imdelltra),1款细胞因子药物(Anktiva),1款融合蛋白(Winrevair),1款单克隆抗体(Tevimbra),1款神经毒素(Letybo)。
从治疗领域来看,在获批的5款生物药新药中,占比最多是癌症治疗领域,有Imdelltra、Anktiva、Tevimbra 3款新药上市,值得注意的是国产创新药企百济神州的Tevimbra(替雷利珠单抗)成功登陆美国市场成为第二款在美上市的PD-1药物;代谢领域有一款Winrevair,另外还有一款医美药物Letybo上市。
Anktiva
4月22日,ImmunityBio公司宣布FDA已经批准Anktiva联合卡介苗(BCG),用于治疗卡介苗不响应的非肌层浸润性膀胱癌(NMIBC)伴原位癌(CIS),伴或不伴乳头状瘤患者,成为全球首个获批的白细胞介素-15(IL-15)药物,这是美国FDA时隔32年后批准的又一款应用于肿瘤免疫治疗的细胞因子药物,也是历史上的第三款。
Anktiva是一种IL-15超激动剂复合物,由IL-15突变体与IL-15Rαsushi结构域以及IgG1 Fc融合蛋白结合而成,IL-15Rαsushi结构域使其无需像天然IL-15通过反式呈递就可以激活下游信号通路,且IgG1-Fc片段极大延长了药物半衰期。
Winrevair
3月26日,FDA批准了默沙东Winrevair治疗肺动脉高压(PAH)的上市申请,PAH是由于促进和抑制增生信号的不平衡导致肺动脉壁的血管增厚,限制血流,使得心脏右侧负担日渐加重,最终导致心力衰竭。
Winrevair是首个获批的PAH的激活素信号抑制剂疗法,该药物全年费用高达24.2万美元,据有关机构估计年销售峰值可达75亿美元。
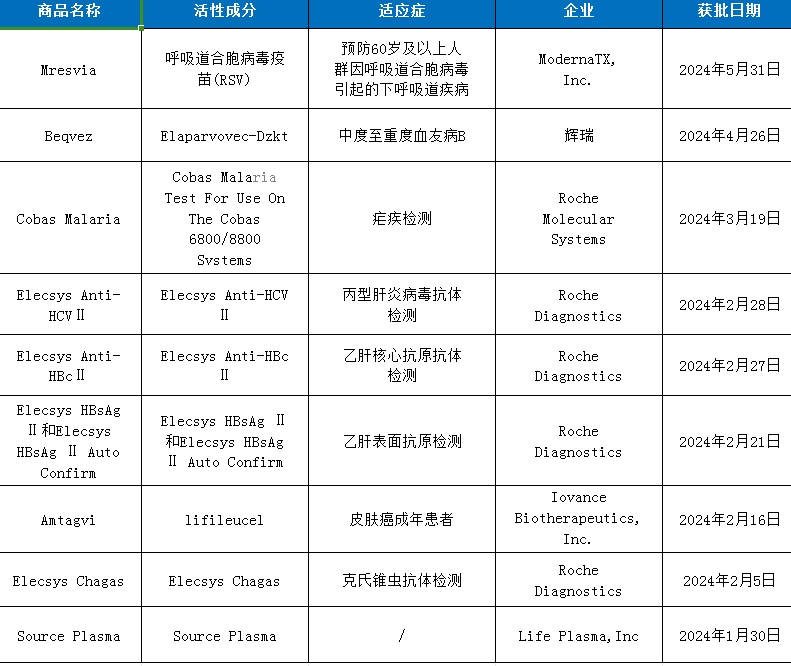
数据来源:FDA、药智数据
截至目前,CBER批准了9款生物制品,其中包括一款RSV疫苗(Mresvia),一款基因疗法(Beqvez),一款细胞疗法(Amtagvi),还有多款疾病诊断技术和血液制品。
Beqvez(Elaparvovec-Dzkt)
4月26日,辉瑞宣布FDA已批准Beqvez上市,Beqvez是一种基于腺相关病毒(AAV)载体的基因疗法,用于治疗中度至重度血友病B且对AAV血清型Rh74的中和抗体检测为阴性的成年(18岁及以上)患者。据悉Beqvez定价为350万美元,能通过一次性治疗产生自体的凝血因子IX蛋白,目前的标准治疗则需要定期输注凝血因子IX。
Amtagvi(Lifileucel)
2月16日,Iovance Biotherapeutics宣布,FDA已通过加速批准Amtagvi上市,lifileucel是一种肿瘤浸润淋巴细胞(TIL)治疗方案,用于治疗PD-1/PD-L1治疗后进展的晚期黑色素瘤。
Lifileucel是全球首款获批上市的TIL细胞疗法,该疗法从肿瘤细胞中分离浸润的淋巴细胞,在体外扩增后像CAR-T疗法样回输给患者,可以特异性识别患者的肿瘤细胞进行杀伤。根据C-144-01研究已读出的结果显示,队列4的73名患者中31.5%的患者达到客观缓解。
结语
今年上半年,美国FDA批准的新药中抗肿瘤、自免、代谢、抗感染和罕见病仍是热点领域,与去年相比肿瘤药物占比明显提高,这表明肿瘤药物仍是药物研发的热点。在获批的化药新药中罕见病药物占比接近一半,在FDA的政策鼓励下,可见药企对罕见病治疗药物的研发热情依然高涨,另外MASH治疗领域的突破和多款FIC药物获批同样令人欣喜。突破还在继续,2024下半年同样不平凡。6月11日,礼来公司的阿尔茨海默病药物donanemab,被药物咨询委员会以11:0的票数一致赞同该药物的有效性,预计不久也将获批上市。
除此之外,FDA又会批准哪些药物呢,我们拭目以待!
参考资料:
1.药智数据、FDA
2.各企业官网
3.近十年首款!Ipsen又一罕见肝病新药获FDA加速批准。(药明康德)
4.40年来首款非酒精性脂肪性肝炎创新药获FDA批准上市(澎湃新闻)
5.全球首个IL-15药物获批!ImmunityBio的Anktiva获FDA批准用于治疗卡介苗不响应的非肌肉浸润性膀胱癌(凯莱英新闻)
转载链接:2024上半年FDA批准的新药_腾讯新闻 (qq.com)
如有侵权请联系我们,我们将会删除。
相关新闻资讯