乙二醇是最简单的脂肪族二元醇。无色粘性透明液体。有甜味。易吸水。相对分子质量62.07。相对密度1.1155。熔点-11.5℃。沸点197.6℃、 140℃(12.932× 103Pa)、109℃(3.333×103Pa)、100℃(2.400×103Pa)、93℃(1.733×103Pa)、70℃ (0.400×103Pa)、20℃(0.00800×103Pa)。折射率1.4319。闪点115℃。燃点380℃。粘度20.93mPa·s (20℃)。难溶于苯 、二硫化碳、氯仿、石油醚、四氯化碳,微溶于乙醚(20℃时7.89),能与水、乙醇、甘油、醋酸、丙酮、乙醛和吡啶等相混溶。乙二醇具有一元醇的某些化学性质,如 能生成醚、酯,能被氧化,还能缩合。它与硝酸反应生成的乙二醇二硝酸酯是一种炸药。乙二醇的最大用途是合成纤维“涤纶” 等高分子化合物。乙二醇二硝酸酯与硝化甘油联合使用可使炸药的冻点降低。乙二醇还可用做药品和塑料的原料、高沸点溶剂及防冻剂。
1859年法国C.A.孚兹首次在实验室制得乙二醇,但未得应用。19世纪初,因硝化甘油炸药的需要,1917年和1919年美国和德国先后建成了工业生 产装置。随着汽车工业的发展和聚酯纤维(涤纶)的兴起,促进了乙二醇生产的发展。至20世纪90年代末,世界乙二醇生产能力达1577.6万t。 其中美国432.6万t,沙特阿拉伯114万t。2000年中国生产了90.75万t。现在,乙二醇已不用于炸药。它主要用于聚酯纤维和聚酯工程塑料, 占总消费量50%以上,35%~40%用于生产醇酸树脂(涂料用)、人造丝防缩剂、增塑剂、防冻剂等。在美国作为汽车散热器的冷却液(用以防冻) 的用量占其消费量的30%以上。
【应用领域】
乙二醇主要用于配制汽车冷却系统的抗冻剂和飞机发动机致冷剂及生产聚对苯二甲酸乙二酯 (聚酯纤维和聚酯塑料的原料),也可用作生产其他合成树脂、溶剂、润滑剂、表面活性 剂、软化剂、增湿剂、炸药等,还可合成涤纶纤维等高分子化合物。乙二醇二硝酸酯与硝化甘油联合使用可使炸药的冻点降低。乙二醇还可作为药品和塑料的原料及高沸点溶剂。
1980年美国用于抗冻剂的乙二醇与用于生产聚酯的消费量相等。用于抗冻剂的乙二醇一般纯度要求不高。
乙二醇常可代替甘油使用。在制革和制药工业中分别用作水合剂和溶剂。
乙二醇有许多重要的衍生物。低分子量的聚乙二醇 (一缩乙二醇、二缩乙二醇、三缩乙二醇或分别称二甘醇、三甘醇、四甘醇)实际上是环氧乙烷水合制乙二醇的副产物。二甘醇可 用作增湿剂、增塑剂、上浆剂、印刷油墨溶剂、天然脱水干燥剂和芳烃萃取溶剂。高分子量聚乙二醇根据分子量的不同,从无色透明粉稠液 体到蜡状固体,也是一类有用的衍生物,用作润滑剂、水分保持剂、溶剂以及橡胶和食品工业的中间体,亦用于配制化妆品及纺织、造纸等 领域的助剂。
乙二醇的醚和酯的品种很多,广泛用作溶剂。长链脂肪酸的乙二醇酯具有表面改进性能,可单独使用或与其它表面活性剂共用,作为乳化剂、稳定剂、分散剂、增湿剂、发泡剂和 悬浮剂等。
【化学反应】
乙二醇有两个羟基,具有醇类的化学性质,如能生成醚、酯,能被氧化,能缩合。氧化可以生成醛或酸。羟基与羧酸反应生成酯(单酯或双酯)。与醇类缩合生成醚。也可被卤素取 代。与酰氯或酸酐反应,一般均形成双酯。在催化剂(二氧化锰、氧化铝、氧化锌或硫酸)作用下加热,可在分子内或分子间脱水,生成环状乙二醇缩乙醛:
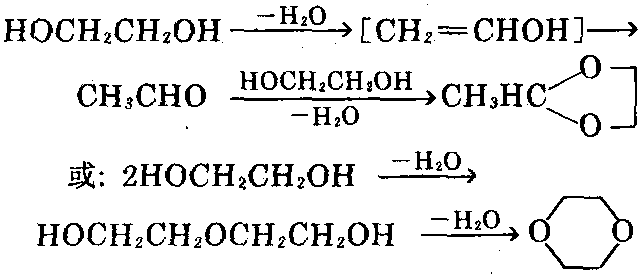
与乙醇一样,也能和碱金属或碱土金属反应,生成醇盐(可以是单盐,也可形成二盐)。当用高碘酸氧化时,可发生断链,用于乙二醇的定量。与 丙酮缩合,生成1,3-二恶烷衍生物。
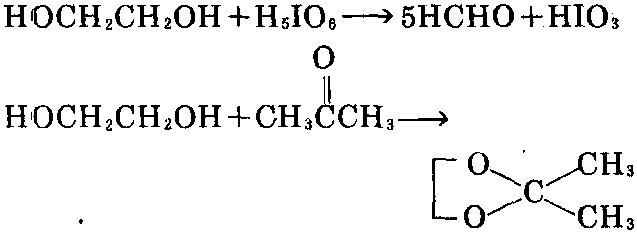
乙二醇与草酸二乙酯反应时,可进行酯交换,生成环状化合物1,4-二恶烷-2,3-二酮。
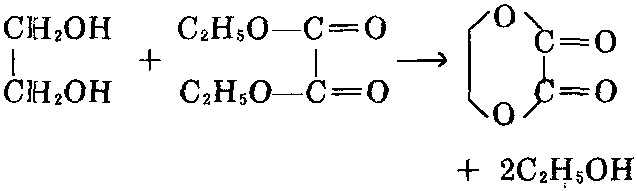
它与硝酸反应生成乙二醇二硝酸酯(一种炸药)。
【毒性】
乙二醇属低毒类。大鼠LD50为5.5ml/kg~8.54ml/kg。人一次口服LD50为80g~100g。血中乙二醇浓度达2.4g/L,可引起急性肾功能衰竭。可由消化道、皮肤及呼吸道吸收。本品挥 发性小,在常温下不能引起呼吸道吸入中毒。主要为口服急性中毒。急性中毒早期症状和急性乙醇中毒相似,继而出现酸中毒。因草酸钙结 晶阻塞肾小管,故急性肾损害较突出。死因主要为急性肾功能衰竭、中枢神经系统抑制呼吸、循环功能衰竭。接触高浓度乙二醇蒸气可发生 昏厥、眼球震颤等。治疗主要是及时纠正酸中毒,防治急性肾损害。必要时及早进行血液净化疗法。防止误服。本品加热时应密闭、排气, 防止吸入本品蒸气或气溶胶。避免皮肤长期直接接触本品。
乙二醇的毒性试验表明,对低级脊椎动物相当安全,无严重毒性,大鼠口服LD50为8540mg/kg。但曾报导有人误服不到50g乙二醇而致死,因为乙二醇进入机体可能转化为草酸,对 人类不安全。本品对中枢神经系统有抑制作用,对肾脏有损害,对粘膜、眼睛有刺激性。
【乙二醇防冻液】
乙醇、乙二醇和甘油(丙三醇)都可用作防冻液。乙醇沸点低,蒸发损失大; 甘油低温粘度太高; 乙二醇是能较好满足以上性能要求的防冻液基本材料。现在的商品防冻液几乎都是 用乙二醇配制的。
化学纯乙二醇与纯水按不同比例混合可以获得冰点从0到-60℃以下的溶液,体积 33.3%的水和66.7%的乙二醇溶液的冰点最低(-75℃)。乙二醇水溶液冻结时形成松散的泥浆状结晶 ,甚至混合液含水55%~65%时,其冻结后的体积亦只增加0.25%~0.30%。因此,乙二醇水溶液即使冷却到冰点温度以下亦不至损坏发动机和 散热器。
工业乙二醇含丙二醇等杂质,带淡黄色。
乙二醇水溶液的热容量和热传导性能优于相应浓度的乙醇或甘油水溶液,但不如水。
乙二醇对金属具有腐蚀作用,商品防冻液内除主剂乙二醇外,必须添加抗腐蚀剂,此外还加入少量水以降低肪冻液的冰点。代表性的防冻液组成为:工业乙二醇90%~95%;添加剂 3%~5%;水0~5%。这种商品防冻液称为永久型防冻液,简称PT型防冻液,它是与易挥发的乙醇或乙醇同甘油混合液作基础液的所谓半永久型 (SPT) 防冻液相对而言。进一步提高永久型防冻液的抗腐蚀性,使其使用期延长到2~3年的产品称为长效防液。这类商品国外加注字头缩写 LLC (Long Life Coolant) 。
【危险情况】 摄入和吸入蒸气均可中毒; 致死量约为100mL。易燃,燃点775℉(412℃)。空气中的容许浓度蒸气美国为50ppm(125mg/m3),微粒为 10mg/m3。
【用途和接触机会】
用作测定水中氧化钙的试剂,色谱分析试剂,电容介质,制冷剂和防冻剂及炸药、蜡、树脂、某些染料的溶剂。水力系统用流体。热交换剂。生产涤纶纤维的主要原料。制造乙二 醇二硝酸酯、乙二醇酯、树脂以及药物的化学中间体。
乙二醇可由消化道、皮肤及呼吸道吸收,以原形或经氧化为乙二酸盐(草酸盐)的形态从肾脏排出。乙二醇氧化成二氧化碳则从呼吸道排出。
尽管乙二醇的毒性较大,但其挥发性很小,故在生产中经吸入而引起严重中毒的可能性不大。吸入中毒时的表现为神志模糊、眼球震颤,尿中有蛋白、草酸钙结晶和红细胞等。
【侵入途径】 主要为误被摄入和蒸气吸入; 皮肤可少量吸收。
【有害影响和中毒症状】 本品有毒,误被摄入或吸入蒸气均会中毒。表现为对中枢神经系统有抑制作用,对肾脏有损害,对粘膜有刺激作用,对 心、肝、肺也有损害。乙二醇的蒸气压低,在室温下不大可能达到中毒的浓度。但在加热乙二醇液体时,有大量蒸气挥发于空气中,因而能 引起中毒。职业性急性中毒少见。但在生产和使用过程中,反复接触本品蒸气或少量长期误服,可引起慢性中毒,其症状和征候有: 食欲缺 乏,眼刺激症状,眼球震颤,少尿,嗜睡,淋巴细胞增多,有时见抑郁,反复发作神志模糊及慢性肾脏损害。口服能引起抑郁,进而呼吸和 心力衰竭、肾和脑损害。
【急救】 用水洗眼。用肥皂和水清洗身体污染部位。如误被吞服,立即用1:2000高锰酸钾溶液洗胃,继之盐水导泻。吸入中毒者,应立即移离 现场,并静脉点滴1/6mol乳酸600mL和10%葡萄糖酸钙10mL及大量维生素C。
【防护措施】 乙二醇容器上应标明“有毒”字样,防止误服和吸入蒸气。操作人员应穿戴防护用具。
【医学监护】 每年体检时,应进行肾和肝功能的检查。定期体检时,特别要查尿常规。
【贮存】 用玻璃瓶或金属筒盛装。存放在阴凉、通风良好的地方,密封保存。长期贮存要氮封、防潮、防火、防冻。
【运输要求】 运输时容器上须标有“有毒、易燃品”标记。运输中要防火、防冻和防止雨淋。
【灭火措施】 如发生火灾,用雾状水、干粉灭火剂、抗溶性泡沫或CO2灭火。如用水或泡沫可引起沸溢现象,但可用水使暴露在火中的容器保持 冷却。如有溢漏,且溢漏物未被点燃,可用雾状水将其冲离火场,并稀释为不易燃的混合物。
【废弃物建议处理方法】 焚烧。另一种方法是,从聚酯厂废液中回收乙二醇。
【网络资料参考】
乙二醇又称甘醇,是最简单的脂肪族二元醇,具有醇类的化学性质,如能生成醚、酯,能被氧化生成醛或酸,能缩合生成醚。也可被卤素取代。与酰氯或酸酐反应,一般均形成双 酯。在催化剂(二氧化锰、氧化铝、氧化锌或硫酸)作用下加热,可在分子内或分子间脱水,生成环状乙二醇缩乙醛,它与硝酸反应生成乙二醇二硝酸酯(一种炸药)。 乙二醇是生产 聚酯树脂、醇酸树脂、聚酯纤维的原料,也用作汽车抗冻剂和飞机发动机致冷剂,1980年美国用于抗冻剂的乙二醇与用于生产聚酯的消费量相等。另外,还可合成涤纶纤维等高分 子化合物。乙二醇二硝酸酯与硝化甘油联合使用可使炸药的冻点降低。乙二醇还可作为药品和塑料的原料及高沸点溶剂。工业上以乙烯为原料,使其先转化成环氧乙烷再水解制得 乙二醇。
【参考资料】
王翔朴,王营通,李珏声 主编.卫生学大辞典.青岛:青岛出版社.2000.第856...
许力以,周谊 主编.百科知识数据辞典.青岛:青岛出版社.2008.
安家驹 主编;包文滁,王伯英,李顺平 合编.实用精细化工辞典.
http://www.chemicalbook.com/ProductChemicalPropertiesCB7852707.htm
http://baike.baidu.com/view/83513.htm
http://zh.wikipedia.org/wiki/%E4%B9%99%E4%BA%8C%E9%86%87
