
1YR企业会员
发布人:武汉恩玑生命科技有限公司
发布日期:2026/2/12 15:34:28
研究背景
随着肿瘤免疫治疗的快速发展,精准评估肿瘤免疫微环境(TME)成为解读免疫逃逸机制、筛选免疫治疗获益人群、优化治疗方案的核心前提。传统单标免疫组织化学(IHC)和免疫荧光(IF)技术仅能检测单一标志物,无法全面呈现TME中复杂的免疫细胞亚群组成、标志物共表达特征及细胞间空间关系,难以满足精准免疫治疗研究与临床应用的需求。在此背景下,多重免疫组织化学(mIHC)和多重免疫荧光(mIF)技术应运而生并快速迭代,凭借可同时检测组织切片中多种标志物的优势,成为解析TME异质性、挖掘免疫治疗生物标志物的核心技术。
近年来,mIHC和mIF技术在基础研究与临床转化中得到广泛应用,涵盖肺癌、黑色素瘤、乳腺癌等多种恶性肿瘤,相关研究成果持续涌现,推动了免疫治疗领域的突破。但与此同时,该技术的标准化进程滞后于应用发展速度,尤其是图像分析和数据管理环节,缺乏统一的行业规范和最佳实践指导,成为制约技术规模化应用、跨机构合作及临床落地的关键瓶颈。
为破解这一难题,癌症免疫治疗学会(SITC)此前已发布文章《The Society for Immunotherapy in Cancer statement on best practices for multiplex immunohistochemistry (IHC) and immunofluorescence (IF) staining and validation》,其中详细介绍了mIHC/IF染色和验证相关的最佳实践指南,规范了技术前端的实验流程,但针对图像采集、处理、分析、算法验证及数据共享等后端核心环节,尚未形成统一标准,导致不同实验室、不同技术平台的研究结果可比性差、数据可重复性低,难以转化为临床可用的诊断依据和治疗参考。基于此,SITC牵头组织全球多领域专家,结合现有研究成果和实践经验,制定并发布了文章《Society for Immunotherapy of Cancer: updates and best practices for multiplex immunohistochemistry (IHC) and immunofluorescence (IF) image analysis and data sharing》,聚焦图像分析和数据共享的标准化建设,填补行业空白,推动mIHC/IF技术从科研向临床规范转化,为精准免疫治疗提供技术支撑。
mIHC/IF图像分析的最佳实践及对应结果图分析
1、mIF染色幻灯片扫描
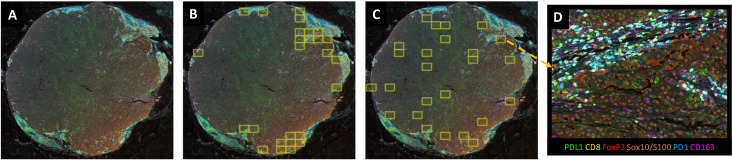
研究以晚期黑色素瘤样本为研究对象,通过mIF染色后的全景扫描图、热点区域采样、异质性捕捉采样及高分辨率高倍视野示例四张子图,直观呈现了mIF图像分析中HPF/ROI的多种标准化采样策略。其中,全景扫描图明确了组织整体结构与免疫细胞分布格局,热点区域采样聚焦肿瘤-基质界面的CD8+T细胞高密度区域,异质性采样覆盖肿瘤不同区域以规避选择偏倚,高分辨率HPF则为下游精准分析提供高质量输入。该图解决了现有研究中ROI选择不统一、采样代表性不足的痛点,为文中图像采集标准化建议提供了可视化支撑,明确了不同采样策略的适配场景,助力提升跨实验室采样流程的一致性,为后续定量分析的可靠性奠定基础。
2、mIHC/IF图像颜色向量分离效果验证
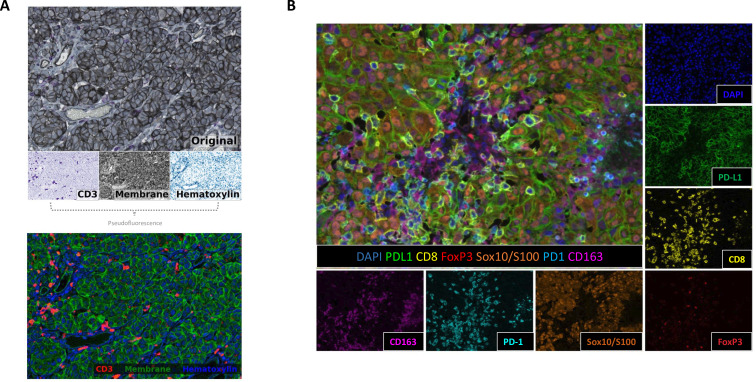
该结果分为mIHC颜色反卷积和mIF光谱解混两部分,清晰展示了两种技术在分离标志物信号中的实操效果。mIHC通过QuPath工具完成颜色反卷积,将混合染色分离为独立颜色向量并转换为伪荧光图,解决了传统mIHC染色信号重叠的问题。mIF通过inForm工具结合荧光团发射光谱解混,分离6标记面板加DAPI的单独信号,有效规避荧光串扰干扰。该图不仅验证了颜色反卷积和光谱解混技术的有效性,更明确了两种技术的标准化操作工具与流程,为不同实验室选择适配的信号分离方法提供参考,减少因信号分离不规范导致的分析误差,提升结果的可比性。
3、组织分割、细胞分割与像素级分析
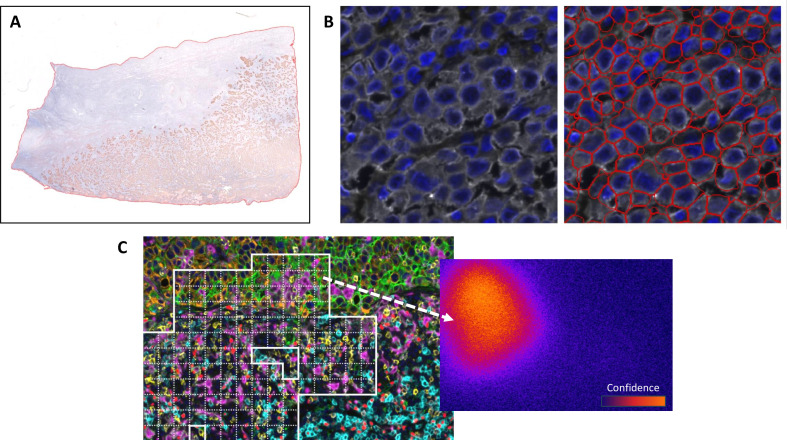
该图聚焦mIHC/IF图像分析的核心处理环节,通过三张子图对比了三种关键分析方式的实操效果与适配场景。组织分割通过QuPath工具精准圈定分析区域,排除无关背景干扰。细胞分割借助Mesmer算法实现单细胞分辨率标注,解决了黑色素瘤样本中不规则细胞分割误差的难题。像素级分析通过NaroNet算法生成置信度热图,适配形态异常细胞或伪影区域的分析需求。该实验为分割方法选择提供了实践依据,明确了不同分割方式的优劣与适用场景,帮助研究者根据样本类型和研究目的选择合适的分析策略,同时强调了分割准确性对后续表型分析、定量结果可靠性的重要影响。
4、表型分析算法的迭代开发及性能验证
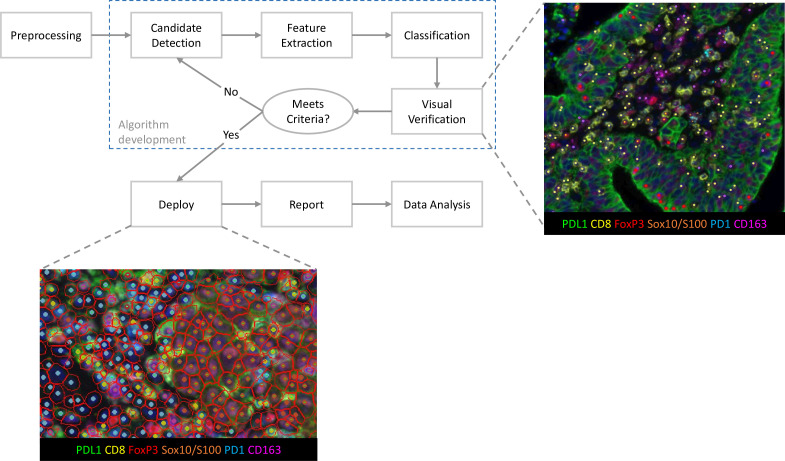
以流程图结合实操示例的形式,完整呈现了mIHC/IF表型分析算法的标准化开发与验证流程,涵盖预处理、候选检测、特征提取、分类、视觉验证、迭代优化及最终部署等关键步骤。通过非小细胞肺癌、晚期黑色素瘤样本的实操示例,展示了算法从开发、验证到优化的全流程,明确了病理学家视觉验证在算法优化中的核心作用,以及算法输出结果的标准化呈现方式。解决了现有研究中算法开发不规范、验证流程缺失导致的结果不可重复问题,为实验室开发和优化表型分析算法提供了标准化流程参考,保障表型分类结果的准确性与一致性。
5、注释工具在TME区域筛选中的标准化应用展示
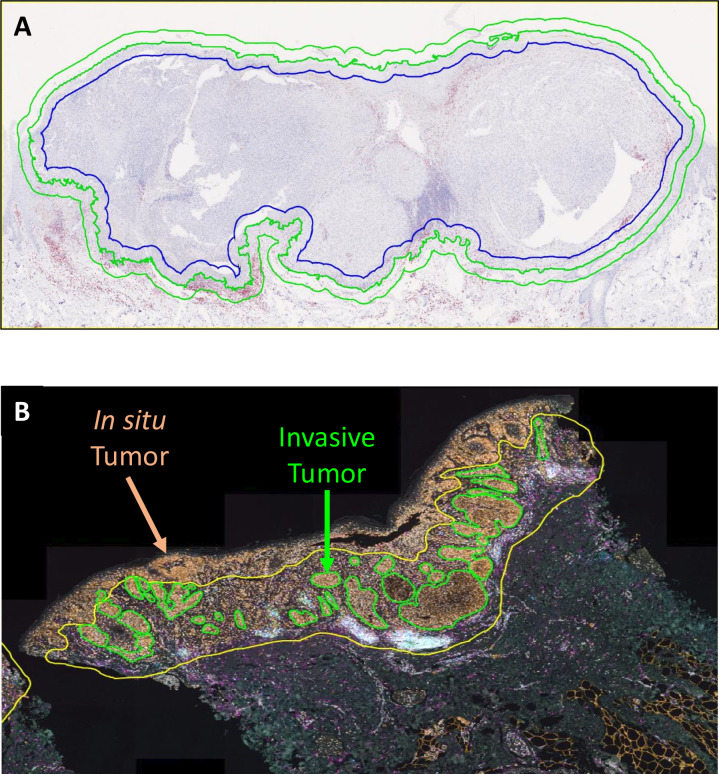
以黑色素瘤、皮肤活检样本为示例,图中展示了注释工具在mIHC/IF图像分析中区域筛选的标准化操作。本示例中注释通过 HALO 软件生成,图像分析工具能够按预设增量扩展该注释范围,为肿瘤周围区域的特征分析提供标准化且可重复的研究方法。注释工具还可用于排除无需分析的区域。在B图皮肤活检样本的代表性显微照片中,样本经多重免疫荧光(mIF)染色后,利用 HALO 软件对侵袭性黑色素瘤结节进行标注(绿色线条),黄色线条划定了纳入最终分析的肿瘤微环境区域, 根据预先设定的研究设计,刻意排除了表皮上层的原位黑色素瘤组织。该图明确了注释工具的标准化使用方法,强调了注释策略预定义和操作一致性的重要性,解决了现有研究中区域筛选主观化、标准不统一的痛点,有效避免因区域筛选偏差导致的分析结果失真,提升研究结果的可靠性与可重复性。
6、连续切片图像配准及合并分析的可行性验证
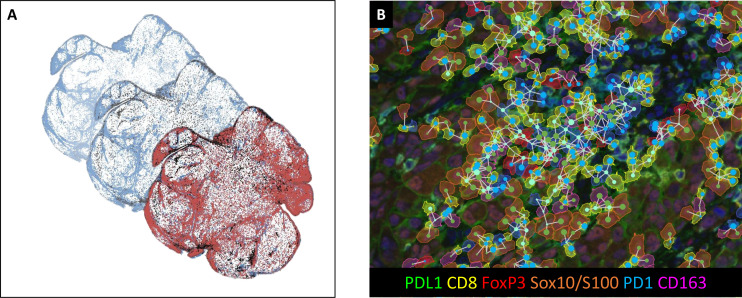
该图以连续切片为研究对象,展示了通过IHC检测、图像扫描、HALO配准、MATLAB合并分析的全流程,验证了连续切片技术在扩展mIHC/IF检测复杂度中的可行性。同时通过细胞表型着色、PD-1/PD-L1表达水平标注及邻近性分析,实现了多标志物、多切片的综合分析,为全面解析TME异质性提供了新路径。
总结
文献系统阐述了mIHC/IF图像分析全流程的标准化方法,涵盖五大关键环节:图像采集强调采用全切片成像技术规避标志物表达异质性带来的偏差,同时规范ROI/HPF采样策略,建议至少采集5个高倍视野以保证代表性。颜色反卷积与光谱解混可有效分离标志物信号,推荐借助QuPath、inForm等工具完成,减少染色重叠或荧光串扰。组织与细胞分割对比了单细胞分辨率分割与像素级分析的优劣,针对巨噬细胞等不规则细胞建议采用分类型独立分割。表型分析介绍了阈值法与机器学习分类器的应用,强调结合两种方法提升准确性。算法验证则突出病理学家视觉验证的核心作用,需通过迭代优化减少漏检、误检。
上述工作将进一步推动mIHC/IF技术在肿瘤免疫研究中的应用,促进跨机构合作和数据共享,为精准免疫治疗的发展提供重要支撑。后续需通过大规模多中心研究、技术创新和行业协同,不断完善mIHC/IF图像分析的标准化体系,优化图像分析方法,充分发挥其在癌症免疫治疗领域的价值。
参考文献
Taube JM, Sunshine JC, Angelo M, Akturk G, Eminizer M, Engle LL, Ferreira CS, Gnjatic S, Green B, Greenbaum S, Greenwald NF, Hedvat CV, Hollmann TJ, Jiménez-Sánchez D, Korski K, Lako A, Parra ER, Rebelatto MC, Rimm DL, Rodig SJ, Rodriguez-Canales J, Roskes JS, Schalper KA, Schenck E, Steele KE, Surace MJ, Szalay AS, Tetzlaff MT, Wistuba II, Yearley JH, Bifulco CB. Society for Immunotherapy of Cancer: updates and best practices for multiplex immunohistochemistry (IHC) and immunofluorescence (IF) image analysis and data sharing. J Immunother Cancer. 2025 Jan 8;13(1):e008875. doi: 10.1136/jitc-2024-008875. PMID: 39779210; PMCID: PMC11749220.
EnkiLife mIF 技术服务
提供有偿代检和分析服务
承接多色配套服务

相关新闻资讯