
7YR企业会员
发布人:广州优南科技有限公司
发布日期:2025/8/26 9:46:12
时间:2025-08-26 作者:药智数据【转载】
导读:获得美国食品药品监督管理局(FDA)突破性疗法认定
8月18日,百利天恒全资子公司西雅图免疫与百时美施贵宝公司宣布,Izalontamab Brengitecan(以下简称“iza-bren”)已获得美国食品药品监督管理局(FDA)突破性疗法认定,用于治疗携带EGFR 19号外显子缺失或21号外显子L858R置换突变、且在EGFR-TKI及铂类化疗后进展的局部晚期或转移性非小细胞肺癌患者。
非小细胞肺癌(NSCLC)约占所有肺癌患者的80%,仍是全球癌症相关死亡的主要原因。其药品市场规模显著增长,药智数据【药品全终端销售分析系统】显示,2024 年国内三大终端(公立医院/零售药房/电商B2C)总销售额超723亿元。Iza-bren作为全球首个进入III期临床研究的双抗ADC药物,将有望在未来市场中占据重要地位。
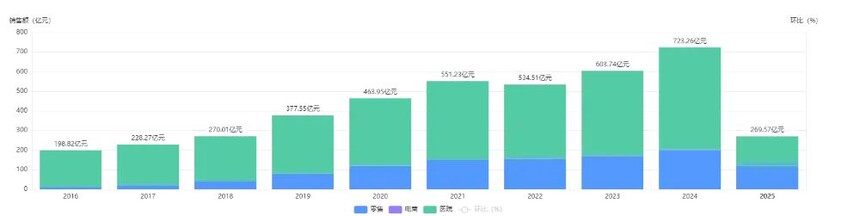
图片来源:药智数据企业版-药品全终端销售分析系统
Iza-bren是一款潜在全球首创的双特异性抗体偶联药物(ADC),其载荷为拓扑异构酶1抑制剂,可同时靶向表皮生长因子受体和人表皮生长因子受体3(EGFRxHER3)。该药物在中国由百利天恒独家开发,在中国以外的地区,根据合作协议和独家授权条款,由西雅图免疫与百时美施贵宝共同开发。此次突破性疗法认定基于BL-B01D1-101(中国)、BL-B01D1-203(中国)和BL-B01D1-LUNG-101(美国/欧洲)三项临床试验数据。在这些临床试验中,iza-bren在既往接受过第三代EGFR-TKI和含铂化疗后进展的EGFR突变非小细胞肺癌患者中显示出疗效提升和安全性可控的特征。
药智数据显示,2023年12月,百利天恒与百时美施贵宝(BMS)达成总额84亿美元的全球战略合作,创下中国创新药出海授权纪录。据悉,百利天恒将继续推进iza-bren的全球多中心临床试验,力争在2026年前提交NSCLC适应症的上市申请。

图片来源:药智数据企业版-全球药物分析系统
未来,期待更多像iza-bren这样的“中国方案”破局而出,以科学突破打破壁垒,以创新合作凝聚共识,让全球患者共享中国医药创新的红利。
转载链接:https://news.yaozh.com/archive/45940.html
如有侵权请联系我们,我们将会删除。
优南推荐产品
Compound T5398(SC)
1781932-33-9
TX1-85-1
1603845-32-4
相关新闻资讯