
7YR企业会员
发布人:广州优南科技有限公司
发布日期:2025/8/14 9:26:31
时间:2025-08-14 作者:药研网【转载】
2025年7月2日,美国FDA宣布,加速批准再生元制药(Regeneron)研发的linvoseltamab-gcpt(商品名:Lynozyfic)上市,用于治疗既往接受至少四线治疗的复发或难治性多发性骨髓瘤(RRMM)成人患者,此前治疗方案需包括蛋白酶体抑制剂(PI)、免疫调节剂(IMiD)以及抗CD38单抗。

该疗法由再生元(Regeneron)开发,Linvoseltamab是一种双特异性抗体,通过将MM细胞表面的B细胞成熟抗原(BCMA)与T细胞表面的CD3连接,促进T细胞激活并杀伤肿瘤细胞。获得批准后,Regeneron股价上涨了2%。
此次加速批准基于LINKER-MM1研究(NCT03761108)的数据支持。这是一项开放标签、多中心、多队列的临床试验,纳入既往接受过至少3种治疗方案的RRMM患者,但排除曾接受BCMA靶向双抗、BCMA CAR-T或其他T细胞连接器疗法的患者。
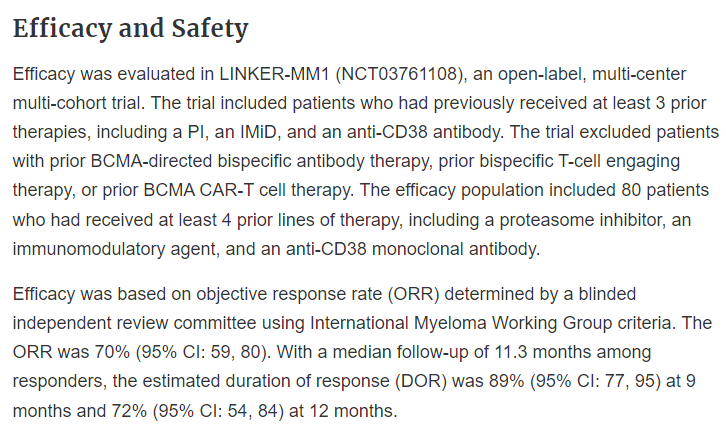
在已接受至少4线治疗的80例患者中,客观缓解率(ORR)达70%(95% CI: 59%-80%),经盲法独立审查委员会依据IMWG标准评估。中位随访11.3个月后,缓解持续率(DOR)在9个月时为89%,12个月时为72%,显示出持久的抗瘤活性。
说明书包含黑框警告,提示可能发生危及生命的细胞因子释放综合征(CRS)和神经毒性,包括ICANS:
CRS发生率为46%,其中≥3级不足1%;
神经毒性(含ICANS)发生率为54%,其中8%为3-4级。
此外,还需警惕感染、中性粒细胞减少、肝毒性及胚胎-胎儿毒性风险。
由于潜在的严重不良事件,Lynozyfic仅可在REMS(风险评估与管理策略)限制性计划中使用,确保治疗安全性。

结语
BCMA靶向疗法是近年来多发性骨髓瘤治疗中最炙手可热的方向。随着Lynozyfic的获批,双抗BiTE疗法正成为CAR-T之外的又一重要治疗支柱,为多线治疗失败后的患者带来了新的希望。
原文标题 : 美国FDA批准再生元BCMA/CD3双抗治疗多发性骨髓瘤
转载链接:https://www.ofweek.com/medical/2025-07/ART-11163-8500-30666131.html
如有侵权请联系我们,我们将会删除。
优南推荐产品
CD3254
196961-43-0
CD38 inhibitor 1
1700637-55-3
相关新闻资讯