
4YR企业会员
发布人:上海优宁维生物科技股份有限公司
发布日期:2025/1/3 16:42:58
一、抗体偶联药物ADC介绍
抗体偶联药物(Antibody-Drug Conjugate,ADC),是一种通过连接子将抗体与具有生物活性的小分子细胞毒性载荷连接起来的新型高效生物药物(图1)。ADC药物的三大元件包括:①特异性靶向抗体;②毒素;③可裂解/不可裂解的连接子。特异性靶点识别及有效的毒素作用使ADC成为名副其实的“生物导弹”。 ADC药物的开发具有较高的技术壁垒,需要综合考虑靶点的合理选择;抗体、连接子、小分子药物及它们之间的合理组合;抗体偶联技术以及ADC药物的耐药性等多个因素。 其中,靶点的选择、连接子的选择、偶联技术以及临床前的药效评价是ADC研发过程中关注的焦点。
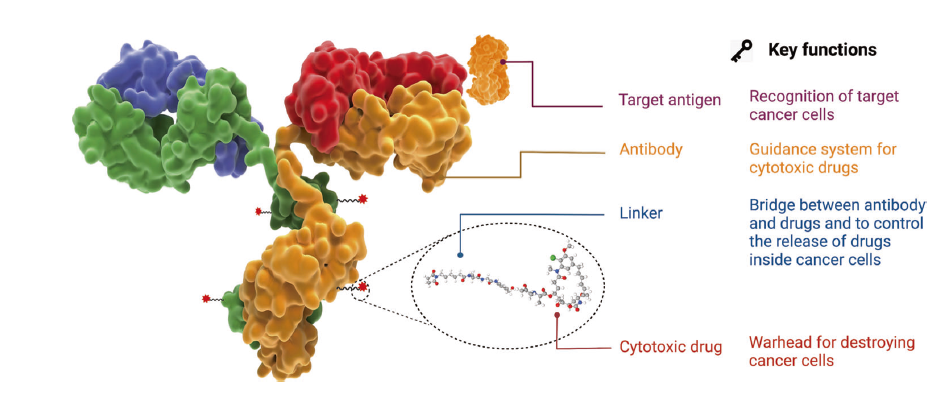 图1 ADC药物的结构和特性[1]
图1 ADC药物的结构和特性[1]
二、ADC的制备
ADC的制备始于靶抗原的选择,ADC的安全性和有效性在很大程度上依赖于靶抗原的选择以及和它的相互作用。然后针对靶抗原先行研制高度特异性的抗体,而后利用特定的可裂解或不可裂解的连接子片段,通过赖氨酸偶联、半胱氨酸偶联、定点偶联等方式将细胞毒性载荷与抗体连接起来。
ADC制备常用途径有两种,一步法和两步法。一步法是先将连接子和细胞毒性载荷连接起来再进行抗体偶联,二步法是先将连接子与抗体偶联再进行细胞毒性载荷的连接。ADC开发中的最大挑战之一是为抗体和细胞毒载荷选择适当的连接子及偶联模式,因为除了有效输送细胞毒载荷外,抗体-载荷连接系统的稳定性是决定ADC疗效和毒性的关键性因素,既要保证到达肿瘤细胞前在血液循环中不会提前断裂导致脱靶,毒性又要到达肿瘤细胞后高效释放细胞毒性载荷,是决定ADC治疗潜力的关键性因素。细胞毒性载荷是ADC最重要的核心构件,是最终执行杀伤肿瘤细胞(直接杀伤或旁观者效应) 的活性成分,高毒力的载荷是使ADC发挥预期功效的关键。
三、ADC的关键要素[2]
ADC由抗体、连接子和细胞毒性小分子药物组成,通过抗体与肿瘤细胞表面的特异性抗原结合,实现高活性的细胞毒药物对肿瘤细胞的精准杀伤。此外,靶抗原的选择和偶联方式对于所设计的ADC是否具有安全、有效的临床治疗效果也是极为重要的。
3.1 ADC设计的起点:抗原靶点
抗原靶点的选择需要考虑以下几方面:①靶抗原在肿瘤中高表达,在正常细胞中不表达或低表达;②目标抗原是否在肿瘤细胞的细胞膜表面分布,因而才可以被特异性抗体所识别;③抗原是否不易脱落,以防止抗体与循环内的抗原结合;④目标抗原是否具有内化特性,这将有助于把ADC 所偶联的毒素分子携带入肿瘤细胞内发挥作用,且靶抗原在ADC治疗后不应下调。
目前已有超过50种抗原被作为ADC所识别的靶抗原。实体肿瘤细胞过表达抗原如HER2、EGFR、CD56、Trop2、CD70、Tissue factor、Collagen IV等。目前ADC应用较多的靶抗原包括Her2、CD19、CD33、CD22、MSLN(mesothelin)等。
3.2 ADC中的抗体
抗体是ADC设计中的另一个重要组成部分,其应能够特异性的识别肿瘤细胞的靶抗原并与靶抗原存在较高的亲和力,如缺乏高度特异性或与其他抗原发生交叉反应,都会发生不可预测的副作用。同时,抗体还应具有免疫原性弱、半衰期长、血液循环稳定性好的特点。抗体根据其重链恒定区序列可分为IgG、IgA、IgD、IgE和IgM 共五类,目前已批准的ADC均采用IgG类抗体,其中IgG1由于其分子量适中、亲和力高、半衰期长、制备简便且能发挥较强的Fc效应子功能等特点,在ADC抗体研发中应用最多。
ADC普遍采用人鼠嵌合抗体(鼠源的轻重链可变区与人源的恒定区,如Adcetris) 与人源化抗体(鼠源的CDR片段,其它序列均为人源,如Mylotarg 和Kadcyla),这在一定程度上降低了免疫原性,减少了人抗鼠抗体的产生。但早期ADC仍存在一定程度的脱靶毒性、产品不均一、易聚集或快速被清除等问题,治疗窗口窄。
抗体的特异性、亲和力以及内化率也是需要考虑的因素。高特异性有助于将毒素小分子集中递送至肿瘤部位,从而达到靶向的药理作用。特异性低的ADC 更有可能对正常组织产生毒性。ADC 抗体应该具有较高的结合亲和力,大多数ADC的结合亲和力在0.1~1.0 nM之间。与小分子相比,抗体从血浆进入组织的速度更慢,而较快的内化效率可以提高ADC的药效。
ADC的抗体部分可以采用双特异性抗体或单域抗体等形式。双特异性抗体可针对同一靶抗原的两个不同表位,也可针对两个不同的靶抗原。也有采用单域抗体偶联杀伤性放射性元素或毒性分子,用以开发新型ADC。
3.3 ADC中的连接子(Linker)
Linker将抗体与有效载荷连接起来。连接子在血液中的稳定性非常重要,需要在血液中保持稳定以保持细胞毒性载荷附着在抗体上,但是一旦ADC进入肿瘤细胞或被运输到溶酶体,连接子应迅速分解以释放有效
载荷。连接子会影响ADC 的许多重要特性,例如药物-抗体比值(DAR)、有效载荷释放时间、治疗指数(Therapeutic Index,TI) 和药代动力学。
根据肿瘤细胞内连接子的切割特性,可将连接子分为可切割和不可切割两种类型。可切割的连接子可以通过多种机制进行裂解,包括腙键的酸不稳定裂解、二硫键的还原裂解和多肽键的酶解。例如,酸不稳定连接在血液中通常是稳定的,但在低pH的溶酶体环境中(如Besponsa和Mylotarg)会速裂解,释放出小分子毒素,发挥细胞杀伤作用。二硫键类型的则可通过细胞内谷胱甘肽(Glutathione,GSH) 还原反应释放细胞毒载荷杀伤肿瘤细胞,并且其空间位阻作用可限制ADC在进入细胞之前的不成熟裂解。如果释放的细胞毒载荷能穿过肿瘤细胞膜,它们就能杀死附近的癌细胞,这就是所谓的“旁观者效应”。但可切割连接子并非一定会产生旁观者效应,主要取决于释放载荷的膜穿透性和电荷特性。需要注意的是,旁观者效应也存在一些缺陷,如杀死目标肿瘤细胞附近的正常细胞或免疫细胞。可切割连接子的另一个缺陷是在体内循环时可能存在一定程度的代谢降解,导致脱靶毒性。
不可切割的连接子由具有在血液中稳定的结构组成,含有该连接子的ADC 只有在进入肿瘤细胞的溶酶体被蛋白酶降解后才会释放有效载荷。稳定连接子大大降低了胞外释放引起的脱靶毒性,但释放效率低,需要良好的内化过程。不可切割连接子被内吞入溶酶体后,连接子不会被降解,连接的抗体则会被降解为氨基酸,形成氨基酸-连接子-小分子细胞毒复合物。由于“连接子-氨基酸残基”带有电荷限制了其透膜及扩散,因而通常不会产生旁观者效应。
3.4 ADC中的细胞毒性载荷
ADC所携带的细胞毒性载荷药物是其最重要的效应成分,或称为有效载荷。目前,常用的细胞毒性分子包括微管生成抑制剂、DNA 损伤因子和DNA转录抑制剂等。微管生成抑制剂通过与微管结合阻止微管的聚合,从而阻滞细胞周期,产生细胞毒性,发挥抗肿瘤作用,例如Monomethyl auristatin E(abs810174)、Maytansine(abs817384)及其类似物。DNA损伤因子则通过与DNA的小沟结合并促进DNA 链烷基化、断裂或交联,例如Calicheamicin(abs819016)。DNA转录抑制剂有Amatoxin 和Quinoline Alkaloid(SN-38),例如CL2A-SN-38(abs819783),由 linker CL2A 和 毒性分子 SN-38 连接而成的drug-linker conjugate,可用来制备ADC。
3.5 ADC的偶联方式
偶联方式主要分为非定点偶联和定点偶联。早期使用的是非定点偶联法,主要由赖氨酸或半胱氨酸偶联。定点偶联方式即通过基因工程位点进行特异性偶联,实现更均一的ADC,能在特定位点实现细胞毒素的连接。
爱必信ADC毒素抗体定点偶联试剂盒(abs580253)操作简便,无需抗体工程化等复杂操作,可快速实现单抗的定点偶联。偶联产物均一、稳定。适用于偶联阶段定点偶联,ADC早期偶联研究。
偶联原理:
(1)抗体叠氮化修饰
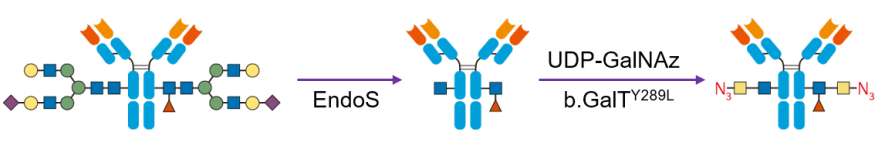
首先使用糖苷酶(EndoS)暴露单抗恒定区的保守N糖链上的乙酰葡糖糖胺(蓝色方块),然后使用牛半乳糖转移酶突变体(b.GalTY298L)将带有叠氮官能团的乙酰半乳糖胺(黄色方块-N3)连在乙酰葡萄糖胺上。
(2)毒素分子连接
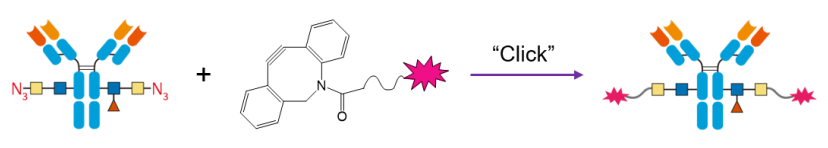
随后可使用无铜催化的炔叠氮化物环加成反应(如SPAAC)将生物素、荧光素或毒素分子等连在单抗上。
爱必信(上海)生物科技有限公司可为科研人员提供ADC细胞毒素、ADC Linker、ADC Linker with Payload、ADC定点偶联试剂盒、ADC热门靶点蛋白、ADC阳性参考抗体、ADC过表达药靶细胞株等试剂以及抗体定制和mIHC服务,可以实现从抗体制备、筛选、偶联到后期的mIHC病理检测,协助加速ADC药物研发。

参考文献:
[1] Fu Z, Li S, Han S, Shi C, Zhang Y. Antibody drug conjugate: the "biological missile" for targeted cancer therapy. Signal Transduct Target Ther[J]. 2022 Mar 22;7(1):93.
[2] 武刚,付志浩,徐刚领,等.抗体偶联药物研发进展[J].生物医学转化, 2021, 2(4):11.
ADC药物研发相关产品推荐:
上海优宁维生物科技股份有限公司
试剂 | 耗材 | 仪器 | 软件 | 定制 | 实验服务 | 供应链
免费热线:4008-168-068
咨询邮箱:info@univ-bio.com
订购商城:www.univ-bio.com
微信公众平台:优宁维抗体专家,欢迎关注!
小优博士(小程序):5大课堂, 让你的科研不再难!


相关新闻资讯