
2YR企业会员
发布人:武汉佰乐博生物技术有限公司
发布日期:2024/10/31 9:35:55
阿尔茨海默病(AD)是一种常见的神经退行性疾病,其主要特征是认知障碍和记忆力丧失,伴随大脑中β-淀粉样蛋白(Aβ)斑块和tau蛋白缠结的堆积。Donanemab 是由礼来公司(Eli Lilly)开发的一种单克隆抗体药物,旨在减少Aβ斑块积累,延缓病情进展。
Donanemab 的设计使其特异性识别Aβ斑块中的N-端焦谷氨酸修饰表位,与斑块结合后,它会激活免疫系统,吸引小胶质细胞等免疫细胞前往病变区域。这些免疫细胞随即促使斑块分解并清除,从而减少Aβ在大脑中的进一步积聚。通过这一机制,Donanemab 旨在减缓神经元损伤,帮助患者保持认知功能并改善生活质量。
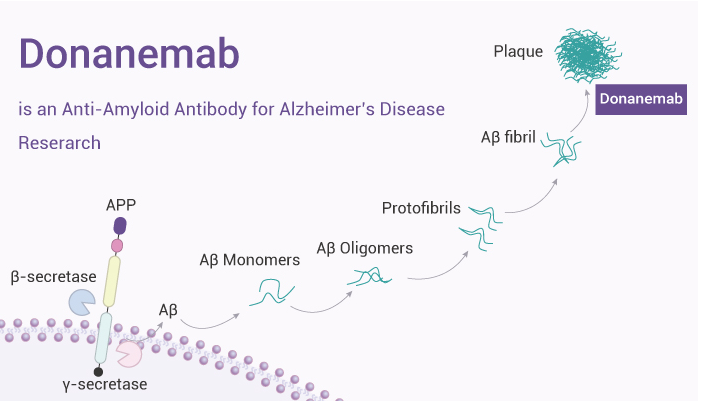
Fig1.Donanemab作用机制
临床试验的发现
在一项名为TRAILBLAZER-ALZ的II期临床试验中,研究人员对257名阿尔茨海默病早期患者进行了Donanemab的测试。患者每四周接受一次静脉注射,疗程为76周。试验结果表明,Donanemab在一定程度上减缓了患者认知与生活能力的退化。
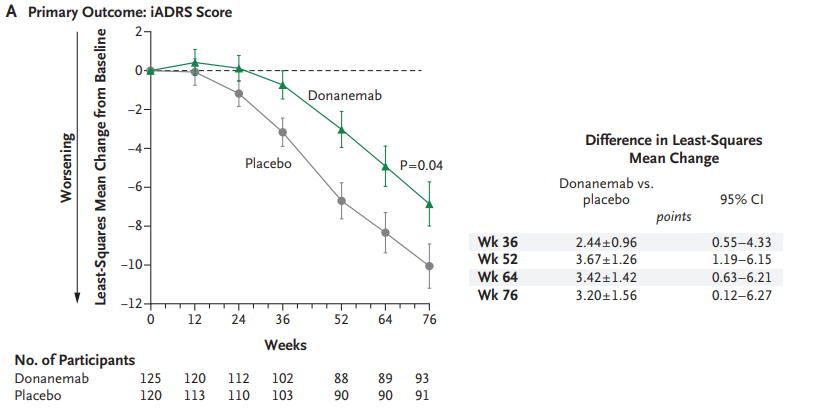
Fig 2.iADRS评分的变化
■主要结果:
在76周内,Donanemab组的综合阿尔茨海默病评分量表(iADRS)平均下降6.86分,而安慰剂组则下降10.06分,显示出3.20分的差距(P=0.04),表明Donanemab减缓了病情恶化的速度。
■次要结果:
尽管某些次要指标(如ADAS-Cog13认知评分)显示出了一些改善,但整体疗效有限,并未在所有指标上达到统计学意义,未能全面支持药物在认知和日常功能上的显著改善。
■生物标志物变化:
Donanemab显著降低了Aβ斑块水平。在76周时,Donanemab组患者的Aβ水平减少了85.06个centiloid单位。然而,尽管Aβ斑块减少,tau蛋白负荷和脑容量变化未表现出显著差异。
副作用与安全性问题
尽管Donanemab在一定程度上减缓了病情进展,但其安全性问题也引发了广泛关注:
■淀粉样蛋白相关影像异常(ARIA-E):
Donanemab组中26.7%的患者出现ARIA-E,而安慰剂组仅为0.8%。部分患者报告了意识混乱和语言表达困难等症状,甚至需要住院治疗。
■不良反应与治疗中断:
Donanemab组中30.5%的患者因不良反应停止治疗,而安慰剂组仅为7.2%。常见的不良反应包括头痛、恶心、头晕和输液相关反应,这些副作用提高了患者使用该药物的风险。
NICE的拒绝与争议
尽管Donanemab在临床试验中展现了潜在的治疗效果,但英国国家卫生与临床优化研究所(NICE)最终拒绝了其上市申请。根据10月24号发表于BMJ(英国医学期刊)上“NICE rejects Alzheimer's drug donanemab owing to cost and "significant health risks"”新闻稿中披露“NICE认为:高昂的药物成本和显著的健康风险使其性价比不符合推广标准。特别是ARIA-E的高发率和多种副作用引发了对其安全性的担忧。”此外,尽管药物在一定程度上延缓了病情进展,但其总体效益有限,不足以证明其高成本的合理性。

Fig 3.NICE rejects Alzheimer’s drug donanemab owing to cost and “significant health risks”
阿尔茨海默病(AD)一直是神经退行性疾病领域中最具挑战的治疗难题之一。多年来投入了大量的资源与科研力量,但药物开发的成功率极低,因此被誉为药物研发的“死亡谷”。许多大型制药公司和研究机构在这个领域付出了巨大的努力,但最终成功上市的药物很少。即便存在诸多困难,但这并未阻止科学界的探索步伐。未来的研究可能需要多靶点联合治疗,不仅关注Aβ和tau蛋白的清除,还需控制神经炎症和修复神经元连接。此外,生物标志物的进步和更敏感的临床量表将有助于提高试验的成功率。而Donanemab的出现正是代表了人类对抗阿尔茨海默病(AD)的一次重要的尝试,也为未来的探索者提供了宝贵的经验与启示。
AntibodySystem作为退行性疾病领域的积极探索者,专注于科研用蛋白/抗体的开发和应用,助力Aβ斑块、tau蛋白、神经炎症等多靶点机制的探索及阿尔茨海默病等退行性疾病的药物筛选。我们致力于提升抗体的特异性和数据可靠性,为基础研究和药物开发提供高质量工具,加速创新疗法的突破。
更多推荐产品一览:

参考文献:
[1]Mintun, Mark A et al. “Donanemab in Early Alzheimer's Disease.” The New England journal of medicine vol. 384,18 (2021): 1691-1704. doi:10.1056/NEJMoa2100708
[2]Mahase, Elisabeth. “NICE rejects Alzheimer's drug donanemab owing to cost and "significant health risks".” BMJ (Clinical research ed.) vol. 387 q2342. 23 Oct. 2024, doi:10.1136/bmj.q2342
相关新闻资讯