庆大霉素的说明书
发布日期:2020/10/24 7:56:57
背景及概述[1][2]
庆大霉素最早是由Weinstein等于1963年发现的,它是小单孢菌产生的多组分的氨基糖苷类抗生素,包括C1,C2,C1a,C2a和C2b等组分。庆大霉素主要组分C1,C2和C1a在临床上被广泛使用,其中抗菌活性最高的是C1a,它是合成依替米星的前体,其次是C2b,又称之为沙加霉素。此类抗生素能够与细菌核糖体30S亚基上的16S rRNA结合,引起遗传密码的误读,从而阻断细菌蛋白质的合成,所以主要用于治疗细菌感染,尤其是革兰阴性菌引起的感染。然而,在实际使用过程中由于有很高的肾毒性,所以它们在临床上的应用受到限制。
有文献表明其肾毒性是由于庆大霉素能够特异性的结合73kDa的分子伴侣HSP73,从而导致伴侣蛋白活性的降低,但是其具体的毒副作用机制还有待探明。目前已经测序并且公布了3 Accession No. AJ575934),另外两株棘孢小单孢(GenBank Accession No. AY524043和AJ628149)。庆大霉素对各种革兰阴性细菌及革兰阳性细菌都有良好抗菌作用,对各种肠杆菌科细菌如大肠埃希菌、克雷伯菌属、变形杆菌属、沙门菌属、志贺菌属、肠杆菌属、沙雷菌属及铜绿假单胞菌等有良好抗菌作用,奈瑟菌属和流感嗜血杆菌 对该品中度敏感。对布鲁菌属、鼠疫杆菌、不动杆菌属、胎儿弯曲菌也有一定作用。
对葡萄球菌属(包括金黄色葡萄球菌和凝固酶阴性葡萄球菌)中甲氧西林敏感菌株的约80%有 良好抗菌作用,但甲氧西林耐药株则对该品多数耐药。对链球菌属和肺炎链球菌的作用较差,肠球菌属则对该品大多耐药,硫酸庆大霉素与β内酰胺类合用时,多数可获得协同抗菌作用。硫酸庆大霉素的作用机制是与细菌核糖体30S亚单位结合,抑制细菌蛋白质的 合成,近年来革兰阴性杆菌对庆大霉素耐药株显著增多。但使用现有庆大霉素生产配方进行发酵生产其产品杂质很高,很难符合《中国药典》2010版的要求。
规格[3]
注射剂:20mg(2万IU)/1ml,40mg(4万IU)/1ml,80mg(8万IU)/2ml。
片剂:20mg、40mg。
滴眼剂:40mg/8ml。
用法用量[4]
1. 肌注或静滴,1次80mg,1日2~3次(间隔8小时)。对于革 兰阴性杆菌所致重症感染或铜绿假单胞菌全身感染,1日量可用到5mg/kg。静脉滴注给药可将1次量(80mg),用输液100ml稀释,于30分钟左右滴入。小儿1日量3~5mg/kg,分2~3次给予。
2. 口服,一次80~160mg,一日3~ 4次。小儿每日10~15mg/kg,分3~4次服,用于肠道感染或术前准备。庆 大霉素珠链:系由塑料制成的小珠,串连成链状,含有庆大霉素,放置脓腔 中,缓缓地释放药物起局部抗菌作用(1mg=庆大霉素1000U)。滴眼液:8ml (40mg)。
应用[4]
主要用于大肠埃希菌、痢疾志贺菌、克雷伯肺炎杆菌、变形杆菌、铜绿假 单胞菌等革兰阴性菌引起的系统或局部感染(对中枢感染无效)。
药理作用 [4]
对大肠埃希菌、产气杆菌、克雷伯杆菌、奇异变形杆菌、某些吲哚阳性变形杆菌、铜绿假单胞菌、某些奈瑟菌、某些无色素沙雷和志贺菌等革兰阴性菌有抗菌作用。革兰阳性菌中,金黄色葡萄球菌(包括产β-内酰胺酶株)对本品敏感;链球菌(包括化脓性链球菌、肺炎链球菌、粪链 球菌等)均对本品耐药。厌氧菌(拟杆菌属)、结核分枝杆菌、立克次体、真菌和病毒也对本品耐药。近年来,由于本品的广泛应用,耐药菌株逐渐增多,铜绿假单胞菌、克雷伯杆菌、沙雷杆菌和吲哆阳性变形杆菌对本品的耐药率甚高。
不良反应[4]
1.本品血药峰浓度超过12μg/ml,谷浓度超过2μg/ml以上 时可出现毒性反应,对于肾功能不全者或长期用药者应进行药物监测。
2. 本品1日量宜分2~3次给药,以维持有效血药浓度,并减轻毒性反应。不要把1日量集中在1次给予。
3. 毒性反应与卡那霉素近似,因剂量小,故毒性反应稍轻。但若用量过大或疗程延长,仍可发生耳、肾损害,应予注意。
4.对链球菌感染无效。由链球菌引起的上呼吸道感染不应使用。
5.有抑制呼吸作用,不可静脉推注。
注意事项[3]
1. 本药损害第八对颅脑神经,与链霉素一样以损害前庭功能为主,对耳蜗的损害较小,一般较难恢复。如发现早,及早停药,则属可逆。
2. 肾功能损伤病人更易发生,严重烧伤病人局部即使外用,也可能出现上述损伤。偶见贫血、紫癜、惊厥、血清转氨酶和胆红素升高。肾功能减退病人或长期用药者应进行药物监测。
3. 与新霉素、卡那霉素有交叉过敏。有抑制呼吸作用,不可静脉推注。
4. 小儿慎用。
5. 禁用于有过敏史或其他氨基糖甙类抗生素过敏的病人。
药物相互作用[3]
与利尿剂合用可增加耳、肾毒性。与两性霉素、头孢菌素类、红霉素、肝素、青霉素类、碳酸氢钠、磺胺嘧啶等在体外有配伍禁忌。
制备[2]
庆大霉素属于4,6-二取代的氨基糖苷类抗生素,其核心结构是2-脱氧链霉胺。生物合成途径最早是由Testa和Tilley在研究一株产巴龙霉胺的绛红色小单孢突变株时提出来的,发现庆大霉素C1不能转化为其它物质,然而C2能够转化为C1,同时C1a能够转化为C2b。庆大霉素的生物合成途径大致可以分为两个主要的阶段:①庆大霉素前体A2的合成;②庆大霉素C族化合物的合成。
1)庆大霉素前体A2的生物合成庆大霉素的生物合成起始于D-葡萄糖。首先是D-葡萄糖的C-6位发生磷酸化作用形成D-葡萄糖-6-磷酸,紧接着2-脱氧青蟹肌糖(DOI )合酶催化其形成2-脱氧青蟹肌糖,然后在2-脱氧青蟹肌糖氨基转移酶的作用下C1位发生转胺作用形成2-脱氧青蟹肌糖胺,随后在脱氢酶的作用下C3位脱氢形成2-脱氧-3酮青蟹肌糖胺,接下来由2-脱氧青蟹肌糖氨基转移酶催化在C3位转入氨基形成庆大霉素核心单元:2-脱氧链霉胺。
与此同时,D-葡萄糖的C1位发生磷酸化作用形成D-葡萄糖-1-磷酸,然后在UDP-转移酶的作用下形成UDP-葡萄糖,随后在氨基转移酶的作用下在C2位转入氨基形成UDP-葡萄糖胺,紧接着由糖基转移酶催化与2-脱氧链霉胺反应形成巴龙霉胺。此时UDP-木糖在糖基转移酶作用下连接到巴龙霉胺上形成庆大霉素前体A。
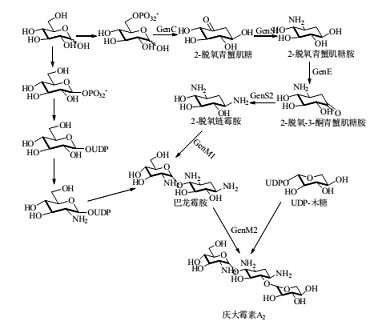
2)庆大霉素C族化合物的生物合成
庆大霉素A2是庆大霉素生物合成中的个假三糖中间体,A2在N-甲基转移酶的作用下形成X2,并且从X2处开始出现分支。其中一条路径在脱氢酶和氨基转移酶的作用下形成JI-20A,随后在脱水酶的催化下,C-3'和C-4'位发生还原脱氧反应形成C1a,最后由甲基转移酶催化C-6'氨基甲基化形成C2b。
另外一条路径在C-甲基转移酶的作用下形成G418,随后同样在脱氢酶和氨基转移酶的作用下形成JI-20B,接着在脱水酶的作用下,C-3'位和C-4'位发生还原脱氧反应形成了庆大霉素C2,其中一部分C2的C-6'位发生N-甲基化形成庆大霉素C1,另一部分C2通过差向异构化形成C。
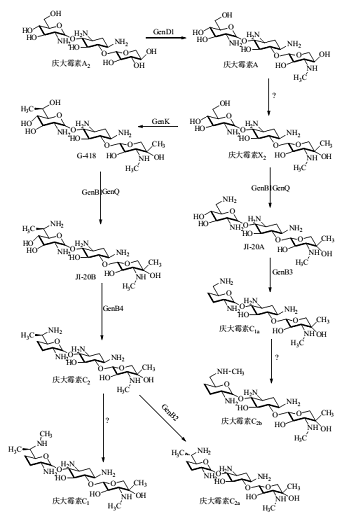
主要参考资料
[1] 王玉红;葛祥斌。CN201310099477.5 .硫酸庆大霉素的制备方法
[2] 蒋明星, 鲁涛, & 文孟良. (2016). 庆大霉素的生物合成. 中国抗生素杂志, 41(1), 16-25.
[3] 常用临床药物手册
[4] 临床常用药物