左旋环氧氯丙烷的制备与应用
发布日期:2023/4/24 17:35:06
手性环氧氯丙烷是重要的C合成子,其中(S)-环氧氯丙烷(S)-ECH是降血脂药物阿托伐他汀、降血压药物卡维地洛等医药的前体,(R)-环氧氯丙烷(R)-ECH是治疗心绞痛药物美托洛尔和减肥药物肉毒碱合成的关键中间体。(R)-环氧氯丙烷别名左旋环氧氯丙烷,英文名(R)-Epichlorohydrin。
左旋环氧氯丙烷的制备[1-3]
手性环氧氯丙烷的制备,目前主要利用化学拆分法和生物催化法来合成手性环氧氯丙烷。
化学拆分法制备手性环氧氯丙烷
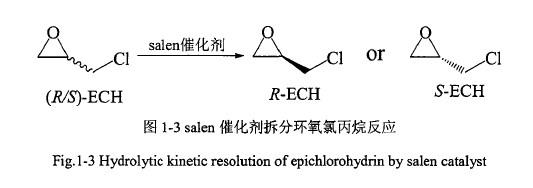
化学拆分法是以Salen催化剂来催化拆分外消旋环氧氯丙烷,得到手性环氧氯丙烷(如图1-3),它是目前最常用的一种制备手性环氧氯丙烷的方法。Salen催化剂的构成包括Salen配体和与之络合的金属两部分。Pfeiffer 等人在1933年首次用1,2-二胺和水杨醛合成配体。1990年,Jacobsen等人用1,2-环己二胺取代了1,2-二胺,合成了目前运用最为广泛的salen配体(见图1-4)。
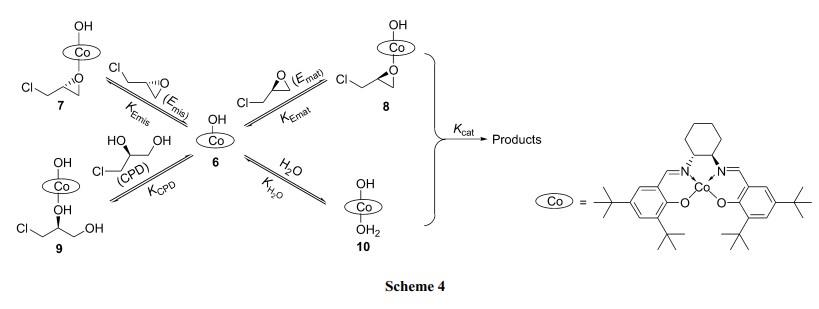
按单元结构可将salen催化剂分成单核催化剂、双核催化剂、聚合salen催化剂以及负载型salen催化剂。虽然化学拆分法制备手性环氧氯丙烷,具有拆分效率高,生产工艺简单等优点,但由于salen催化剂多使用Co等重金属元素作为其络合的金属,对环境存在一定的污染,并且重复性也不理想。
生物催化法制备手性环氧氯丙烷
生物催化法制备手性环氧氯丙烷相对于化学拆分法来说,环境污染小,绿色环保,并且作为催化剂的酶来源广泛,价格低廉,反应条件温和,立体选择性专一,因此越来越受到了人们的青睐与关注。生物催化法主要包括:生物不对称合成法和生物拆分法。
生物不对称合成法:
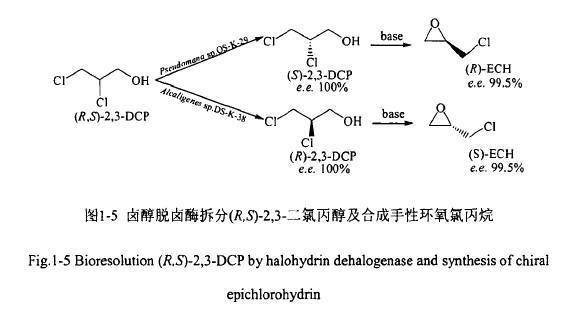
生物不对称合成法是利用卤醇脱卤酶来催化二氯丙醇,来制备手性环氧氯丙烷。1982年,Iruchijima 等人利用胰脂酶将(S)-1-乙酸2,3-二氯丙烷不对称水解生成左旋环氧氯丙烷,但产率只有15.4%,ee为90%。1992年,Kasai等人从活性污泥中筛选到一株假单胞菌(Pseudomonas sp. OS-K-29)和产碱杆菌(Alcaligenes sp. DS-K-S38),它们能拆分外消旋的2,3-二氯丙醇(2,3~DCP),分别得到100%ee.的(S)-2,3-DCP和(R)-2,3-DCP,然后再通过加碱皂化,即可获得左旋环氧氯丙烷和(S)-环氧氯丙烷,ee值可达99.5%(见图1-5)。
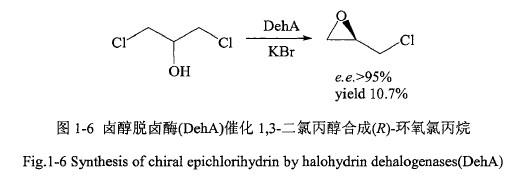
1998年,Assis等人通过卤醇脱卤酶(DehA)催化1,3-二氯丙醇(1,3-DCP)合成(R)-环氧氯丙烷。在反应体系中添加了KBr,反应最终得到(R)-环氧氯丙烷的ee值大于95%,收率10.7%(如图1-6)。
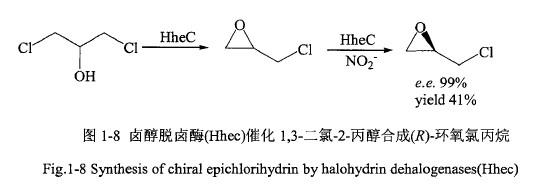
2012年,Jin等人利用来源于放射性土壤农杆菌的卤醇脱卤酶HheC,催化转化1,3-二氣丙醇,合成外消旋环氧氯丙烷(见图1-8)。之后通过NO2的开环作用,将(S)-环氧氯丙烷开环,得到左旋环氧氯丙烷ee值99%,产率41%。
生物拆分法.
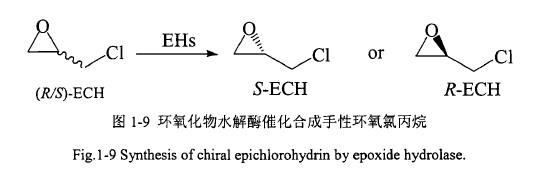
生物拆分法主要是通过环氧化物水解酶(EHs)来拆分外消旋环氧氯丙烷,制备手性环氧氯丙烷(见图1-9)。近年来,随着生物柴油副产物甘油合成环氧氯丙烷技术的日益成熟及规模化应用,环氧氯丙烷市场价格持续走低。因此,以外消旋环氧氯丙烷为原料,通过环氧化物水解酶对其进行拆分来制备单一构型的环氧氯丙烷得到了许多学者的青睐。
1991年,Weijers等人筛选出一株能产环氧化物水解酶诺卡氏菌(Nocardia H8),利用该菌株来拆分外消旋环氧氯丙烷,得到左旋环氧氯丙烷产率为19%;
1997年,Wejers等人报道了胶红酵母(Rhodotorula gtutinis CIMW147)也能拆分外消旋环氧氯丙烷。但胶红酵母产酶量较低,拆分效果并不理想,最终得到左旋环氧氯丙烷产率仪有10%。
2004年,Kim等人利用胶红酵母的重组环氧化物水解酶催化拆分环氧氯丙境。在反应液中加入了5%(V/V)表面活性剂Teen20,得到>99%的左旋环氧氯丙烷,产率为26%。
2005年,丁奎岭等人用从微生物中分离到的环氧化物水解酶ECU1001和ECU1040,在微水相体系中催化拆分环氧氯丙婉,分别得到了(S)ECH和(R)-ECH,最终手性环氧氯丙烷的收率达到40%, ee值为9%。
2007年,Lee等人构建了能表达胶红酵母环氧化物水解酶基因的重组毕赤酵母(Pichia pastoris)。在正十二烷-水(含2.5% (V/V)微水相体系中,能有效催化拆分20 mmol/L外消旋环氧氯丙烷得到(R)-环氧氯丙烷的e.e.值为99%,收率为28.5%。
2011年,Liu 等人合成了能表达红冬孢酵母(Rhodosporidium toruloides)环氧化物水解酶的基因,并重组到大肠杆菌中。在水相体系中催化拆分环氧氯丙烷,反应40 min后得到e.e.值为99%,产率为18%的(R)-环氧氯丙烷。
2014年,邹树平等人利用重组大肠杆菌(E.coli B21)全细胞产生的环氧化物水解酶,在两相体系中(有机溶剂/缓冲液),催化拆分574 mM外消旋环氧氯丙烷,最终得到e.e.值为99.3%的左旋环氧氯丙烷,产率为37.5%。
左旋环氧氯丙烷合成药物的应用
近几十年来在医药治疗、农药施用和环境污染上相继发生了许多严重的事故,都与光学异构体杂质有关,这引起了世界各国的普遍关注。1992年,美国食品和药物管理局对具有手性分子的药物提出了光学活性药品的管理要求和相关政策。至此,手性药物成为了制药工业的新宠儿,而手性环氧氯丙烷作为重要的手性医药中间体,由于其应用面广正受到了越来越多的关注。
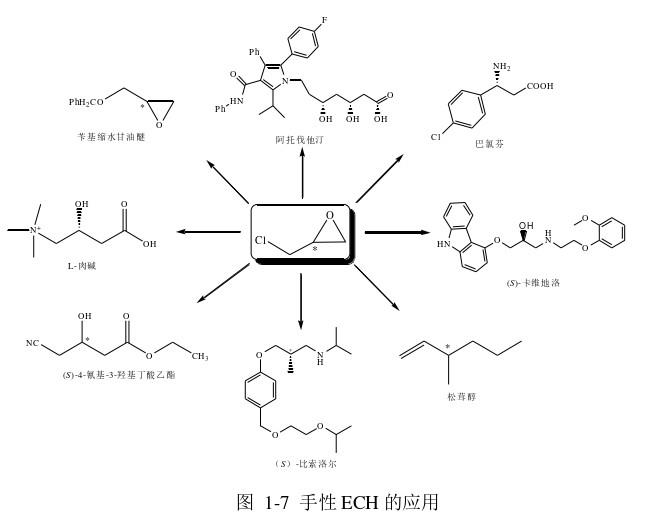
单一手性纯对映异构体(R)-ECH和(S)-ECH (如图1-6所示)均是非常重要的C3手性合成子,广泛用于制备降血脂类药物阿托伐他汀、芳氧丙胺醇类β-肾上腺素阻断剂阿替洛尔、减肥药左旋肉碱以及治疗心绞痛的美托洛尔等多种药物(如图1-7所示)。[4]
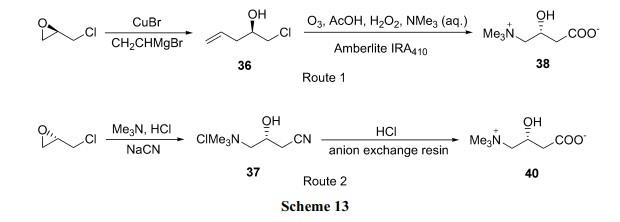
左旋肉碱的合成[3]
手性环氧氯丙烷还常运用于流行减肥药左旋肉碱的合成,1997年,Kabat等通过用左旋环氧氯丙烷与格氏试剂反应经三甲胺取代,阴离子交换后氧化制得L-肉碱。国内沈大冬等则以(S)-环氧氯丙烷为原料经季胺化、氰化、水解后离子交换制得(Scheme13)。
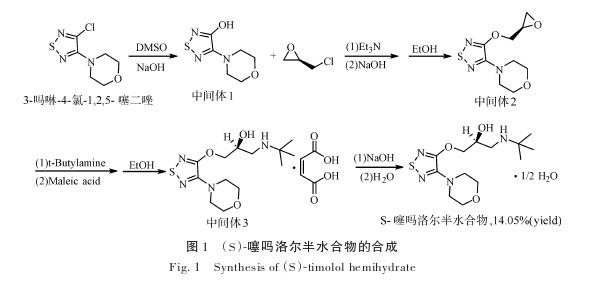
(S)噻吗洛尔半水合物的合成[5]
周政虎等人开发β受体阻断剂新药(S)-噻吗洛尔半水合物的合成策略,采用3-吗啉-4-氣-1,2,5-噻二唑为起始原料,经水解反应得到中间体1(3-吗啉-4-羟基-1,2,5-噻二唑)。中间体1与左旋环氧氯丙烷发生醚化反应,经后处理及重结晶得到中间体2 {(R)-4-[4-(环氧乙 烷-2-基甲氧基)-1,2,5-噻二唑-3-基]吗啉}。中间体2经胺化反应、马来酸成盐及重结晶得到(S)-马来酸噻吗洛尔。(S)-马来酸噻吗洛尔经游离、纯水转晶得到符合药典标准的(S)-噻吗洛尔半水合物,总收率14.05%且ee值为99.66%。
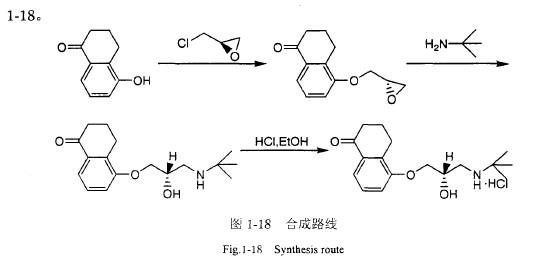
盐酸卡替洛尔的合成[6]
廖新成等报道合成盐酸卡替洛尔(喹酮心安, Carteolol Hydrochloride),其是一新型长效、具有内源拟感活性的非选择性B-肾上腺素受体阻滞剂。廖新成等对(S)-盐酸左布诺洛尔手性合成原路线进行了改进,设计了以α-羟基萘满酮为起始原料,与左旋环氧氯丙烷进行成醚反应,生成手性中间产物5-(2,3-环氧丙氧基)-α-蔡满酮,无需分离纯化即与叔丁基胺反应得(S)-5-[3-(叔丁基氨基)-2-羟基丙基]-3,4-二氢-1(2H)-萘满酮,加盐酸成盐得盐酸左布诺洛尔。该合成路线很好地保持了化合物的立体构型,光学纯度达到90%以上,具体反应路线如下图1-18。
(S)-美托洛尔的合成[6]
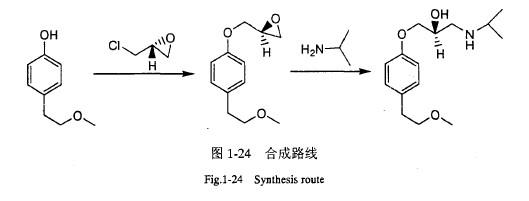
Sang-Hun Jung 等报道,对(S)-美托洛尔手性合成原路线进行了改进,设计了以对甲氧乙基苯酚为起始原料,与左旋环氧氯丙烷进行成醚反应,生成手性中间产物(S)-1-[4-(2-羟乙基)苯氧基]-2,3-环氧丙烷,与异丙胺反应得到(S)-美托洛尔。该合成路线很好地保持了化台物的立体构型、光学纯度达到97%以上,具体反应路线如下图1-24。
参考文献
[1] 颜海蔚. 生物催化合成(R)-环氧氯丙烷[D]. 浙江工业大学, 2013.
[2] 秦超. 基于3-氯-1,2-丙二醇循环利用化学-酶法制备(R)-环氧氯丙烷[D]. 浙江工业大学, 2014.
[3] 卢定强, 涂清波, 凌岫泉等. 手性环氧氯丙烷的制备及其药物应用[J]. 有机化学, 2009, 29(08): 1209-1216.
[4] 王志才. 环氧化物水解酶稳定性改造及在(R)-环氧氯丙烷制备中的应用[D]. 浙江工业大学, 2016.
[5] 周政虎, 左波, 马晓旭等.(S)-噻吗洛尔半水合物的合成及表征[J]. 武汉工程大学学报, 2020, 42(06):628-632.
[6] 纪德华. (S)-卡替洛尔与(S) -美托洛尔的合成[D]. 河北科技大学, 2009.
欢迎您浏览更多关于左旋环氧氯丙烷的相关新闻资讯信息