Галогенированные алифатические углеводороды
Галогенированный алифатический углеводород представляет собой производное, в котором атом водорода в углеводороде с открытой цепью заменен элементом галогена, то есть производным фтора, хлора, брома или йода.
По структуре углеводородов их можно разделить на насыщенные галогенированные углеводороды (галогенированные алканы) и ненасыщенные галогенированные углеводороды (например, галогенированные олефины).
По числу атомов галогена, содержащихся в молекуле, его делят на галогенсодержащие соединения, дигалогениды и полигалогениды.
Физические и химические свойства производных сильно различаются. При комнатной температуре обычные низшие галогенированные углеводороды (C1~C4) представляют собой газ, высшие галогенированные углеводороды (> C16) представляют собой твердое вещество, среднее из двух - жидкость. В молекулах галоидоуглеводородов, если углеводород один и тот же, то доля и температура кипения хлорированных углеводородов самые низкие, а йодированных углеводородов самые высокие. Если галоген тот же, температура кипения увеличивается с увеличением молекулярной массы. Подавляющее большинство галогенированных углеводородов нерастворимы в воде и растворимы в органических растворителях. Галоген представляет собой функциональную группу галогенированных углеводородов, химическая активность которых в основном определяется атомом галогена. Вообще говоря, связь углерод-галоген более активна, чем связь углерод-углерод или связь углерод-водород, легко разрывается, приобретает характер нуклеофила. Кроме того, активность атомов галогена сильно связана со строением группы, которая непосредственно связана с атомами галогена. Галогеналканы являются достаточно активными соединениями, при этом некоторые галогены в галогенолефинах очень активны, некоторые не активны, их активность зависит от расположения галогена и двойной связи. По биологической активности бромированные и йодированные углеводороды более токсичны, чем хлорированные; фторированные углеводороды химически стабильны и менее токсичны, за некоторыми исключениями.
Галогенированные углеводороды, обычно используемые в промышленности, представляют собой в основном летучие жидкости. Большинство галогенированных углеводородов не являются горючими и взрывоопасными, обычно используются в качестве растворителей, химического сырья или промежуточных продуктов, а также широко используются в сельском хозяйстве, медицине и легкой промышленности.
- структура:
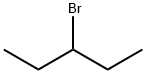
- имя:3-бромпентан
- Номер CAS:1809-10-5
- молекулярная формула:C5H11Br
- структура:
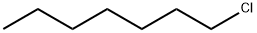
- имя:1-хлоргептана
- Номер CAS:629-06-1
- молекулярная формула:C7H15Cl
- структура:
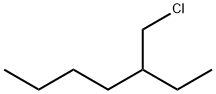
- имя:3- (хлорметил) гептан
- Номер CAS:123-04-6
- молекулярная формула:C8H17Cl
- структура:
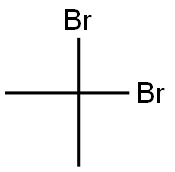
- имя:2,2-дибромпропан
- Номер CAS:594-16-1
- молекулярная формула:C3H6Br2
- структура:
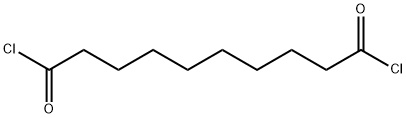
- имя:Хлорид Sebacoyl
- Номер CAS:111-19-3
- молекулярная формула:C10H16Cl2O2
- структура:
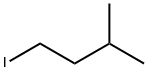
- имя:1-Иод-3-метилбутан
- Номер CAS:541-28-6
- молекулярная формула:C5H11I
- структура:
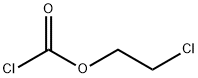
- имя:2-хлорэтил хлорформиа
- Номер CAS:627-11-2
- молекулярная формула:C3H4Cl2O2
- структура:
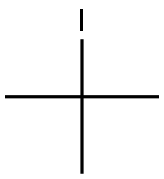
- имя:2-иод-2-метилпропан
- Номер CAS:558-17-8
- молекулярная формула:C4H9I
- структура:
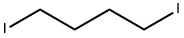
- имя:1,4-дииодбутана
- Номер CAS:628-21-7
- молекулярная формула:C4H8I2
- структура:
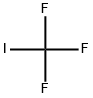
- имя:Трифторметилиодид
- Номер CAS:2314-97-8
- молекулярная формула:CF3I
- структура:

- имя:1-хлор-3-йодпропан
- Номер CAS:6940-76-7
- молекулярная формула:C3H6ClI
- структура:
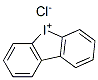
- имя:Хлорид Diphenyleneiodonium
- Номер CAS:4673-26-1
- молекулярная формула:C12H8ClI
- структура:
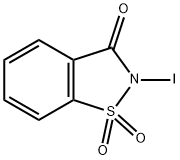
- имя:N-йодосахарин
- Номер CAS:86340-94-5
- молекулярная формула:C7H4INO3S
- структура:

- имя:1-бром-4-метоксибутан
- Номер CAS:4457-67-4
- молекулярная формула:C5H11BrO
- структура:
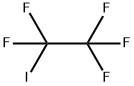
- имя:Йодпентафторэтан
- Номер CAS:354-64-3
- молекулярная формула:C2F5I
- структура:
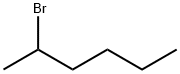
- имя:2-бромгексан
- Номер CAS:3377-86-4
- молекулярная формула:C6H13Br
- структура:
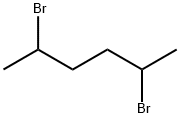
- имя:2,5-дибромгексана
- Номер CAS:24774-58-1
- молекулярная формула:C6H12Br2
- структура:
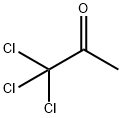
- имя:1,1,1-ТРИХЛОРАЦЕТОН
- Номер CAS:918-00-3
- молекулярная формула:C3H3Cl3O
- структура:
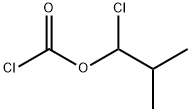
- имя:1-хлор-2-метилпропил хлорформиа
- Номер CAS:92600-11-8
- молекулярная формула:C5H8Cl2O2
- структура:
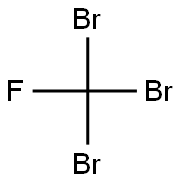
- имя:Tribromofluoromethane
- Номер CAS:353-54-8
- молекулярная формула:CBr3F
- структура:
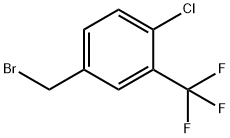
- имя:4-Хлор-3-(трифторметил) бензилбромида
- Номер CAS:261763-23-9
- молекулярная формула:C8H5BrClF3
- структура:
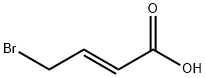
- имя:4-БРОМОКРОТОНОВАЯ КИСЛОТА
- Номер CAS:13991-36-1
- молекулярная формула:C4H5BrO2
- структура:
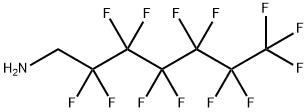
- имя:1H, 1H-ПЕРФТОРОГЕПТИЛАМИН
- Номер CAS:423-49-4
- молекулярная формула:C7H4F13N
- структура:
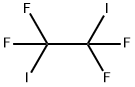
- имя:1,2-Diiodotetrafluoroethane
- Номер CAS:354-65-4
- молекулярная формула:C2F4I2
- структура:
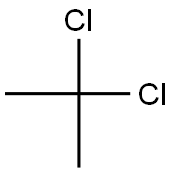
- имя:2,2-дихлорпропан
- Номер CAS:594-20-7
- молекулярная формула:C3H6Cl2
- структура:
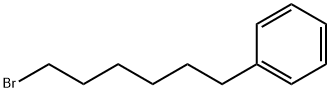
- имя:1-Бром-6-фенилгексан
- Номер CAS:27976-27-8
- молекулярная формула:C12H17Br
- структура:
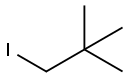
- имя:Неопентил йодид
- Номер CAS:15501-33-4
- молекулярная формула:C5H11I
- структура:
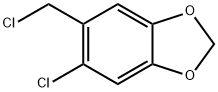
- имя:Хлорид 6-Chloropiperonyl
- Номер CAS:23468-31-7
- молекулярная формула:C8H6Cl2O2
- структура:
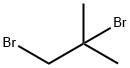
- имя:1,2-дибром-2-метилпропан
- Номер CAS:594-34-3
- молекулярная формула:C4H8Br2
- структура:
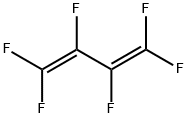
- имя:ГЕКСАФТОР-1,3-БУТАДИЕН
- Номер CAS:685-63-2
- молекулярная формула:C4F6
- структура:
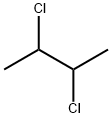
- имя:2,3-дихлорбутана
- Номер CAS:7581-97-7
- молекулярная формула:C4H8Cl2
- структура:
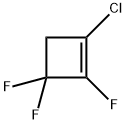
- имя:1-хлор-2 ,3,3-trifluorocyclobutene
- Номер CAS:694-62-2
- молекулярная формула:C4H2ClF3
- структура:
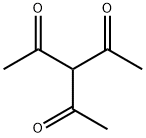
- имя:Триацетилметан
- Номер CAS:815-68-9
- молекулярная формула:C7H10O3
- структура:
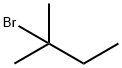
- имя:2-Бром-2-метилбутан
- Номер CAS:507-36-8
- молекулярная формула:C5H11Br
- структура:
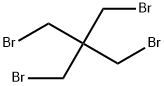
- имя:ПЕНТАЭРИТРИТИЛ ТЕТРАБРОМИД
- Номер CAS:3229-00-3
- молекулярная формула:C5H8Br4
- структура:
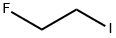
- имя:1-фтор-2-йодэтан
- Номер CAS:762-51-6
- молекулярная формула:C2H4FI
- структура:
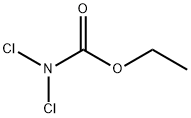
- имя:DCU
- Номер CAS:13698-16-3
- молекулярная формула:C3H5Cl2NO2
- структура:
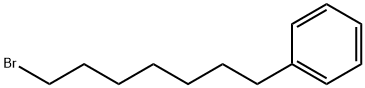
- имя:1-Bromo-7-phenylheptane
- Номер CAS:78573-85-0
- молекулярная формула:C13H19Br
- структура:
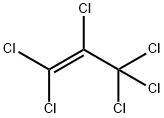
- имя:Гексахлорпропен
- Номер CAS:1888-71-7
- молекулярная формула:C3Cl6
- структура:
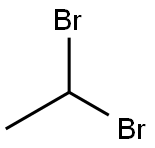
- имя:1,1-дибромэтан
- Номер CAS:557-91-5
- молекулярная формула:C2H4Br2
- структура:
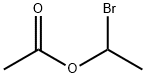
- имя:1-Бромэтилацетат
- Номер CAS:40258-78-4
- молекулярная формула:C4H7BrO2
- структура:
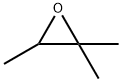
- имя:2,3-ЭПОКСИ-2-МЕТИЛБУТАН
- Номер CAS:5076-19-7
- молекулярная формула:C5H10O
- структура:
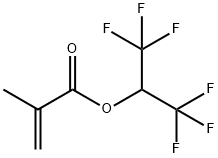
- имя:1,1,1,3,3,3-гексафторизопропилового метакрила
- Номер CAS:3063-94-3
- молекулярная формула:C7H6F6O2
- структура:
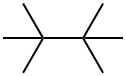
- имя:2,2,3,3-тетраметилбутан
- Номер CAS:594-82-1
- молекулярная формула:C8H18
- структура:
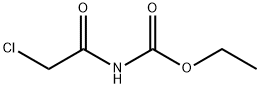
- имя:N-ХЛОРАЦЕТИЛ УРЕТАН
- Номер CAS:6092-47-3
- молекулярная формула:C5H8ClNO3
- структура:
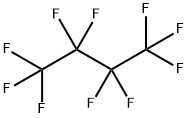
- имя:ДЕКАФТОРОБУТАН
- Номер CAS:355-25-9
- молекулярная формула:C4F10
- структура:
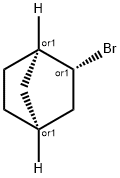
- имя:EXO-2-БРОМОНОРБОРНАН
- Номер CAS:2534-77-2
- молекулярная формула:C7H11Br
- структура:
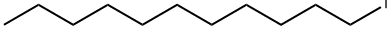
- имя:1-ЙОДУНДЕКАН
- Номер CAS:4282-44-4
- молекулярная формула:C11H23I
- структура:
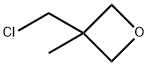
- имя:2-(ХЛОРМЕТИЛ)-2-МЕТИЛ-1,3-ЭПОКСИПРОПАН
- Номер CAS:822-48-0
- молекулярная формула:C5H9ClO
- структура:
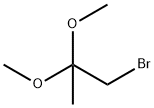
- имя:1-Бром-2 ,2-диметоксипропана
- Номер CAS:126-38-5
- молекулярная формула:C5H11BrO2
- структура:
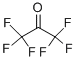
- имя:1,1,1,3,3,3-гексафторацетон полуторагидрат
- Номер CAS:13098-39-0
- молекулярная формула:C3H2F6O2
- структура:
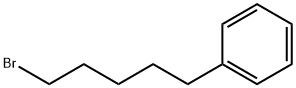
- имя:1-бром-5-фенилпентан
- Номер CAS:14469-83-1
- молекулярная формула:C11H15Br
- структура:
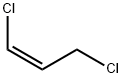
- имя:цис-1,3-дихлорпропен
- Номер CAS:10061-01-5
- молекулярная формула:C3H4Cl2
- структура:
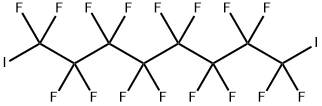
- имя:1,8-дииодперфтороктан
- Номер CAS:335-70-6
- молекулярная формула:C8F16I2
- структура:
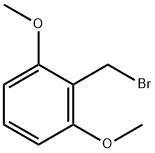
- имя:2,6-диметоксибензилбромид
- Номер CAS:169610-52-0
- молекулярная формула:C9H11BrO2
- структура:
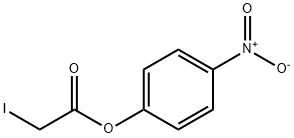
- имя:4-НИТРОФЕНИЛ ЙОДОАЦЕТАТ
- Номер CAS:31252-85-4
- молекулярная формула:C8H6INO4
- структура:
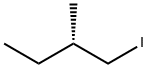
- имя:(S) - (+) - 1-йод-2-метилбутан
- Номер CAS:29394-58-9
- молекулярная формула:C5H11I
- структура:
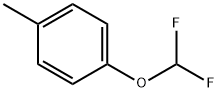
- имя:4-(ДИФТОРМЕТОКС)ТОЛУОЛ
- Номер CAS:1583-83-1
- молекулярная формула:C8H8F2O
- структура:
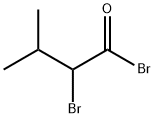
- имя:2-Бром-3-метилбутаноилбромид
- Номер CAS:26464-05-1
- молекулярная формула:C5H8Br2O