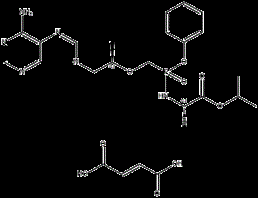
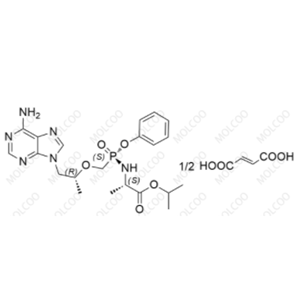
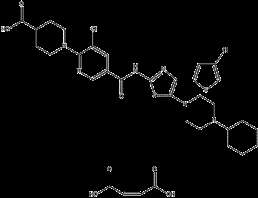
替诺福韦艾拉酚胺富马酸盐
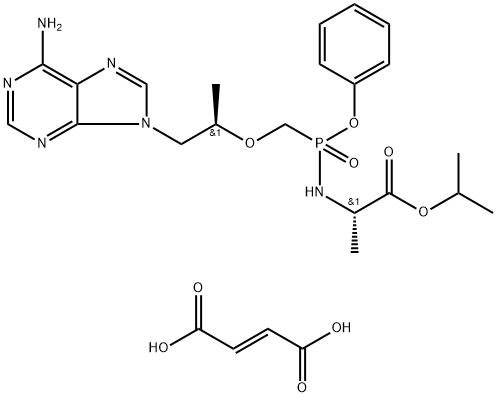
- 中文名称:替诺福韦艾拉酚胺富马酸盐
- 中文别名:替诺福韦艾拉酚胺富马酸盐;替诺福韦艾拉酚胺富马酸;替诺福韦艾拉酚胺富马酸半盐;替诺福韦艾拉芬胺半富马酸;替诺福韦艾拉芬胺;富马酸磷丙替诺福韦;替诺福韦艾拉酚胺富马酸盐 50MG;泰诺福韦艾拉酚胺富马酸
- 英文名称:Tenofovir alafenamide hemifumarate
- CAS No:1392275-56-7
- EINECS号:805-448-8
- 分子式:C25H33N6O9P
- 产品类别:原料药
全国(46)筛选

(Tenofovir alafenamide : fumarate = 2:1)
现货
纯度:99% 化工级 沧州恩科医药科技,大量现货,优势产品,欢迎询价下单,随时为您服务!
类别:中间体
品牌:沧州恩科
包装:1元/元/公斤
询价
河北沧州
沧州恩科医药科技有限公司

替诺福韦艾拉酚胺半富马酸盐 1392275-56-7
纯度:99% 化工级 沧州恩科医药科技,大量现货,优势产品,欢迎询价下单,随时为您服务!
类别:中间体
包装:1元/元
询价
北京
沧州恩科医药科技有限公司

?1392275-56-7富马酸丙酚替诺福韦;纯度≥98.0%高纯精品试剂;湖北研科时代科技-“研”无止境;“科”学创新!检测图谱;MSDS等技术支持
纯度:≥98.0%
类别:精品科研试剂
品牌:湖北研科时代
包装:10元/G
询价
湖北武汉
湖北研科时代科技有限公司
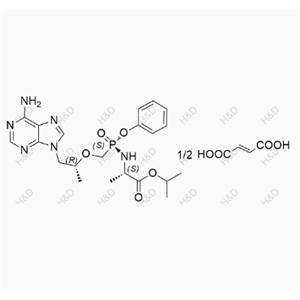
1392275-56-7 替诺福韦艾拉酚胺半富马酸盐 Tenofovir Alafenamide Hemifumarate salt
纯度:>95%
类别:杂质对照品
品牌:H&D
包装:10元/mg
询价
广东深圳
深圳市恒丰万达医药科技有限公司
最新产品
-

-

-
 74150-27-9匹莫苯丹(精品科研试剂)-“研”无止境;“科”学创新!专业之选 品质护航-湖北研科时代科技-支持三方验证;支持定制;检测图谱;MSDS等技术支持!74150-27-9询价2026-04-03
74150-27-9匹莫苯丹(精品科研试剂)-“研”无止境;“科”学创新!专业之选 品质护航-湖北研科时代科技-支持三方验证;支持定制;检测图谱;MSDS等技术支持!74150-27-9询价2026-04-03 -
-

用途
吉利德公司的新药Vemlidy(替诺福韦艾拉酚胺富马酸盐,25mg,每日一次)获得美国FDA批准,用于代偿性肝病的慢性乙肝病毒感染。Vemlidy是一种创新的靶向性替诺福韦前药,与先前产品300mg的Viread(替诺福韦酯富马酸盐,tenofovir disoproxil fumarate) 相比,只需要少于十分之一的剂量便可获得相似的抗病毒效用。临床数据显示,Vemlidy具有更好的血浆稳定性,同时能够更有效地将替诺福韦递送给肝细胞。由于用药剂量更低,Vemlidy能够改善患者肾脏和骨骼的安全风险。Vemlidy在两个国际型III期临床试验(研究108和研究110)中,获得了长达48周的数据支持。共有1298名初治和有治疗史的慢性HBV感染成人患者参与了上述试验。研究108和研究110分别招募了425例HBeAg阴性患者和873名HBeAg阳性患者使用Vemlidy或Viread做对比治疗。两个研究都达到了主要临床研究终点:在治疗第48周后,Vemlidy治疗组中血浆HBV的DNA水平低于29 IU/mL的人数百分比不低于Viread组。对数据分析后发现,Vemlidy治疗组患者的骨骼、肾脏实验室参数相比Viread治疗组有明显改善,且血清转氨酶水平恢复正常的比例更高。Vemlidy和Viread在两项研究中耐受性均良好,因为不良事件终止治疗的人数比例分别为1%和1.2%,主要不良反应包括头痛、腹痛、疲劳、咳嗽、恶心、背痛,且发生率相似。Vemlidy在产品标签中有一个黑框警告,提示其潜在的乳酸中毒风险、严重的脂肪性的肝肿大风险和用药后急性乙肝加重的风险。