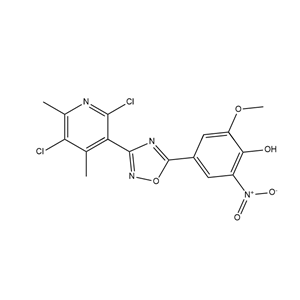
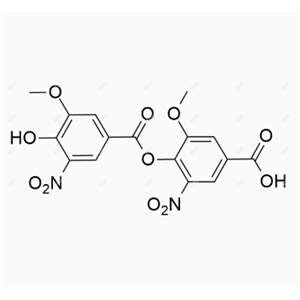
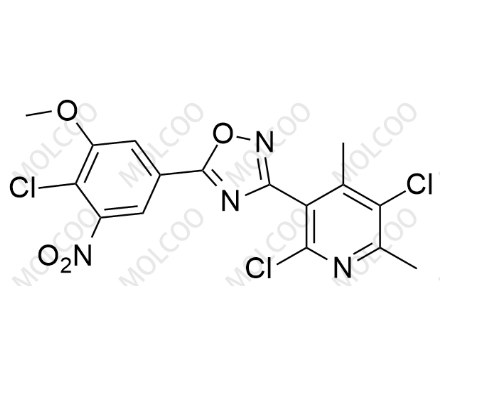
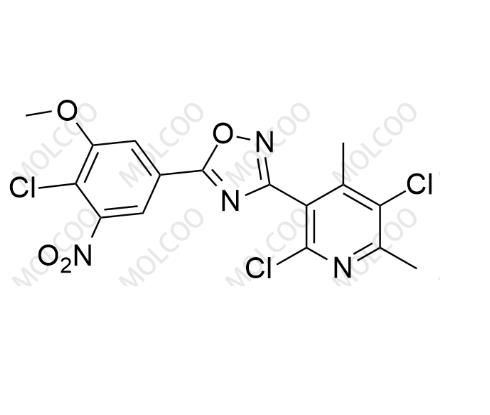
奥匹卡朋杂质39

联系方式:杜经理 TEL: 17320513646(微信同号) QQ: 2853567688
产品编号:O022039
英文名:Opicapone Impurity 39
英文别名:5-(4-chloro-3-methoxy-5-nitrophenyl)-3-(2,5-dichloro-4,6-dimethylpyridin-3-yl)-1,2,4-oxadiazole(注:核心结构为 1,2,4 - 恶二唑环连接双芳环,含 4 - 氯 - 3 - 甲氧基 - 5 - 硝基苯基、2,5 - 二氯 - 4,6 - 二甲基吡啶 - 3 - 基特征取代基,是奥匹卡朋合成中的芳环偶联类中间体杂质)
CAS 号:无
分子式:C16H11Cl3N4O4
分子量:429.64
结构专属与纯度双优:纯度经 HPLC 与 LC-MS 双重验证,明确含 1,2,4 - 恶二唑环、三氯取代(3 个 Cl 原子)、硝基(-NO₂)、甲氧基(-OCH₃)及二甲基吡啶特征结构,与奥匹卡朋主峰(含脲基与单恶二唑环,氯取代数量及芳环结构不同)差异显著,可作为合成过程中 “双芳环 - 恶二唑” 类中间体杂质的专属对照,避免与其他杂质(如单氯取代类似物、无硝基杂质)交叉干扰,确保定性定量结果精准。
稳定性适配抗帕金森药检测场景:在避光、干燥、常温(15-25℃)储存条件下,恶二唑环稳定性高,无明显水解风险;碳 - 氯键、甲氧基与芳环连接牢固,硝基无还原分解迹象,能保障多批次检测数据的重复性与准确性,适配奥匹卡朋原料药及片剂的长期质量监控需求。
溶解性与分离性能优异:分子以疏水芳环(双苯环、吡啶环)为主,可溶于二氯甲烷、甲醇 - 乙腈(1:1)等有机溶剂;通过反相高效液相色谱(RP-HPLC),以 C18 柱与乙腈 - 水(含 0.1% 甲酸)梯度洗脱,能与奥匹卡朋主峰及制剂辅料(如乳糖、硬脂酸镁)实现基线分离,检测限可达 μg 级,满足中间体杂质常规监控需求。
核心杂质监控场景:用于奥匹卡朋原料药及片剂的质量控制,重点监测 “双芳环 - 恶二唑” 类中间体杂质含量 —— 作为儿茶酚 - O - 甲基转移酶(COMT)抑制剂(辅助治疗帕金森病),奥匹卡朋的合成需通过芳环偶联构建恶二唑环,若该中间体未完全转化(如后续脲基化反应不完全),易残留于终产品,精准检测可避免杂质影响药效或增加中枢神经系统代谢负担。
工艺优化的关键参照:辅助排查杂质生成源头,例如合成中 “4 - 氯 - 3 - 甲氧基 - 5 - 硝基苯甲酰氯” 与 “2,5 - 二氯 - 4,6 - 二甲基吡啶 - 3 - 基脒” 的恶二唑环合反应不完全、偶联试剂(如三乙胺)用量不足等问题,通过调整反应温度(控制在 80-90℃)、优化投料比(脒过量 10%),减少该杂质的残留量。
检测方法开发与验证:作为标准品用于 HPLC-UV 或 LC-MS 检测方法的验证,确认方法的线性范围(通常为 0.1-20 μg/mL)、回收率(95%-105%)及精密度(RSD<2%)—— 针对制剂中辅料的基质干扰,可通过选择 270 nm(硝基与芳环的特征吸收峰)作为检测波长,或采用 LC-MS 监测分子离子峰 m/z 430.0([M+H]+,含氯同位素峰),提升检测特异性。
奥匹卡朋是一种选择性、可逆性儿茶酚 - O - 甲基转移酶(COMT)抑制剂,通过抑制左旋多巴的外周代谢,提高脑内左旋多巴浓度,临床用于辅助治疗帕金森病(与左旋多巴 / 卡比双多巴联用),患者需长期服药以改善运动症状、减少 “开关” 现象。
奥匹卡朋杂质 39 是其合成过程中的关键中间体杂质:奥匹卡朋的核心结构构建需以 “4 - 氯 - 3 - 甲氧基 - 5 - 硝基苯甲酸” 与 “2,5 - 二氯 - 4,6 - 二甲基吡啶 - 3 - 基脒” 为原料,经酰氯化、环合反应形成 1,2,4 - 恶二唑环中间体(即该杂质),再通过脲基化反应引入目标官能团;若脲基化反应效率不足(如异氰酸酯试剂用量不足、反应时间过短),该中间体便会残留于终产品中。
由于帕金森病患者多为老年人,肝肾功能衰退,对药物杂质的耐受性低,该中间体杂质的残留可能增加不良反应风险(如胃肠道刺激、肝功能异常)。因此,对该杂质的研究与控制,是保障帕金森病患者用药安全、符合 FDA(美国食品药品监督管理局)、EMA(欧洲药品管理局)对中枢神经系统药物杂质控制要求的关键环节。
检测技术成熟度:当前主流检测方法为 RP-HPLC-UV,采用 C18 色谱柱(如 Waters XBridge C18),以乙腈 - 0.1% 甲酸水为流动相进行梯度洗脱,检测波长 270 nm,可在 18 分钟内实现杂质与主峰的分离,定量限(LOQ)可达 0.05 μg/mL,满足 “中间体杂质限量<0.5%” 的常规要求;对于痕量分析,LC-MS/MS 技术可通过监测 m/z 430.0→356.0(失去硝基片段)的特征离子对,进一步提升灵敏度至 ng 级,有效规避其他氯代杂质干扰。
生成机制明确性:研究证实,该杂质的残留主要与 “脲基化反应转化率” 相关 —— 若反应体系中叔丁基异氰酸酯用量不足(<1.1 当量),或反应温度过低(<60℃),恶二唑中间体无法完全转化为脲基衍生物;此外,中间体精制时若仅采用单一溶剂(如乙醇)重结晶,可能因杂质与目标产物溶解度差异小导致残留。基于此,工艺优化方向已明确为 “足量异氰酸酯试剂 + 适宜反应温度(70-75℃)+ 两步精制(乙醇 - 水重结晶 + 柱层析)”。
安全性与标准进展:毒理学研究显示,该中间体杂质无 COMT 抑制活性,短期暴露无明显急性毒性,但长期高剂量暴露可能轻微影响肝细胞线粒体功能;目前,FDA 已在奥匹卡朋的药品生产质量管理规范(GMP)要求中提及该中间体的监控,USP(美国药典)、EP(欧洲药典)在奥匹卡朋质量标准草案中,正逐步将其列为需控制的中间体杂质,建议限量为<0.5%,现有研究数据为限量设定提供了核心依据。
联系方式:杜经理 TEL: 17320513646(微信同号) QQ: 2853567688
备注:我们也可以定制相关类似物和修饰肽,提供包括高效液相色谱(HPLC)、质谱(MS)、核磁共振氢谱(1H-NMR)、质谱(MS)、高效液相色谱(HPLC)、红外光谱(IR)、紫外光谱(UV)、分析报告(COA)、物质安全数据表(MSDS)等资料。本产品仅用于实验室用途!