蛇床子素的化学性质
| CAS 编号 | 484-12-8 | SDF 系列 | 下载 SDF |
| PubChem 编号 | 10228 | 外观 | 白色粉末 |
| 公式 | C15H16O3 | M.Wt | 244.3 |
| 化合物类型 | 香 豆 素 | 存储 | 在 -20°C 下干燥 |
| 同义词 | NSC 31868;奥斯托尔;奥斯托尔 |
| 溶解度 | DMSO:125 毫克/毫升(511.69 毫米;需要超声波和加热) |
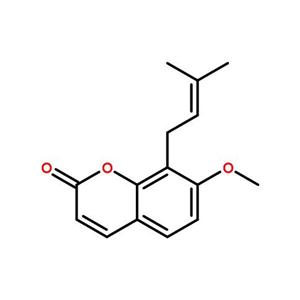
| 化学名称 | 7-甲氧基-8-(3-甲基丁-2-烯基)铬-2-酮 |
| 一般提示 | 为了获得更高的溶解度,请在 37 °C 下加热试管,并在超声波浴中摇晃一会儿。储备液可在 -20°C 以下储存数月。
我们建议您在同一天准备并使用该解决方案。但是,如果测试计划需要,可以提前制备储备液,并且储备液必须密封并储存在 -20°C 以下。一般来说,储备溶液可以保存几个月。
使用前,我们建议您将样品瓶在室温下放置至少一个小时,然后再打开。 |
| 关于打包 | 1. 产品包装在运输过程中可能会颠倒,导致高纯度化合物粘附在小瓶的颈部或瓶盖上。从包装中取出 vail 并轻轻摇晃,直到化合物落到样品瓶底部。
2. 对于液体产品,请以 500xg 离心,以将液体收集到样品瓶底部。
3. 实验过程中尽量避免丢失或污染。 |
| 运输条件 | 根据客户要求包装(5mg、10mg、20mg 等)。 |
蛇床子素 的来源
1 柑橘属 2 蛇床子属 3 帕斯蒂纳卡属
蛇床子素 的生物活性
| 描述 | Osthol 是一种天然的抗组胺药替代品,可能是组胺 H1 受体活性的潜在抑制剂。Osthol 具有毒性,可用作生物杀虫剂。Osthol 是人 Pgp 和金黄色葡萄球菌多药外排泵的抑制剂,可逆转对一线抗菌药物的耐药性。Osthol 具有抗过敏、抗骨质疏松、抗脂肪肝、抗肿瘤和心脏保护作用。 Osthol 抑制肝脏 SREBP-1c/2 mRNA 表达和随后对 SREBP-1c/2 介导的靶基因如 FAS、CYP7A 和 LDL 受体的调节;它可以通过 BMP-2/p38MAPK/Runx-2/osterix 通路刺激大鼠颅骨成骨细胞培养物的成骨细胞分化。 |
| 体外 | 使用两种水生生物对生物农药中 Osthol 含量进行急性毒性评估。本研究的重点是通过使用两种水生生物生物来评估 Oshol 引起的急性毒性,Oshol 是环境友好型生物杀虫剂的主要成分。
方法和结果:
在大型水蚤中进行 Osthol 引起的急性毒性评估,并通过检查 Danio rerio 胚胎的形态学异常进行。 接种后 48 小时,Osthol 在 D. magna 中的中位有效浓度值为 19.3 μM。D. rerio 胚胎在 96 小时时的中位致死浓度为 30.6 μM。将 D. magna 和 D. rerio 中 Osthol 的无观察到效应浓度和预测无效应浓度计算为 5.4 和 0.19 μM。随着时间的推移,由于 Osthol 导致的 D. rerio 胚胎形态异常增加。在 24-48 小时时,胚胎观察到凝血、孵化延迟、卵黄囊水肿、心包水肿和色素沉着。72 小时后出现脊柱侧凸和头部水肿的症状。此外,在 96 小时内在受精胚胎组织中观察到弯曲的尾巴、眼部缺陷和塌陷症状。眼部缺陷和色素沉着是本研究中观察到的额外症状。
结论:
由于 Osthol 显示出相当大的毒性水平,因此当使用含有 Osthol 的生物杀虫剂时,有必要在农业生态系统中进行持续的毒性评估。 蛇床床子 Osthol 的抗肿瘤作用:体外和体内研究。蛇床子 (L.) Cusson 是一种中药,被传统医学医生广泛使用。Osthol 是该草药的主要生物活性化合物。
方法和结果:
在本研究中,从 C. monnieri 中分离出 Osthol 并研究了其体外和体内抗肿瘤作用。体外研究结果表明:Osthol 以时间和浓度依赖性方式抑制 HeLa 的生长,IC(50) 值分别为 77.96 和 64.94 μm,持续 24 小时和 48 小时;Osthol 在原代培养的正常宫颈成纤维细胞中具有较低的细胞毒性作用;用 Osthol 处理后,HeLa 中的 DNA 片段化增加并激活 PARP,可诱导细胞凋亡。体内模型结果显示,每天一次给予 Oshol (30 mg/kg) 持续 9 天后,P-388 D1 荷瘤 CDF(1) 小鼠的存活天数延长 (ILS% = 37)。
结论:
基于这些结果,建议 Osthol 在体内抑制 P-388 D1 细胞,在体外诱导 HeLa 细胞凋亡,并且 Osthol 是开发抗肿瘤药物的良好先导化合物。然而,台湾特有植物的 C. formosanum Yabe 含有少量的骨片醇,不含 Imperatorin,其主要成分与 C. monnieri 不同。因此,有人认为 C. formosanum 也可能具有经济价值。 |
| 体内 | Osthol 通过减少甘油三酯合成而不是通过胰岛素抵抗来减轻肝脂肪变性。通过多方面分析评估 Osthol 对肝内脂肪合成、β氧化、炎症和胰岛素抵抗的影响。
方法和结果:
将 Sprague-Dawley 大鼠 (n = 30) 随机分为对照组、非酒精性脂肪肝 (NAFLD) 和 Osthol 组。NAFLD 和 Osthol 组饲喂高脂饮食 14 周。高脂饮食 8 周后,Osthol 组也接受 Osthol 20 mg/kg 口服 5 次/周。为了评估胰岛素抵抗,在 14 周结束时进行口服葡萄糖耐量。动物处死 14 周后对肝组织提取物进行免疫组织化学 (4-HNE, F4/80) 和苏木精和伊红 (HE) 染色。用逆转录-聚合酶链反应评估 SREBP1c 、 FAS 、 SCD-1 、 PPAR-α、 CROT、 MCP-1 、 IRS-1 和 IRS-2 mRNA 表达。 HE 染色显示,与 NAFLD 组相比,Osthol 组肝内脂肪含量显著降低 (39.4% vs 21.0%;P = 0.021)。与对照组相比,NAFLD 组的 SREBP1c 表达增加 (P = 0.0001),而与 NAFLD 组相比,Osthol 治疗降低 SREBP1c 表达 (P = 0.0059)。在 Osthol 组中,与 NAFLD 组相比,作用于 SREBP1c 下游的肝内 FAS 和 SCD-1 显着降低。此外,Osthol 组的 PPAR-α 表达也显著高于 NAFLD 组 (P = 0.0147)。
结论:
骨片醇治疗通过减少肝脏甘油三酯的新合成来减轻肝脏脂肪变性,对胰岛素抵抗和肝脏炎症有名义影响。 鸵逸醇减少大鼠心脏肥大与心脏氧化应激和脂质代谢的调节有关。本研究的目的是检查从蛇床子 (L.) Cusson 果实中分离的香豆素化合物 Oshol 对大鼠心脏肥大的治疗效果,并探讨其潜在机制。
结论:
肾血管性高血压诱导心脏肥大大鼠灌胃口服 Osthol 4 周。结果显示,乙片醇 20 mg/kg 组血压、心脏体重指数和心肌丙二醛含量降低 (p < 0.001,p = 0.002 和 p = 0.025),心肌超氧化物歧化酶和谷胱甘肽过氧化物酶含量增加 (p < 0.001),心肌组织中未酯化脂肪酸和三酰甘油升高降低 (p = 0.017 和 p = 0.004, 分别)。同时,Osthol 20 mg/kg 组心肌过氧化物酶体增殖物激活受体 (PPAR)-α 和肉碱棕榈酰转移酶 (CPT)-1a mRNA 表达增加,心肌甘油二酰基酰基转移酶 (DGAT) mRNA 表达降低 (p < 0.001)。Osthol 治疗与心肌细胞横截面积减少有关 (p < 0.001)。
结论:
这些发现表明 Osthol 可能对大鼠心脏肥大发挥治疗作用,其机制可能通过调节 PPARα 介导的靶基因表达(包括 CPT-1a mRNA 表达的增加和 DGAT mRNA 表达的降低)与心肌氧化应激和脂质代谢的改善有关。 |
蛇床子素 协议
| 激酶检测 | 奥斯托醇和姜黄素作为人 Pgp 和金黄色葡萄球菌多药外排泵的抑制剂:逆转对一线抗菌药物的耐药性筛选了 302 个小分子的内部 IIIM 天然产物库,以确定它们在 Pgp 过表达的人腺癌 LS-180 细胞中抑制 p-糖蛋白 (Pgp) 的能力。
方法和结果:
筛选确定了 13 种表现出显著 Pgp 抑制活性的天然产物,包括 praeruptorin B、姜黄素、前胡素、Osthol、5,7-二乙酰氧基-8-(3-甲基-2-丁烯基)-香豆素、5,7-二羟基-8-(3-甲基-2-丁烯基)香豆素、pongamol、phellopterin、tangerettin、3-(2-甲基But-3-en-2-yl)黄素、7-demethyl Osthol、allorottlerin 和四氢angeolide。然后筛选这些天然产物对 Nor A (金黄色葡萄球菌)、Mde A (金黄色葡萄球菌 Mupr-1)、Tet K (金黄色葡萄球菌 SA-K2192) 和 Msr A (金黄色葡萄球菌 SA-K2191) 外排泵的细菌外排泵抑制活性的影响。
结论:
姜黄素和奥斯托醇对金黄色葡萄球菌 NorA 外排泵有显著抑制作用,环丙沙星的 MIC 在 25 μM 时分别降低了 8 倍和 4 倍。姜黄素和奥斯特霍尔与人 Pgp 和金黄色葡萄球菌 Nor A 外排泵的分子对接研究确定了这些天然产物的合理结合模式和结合位点。 |
| 细胞研究 | Oshol 是一种从常见的蛇床子果实中分离的香豆素,可在体外增强成骨细胞的分化和成熟。点击化学启发了鸵鸟醇的新型三唑基衍生物作为有效的细胞毒性药物的合成和生物评价。使用点击化学方法合成了一系列通过内酯环打开的 Osthol 羟基 (1) 连接的新的不同三唑类。
方法和结果:
对所有衍生物进行 3-(4,5-二甲基噻唑-基)-二苯基四唑溴化物 (MTT) 细胞毒性筛选,针对一组 7 种不同的人类癌细胞系,即结肠 (COLO-205)、结肠 (HCT-116)、乳腺癌 (T47D)、肺 (NCI-H322)、肺 (A549)、前列腺 (PC-3) 和皮肤 (A-431),以检查它们的细胞毒潜力。有趣的是,在测试的分子中,大多数类似物显示出比母体 Osthol 更好的细胞毒活性 (1)。在合成的三唑类化合物中,化合物 8 对结肠 (Colo-205 和 HCT-116)、乳腺癌 (T47D)、肺 (NCI-H322 和 A549)、前列腺 (PC-3) 和皮肤 (A-431) 癌系的 IC50 分别为 1.3、4.9、3.6、41.0、35.2、26.4 和 7.2 μM。化合物 8 在 Colo-205 细胞中诱导有效的凋亡作用。凋亡细胞群从阴性对照时的 11.4% 增加到 25 μM 时 8 的 24.1%。化合物 8 还诱导线粒体膜电位 (ΛΨm) 显着降低,导致所用癌细胞凋亡。
结论:
本研究鉴定了带有吸电子取代基的类似物的广谱细胞毒活性,此外还增强了具有电子供体部分的类似物的选择性活性。 在从新生 Wistar 大鼠分离的原代成骨细胞中研究 Osthol 对成骨细胞的影响。
方法和结果:
将骨片醇分别以 10⁻⁷ 、 10⁻⁶、 10⁻⁵ 和 10⁻⁴ mol/l 的浓度补充到培养基中。未发现对细胞增殖的刺激作用,但 10⁻⁵ mol/l Osthol 导致碱性磷酸酶 (ALP) 活性显着增加。在该浓度下检查一段时间内的成骨分化标志物,并与未补充 Oshol 的对照细胞进行比较。结果显示,用 Oshol 处理的细胞的 ALP 活性、骨钙素分泌和钙沉积水平分别比对照细胞高 1.52、2.74 和 2.0 倍。ALP 组织化学染色和矿化骨结节测定的结果均显示,在 Oshol 处理的细胞中实现的数量和面积比对照细胞高 1.53 倍。还研究了与骨骼发育相关的生长和转录因子碱性成纤维细胞生长因子、胰岛素样生长因子 I、骨形态发生蛋白 2 (BMP-2)、Runt 相关基因 2 (Runx-2) 和 osterix 的基因表达。mRNA 表达增加分别为 1.94 、 1.74 、 1.68 、 1.83 和 2.31 倍,比对照高。此外,Osthol 增加了 p38 丝裂原活化蛋白激酶 (MAPK) 和 I 型胶原蛋白的蛋白表达。与对照相比,Osthol 处理的细胞中 osthol 处理的细胞中的 p38MAPK 蛋白和胶原蛋白分别高 1.42 倍和 1.58 倍。
结论:
这些研究的结果支持这样一个结论,即 Osthol 显着增强培养成骨细胞的成骨分化。结果还表明,Osthol 可通过 BMP-2/p38MAPK/Runx-2/osterix 通路刺激大鼠颅骨成骨细胞培养物的成骨细胞分化,并且 Osthol 可能作为新型抗骨质疏松药物开发的重要化合物。 |
| 动物研究 | 刺胞胞菌 (Chromidium monnieri) 的干果)及其主要成分鸵鸟的抗过敏作用。Osthol 通过调节肝脏甾醇调节元件结合蛋白-1c/2 介导的靶基因表达来改善脂肪乳诱导的小鼠脂肪肝。本研究的目的是检查 Osthol(Ponidium monnieri (L.) Cusson (Apiaceae) 的活性成分)对高脂血症性脂肪肝小鼠的治疗效果,并探讨 Osthol 治疗的潜在机制。
方法和结果:
通过口服脂肪乳 4 周诱导高脂血症性脂肪肝小鼠模型。然后用 Osthol 10-40 mg/kg 处理实验小鼠 6 周。口服后,模型组和药物治疗组小鼠再次连续给予脂肪乳 2 周。此后,测量血清和肝脏中的脂质水平、肝脏权重系数和组织病理学评估。检测肝脏甾醇调节元件结合蛋白 (SREBP)-1c 、 SREBP-2 、脂肪酸合酶 (FAS) 、低密度脂蛋白 (LDL) 受体和胆固醇 7α-羟化酶 (CYP7A) mRNA 表达。结果显示,在 Osthol 治疗组中,血清和肝脏中总胆固醇、甘油三酯和游离脂肪酸水平以及肝脏重量系数随剂量的增加而逐渐降低。重要的是,肝脏标本的组织病理学评估表明 Osthol 可能会减少脂质积累。Osthol 可增加脂肪乳诱导的脂肪肝小鼠肝脏中 CYP7A 的 mRNA 表达,降低肝脏中 SREBP-1c 、 SREBP-2 、 FAS 和 LDL 受体的 mRNA 表达。
结论:
这些结果表明,Osthol 可能通过抑制肝脏 SREBP-1c/2 mRNA 表达和随后调节 SREBP-1c/2 介导的靶基因如 FAS 、 CYP7A 和 LDL 受体,对脂肪乳诱导的小鼠脂肪肝发挥治疗作用。 方法和结果:
研究了从刺胞子 (蛇床子干果) 中获得的 70% 乙醇提取物 (CM-ext) 对 48 小时同源被动皮肤过敏反应 (PCA) 、 2,4-二硝基氟苯 (DNFB) 诱导的接触性皮炎和苦味酰氯 (PC) 诱导的实验动物接触性皮炎的抗过敏作用 (I 型和 IV)。CM-ext 对这些过敏模型显示出抑制作用。从 CM-ext 中分离的 osthol 也具有抑制作用。
结论:
这些结果表明 Cnidii Monnieri Fructus 可能可用作过敏性疾病的药物,其抗过敏作用部分归因于香豆素衍生物 Osthol。 |
制备
Osthol
储备液
| 1 毫克 | 5 毫克 | 10 毫克 | 20 毫克 | 25 毫克 |
| 1 毫米 | 4.0933 毫升 | 20.4666 毫升 | 40.9333 毫升 | 81.8666 毫升 | 102.3332 毫升 |
| 5 毫米 | 0.8187 毫升 | 4.0933 毫升 | 8.1867 毫升 | 16.3733 毫升 | 20.4666 毫升 |
| 10 毫米 | 0.4093 毫升 | 2.0467 毫升 | 4.0933 毫升 | 8.1867 毫升 | 10.2333 毫升 |
| 50 毫米 | 0.0819 毫升 | 0.4093 毫升 | 0.8187 毫升 | 1.6373 毫升 | 2.0467 毫升 |
| 100 毫米 | 0.0409 毫升 | 0.2047 毫升 | 0.4093 毫升 | 0.8187 毫升 | 1.0233 毫升 |
| *注意:如果 你正在实验过程中,有必要制作 样品的稀释比例。上述稀释数据 仅供参考。通常,它可以变得更好 在较低浓度内的溶解度。 |
484-12-8是一个化学物质的CAS号,该物质指的是蛇床子提取物或蛇床子素,以下是对该物质的详细介绍:
一、基本信息
中文名称:蛇床子提取物/蛇床子素
英文名称:Osthole
CAS号:484-12-8
分子式:C15H16O3
分子量:244.29(或244.28574)
二、物理和化学性质
三、来源与提取
四、用途与功效
医药领域:蛇床子素具有解痉、降血压、抗心律失常、增强免疫功能及广谱抗菌作用,因此在医药领域有广泛应用
化妆品领域:由于其具有独特的杀虫抑菌活性,蛇床子素也被用于化妆品中,以提供额外的保护效果
农药领域:蛇床子素对多种害虫和植物病原真菌具有显著的作用,因此也被用作生长调节剂和农药增效剂
储存条件:通常需要在2~8°C的条件下储存,并保持密封和避光
运输要求:根据具体的危险品运输规定进行运输,确保安全
请注意,以上信息可能因不同的生产商和产品批次而有所差异。在实际应用中,请遵循具体产品的说明书和安全操作规程。