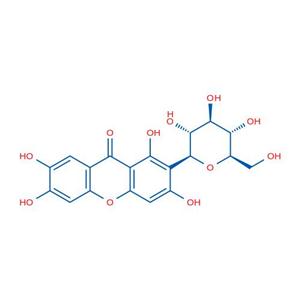
芒果苷的化学性质
| CAS 编号 | 4773-96-0 | SDF | 下载 SDF |
| PubChem 标识 | 5281647 | 外观 | 粉 |
| 公式 | C19H18O11 | M.Wt | 422.3 |
| 化合物的种类 | 氧杂蒽酮 | 存储 | 在 -20°C 下干燥 |
| 同义词 | Alpizarin;阿夫洛伊尔;奇诺明;甲壳素;赫迪萨里德;沙明;1,3,6,7-四羟基氧杂蒽酮 2-C-葡萄糖苷 |
| 溶解度 | DMSO:22 mg / mL(52.09 mM;需要超声波和加温) |
| 英文名称 | 1,3,6,7-四羟基-2-[(2S,3R,4R,5S,6R)-3,4,5-三羟基-6-(羟甲基)氧杂环戊烷-2-基]氧杂蒽-9-酮 |
| SMILES | C1=C2C(=CC(=C1O)O)OC3=CC(=C(C(=C3C2=O)O)C4C(C(C(C(O4)CO)O)O)O)O |
| 标准 InChIKey | AEDDIBAIWPIIBD-ZJKJAXBQSA-N |
| 标准 InChI | InChI=1S/C19H18O11/c20-4-11-15(25)17(27)18(28)19(30-11)12-8(23)3-10-13(16(12)26)14(24)5-1-6(21)7(22)2-9(5)29-10/h1-3,11,15,17-23,25-28H,4H2/t11-,15-,17+,18-,19+/m1/s1 |
| 一般提示 | 为了获得更高的溶解度,请在37°C下加热试管,并在超声波浴中摇晃一段时间。储备溶液可在 -20°C 以下储存数月。
我们建议您在同一天准备并使用该溶液。但是,如果测试计划需要,可以提前准备储备溶液,并且必须将储备溶液密封并储存在-20°C以下。一般来说,储备溶液可以保存几个月。
使用前,我们建议您将小瓶在室温下放置至少一个小时,然后再打开它。 |
| 关于包装 | 1.产品的包装在运输过程中可能会反转,导致高纯度化合物粘附在小瓶的颈部或瓶盖上。将滤瓶从包装中取出,轻轻摇晃,直到化合物落到小瓶底部。
2.对于液体产品,请以500xg离心,将液体聚集到小瓶底部。
3.尽量避免实验过程中的损失或污染。 |
芒果苷的来源
1 獐牙属 2 龙胆属 3 金丝桃属 4 芒果属 5 獐牙草属 6 獐牙草属
芒果苷的生物活性
| 描述 | 芒果苷是一种生物活性化合物,具有许多健康前景,并已用于制备药物和食品补充剂。芒果苷具有抗脂肪变性、抗癌、驱虫和抗过敏活性,对调节内皮稳态具有有益作用,可用于糖尿病心血管并发症的管理。芒果苷通过诱导miR-15b和抑制MMP-9表达来调节神经胶质瘤细胞的增殖和凋亡,减弱破骨细胞生成、骨吸收和RANKL诱导的NF-κB和ERK激活。 |
| 目标 | IL受体 |否 |半胱天冬酶 |考克斯 |MMP(例如TIMP) |阿克特 |ERK公司 |中国 |EGFR系列 |IKB公司 |ATP酶 |安普克 |罗斯 |NF-kB型 |第 65 页 |IKK公司 |
| 体外研究 | Mangiferin 通过诱导 microRNA-15b 和抑制 MMP-9 表达来调节神经胶质瘤细胞的增殖和凋亡。[Pubmed:25901555]Oncol Rep. 2015 年 6 月;33(6):2815-20.芒果苷是一种从芒果树桫椤科植物叶中提取的类黄酮,在许多方面具有生理活性和药理作用。
方法和结果:
本研究旨在阐明芒果苷对神经胶质瘤细胞增殖和凋亡的影响以及芒果苷这些疗效的机制。在本实验中,我们使用 3-(4,5-二甲基噻唑-2-基)-2,5 二苯基四唑溴化物 (MTT) 测定法检测增殖。然后,采用膜联蛋白V-FITC/碘化丙啶(PI)凋亡检测试剂盒、DAPI染色试验和caspase-3和caspase-9活性测定试剂盒检测U87神经胶质瘤细胞凋亡。接下来,采用实时荧光定量PCR和明胶酶法分别分析microRNA-15b(miR-15b)和基质金属蛋白酶-9(MMP-9)的表达。将MMP-9激动剂、miR-15b类似物和抗miR-15b类似物添加到U87神经胶质瘤细胞中,以阐明芒果苷的疗效机制。在本研究中,芒果苷显著抑制了U87神经胶质瘤细胞的增殖并增加了细胞凋亡。同时,芒果苷特异性促进了U87神经胶质瘤细胞中miR-15b的表达,抑制了MMP-9的水平。miR-15b 调节 U87 胶质瘤细胞中 MMP-9 的表达。MMP-9激动剂和抗miR-15b降低了芒果苷在U87神经胶质瘤细胞中的疗效。
结论:
芒果苷通过诱导miR-15b和抑制MMP-9表达调控胶质瘤细胞的增殖和凋亡。 |
| 体内研究 | 芒果提取物(Vimang)及其主要成分芒果苷对铁诱导的大鼠血清和肝脏氧化损伤的保护作用。[Pubmed:18243014 ]2008年1月药理学研究;57(1):79-86.
方法和结果:
研究了芒果 L 提取物 (Vimang) 或其主要成分芒果苷对铁过载损伤的体内预防作用,分别给予 50、100、250 mg kg(-1) 体重的 Vimang 或 40 mg kg(-1) 体重的芒果苷,在给予有毒量的铁-葡聚糖前 7 天和之后 7 天。Vimang或Mangiferin处理均可预防血清中的铁超载以及肝脏氧化应激,降低血清和肝脏脂质过氧化,血清GPx活性,并增加血清和肝脏GSH,血清SOD和动物的整体抗氧化状况。血清铁浓度降低,尽管在较高剂量下,Vimang倾向于增加它;转化铁蛋白饱和度百分比、肝脏重量/体重比、肝脏铁含量降低。治疗增加了血清铁结合能力,降低了血清天冬氨酸-胺转移酶(ASAT)和丙氨酸-胺转移酶(ALAT)的水平,以及铁负载肝脏中异常Kupffer细胞的数量。
结论:
建议除了作为抗氧化剂外,Vimang 提取物或其芒果苷成分通过增加其排泄来降低肝铁。补充我们小组早期的体外结果,似乎有可能支持Vimang和Mangiferin在铁过载相关疾病中具有治疗作用的假设。
Mangifera indica L. 茎皮成分 Vimang 和 mangiferin 的驱虫和抗过敏活性。[Pubmed:14669257 ]2003年12月;17(10):1203-8.本研究调查了 Vimang(芒果家族茎皮的水提取物)和芒果苷(Vimang 中存在的主要多酚)口服给实验感染线虫旋毛虫的小鼠的抗过敏和驱虫特性螺旋旋毛虫。
方法和结果:
在整个寄生虫生命周期中用 Vimang 或 Mangiferin(分别为 500 或 50 mg/kg 体重/天)治疗导致肌肉组织中包囊的寄生虫幼虫数量显着下降;然而,这两种治疗方法对肠道中的成年人都无效。在整个寄生虫生命周期中,用Vimang或Mangiferin治疗同样导致特异性抗旋毛虫IgE的血清水平显着下降。最后,每天用 Vimang 或芒果苷口服治疗大鼠 50 天,抑制肥大细胞脱颗粒,如被动皮肤过敏反应试验评估(用高 IgE 滴度的感染小鼠血清致敏,然后用螺旋毛滴虫的胞质部分刺激)。
结论:
由于 IgE 在过敏性疾病的发病机制中起关键作用,这些结果表明 Vimang 和 Mangiferin 可能有助于治疗此类疾病。 新的抗糖尿病化合物,芒果苷及其葡萄糖苷。[Pubmed:9881663]Biol Pharm Bull.1998年12月;21(12):1389-90.
方法和结果:
Mangiferin (MF) 及其葡萄糖苷 (Mangiferin-7-O-beta-glucoside) (MG) 从 Anemarrhena asphodeloides Bunge 根茎中分离出来,在非胰岛素依赖型糖尿病 (NIDDM) 动物模型 KK-Ay 小鼠中测试其抗糖尿病活性。MF和MG降低了口服KK-Ay小鼠的血糖水平。然而,在正常小鼠中,没有观察到对血糖水平的影响,表明MF和MG可用于治疗NIDDM。此外,MF或MG改善了KK-Ay小鼠的高胰岛素血症。
结论:
从这些发现来看,MF 和 MG 似乎可能通过增加胰岛素敏感性来发挥其抗糖尿病活性。
|
芒果苷的方案
| 激酶测定 | 芒果苷可减弱破骨细胞生成、骨吸收和 RANKL 诱导的 NF-κB 和 ERK 激活。[Pubmed:20683903 ]Mangiferin 抑制内质网应激相关的硫氧还蛋白相互作用蛋白/NLRP3 炎症小体激活,调节内皮细胞中的 AMPK。[Pubmed:25499441]新陈代谢。2015年3月;64(3):428-37.
方法和结果:
芒果苷通过减弱 IRE1α 磷酸化和减少 ROS 产生有效抑制 ER 应激相关的氧化应激。在内质网胁迫下,硫氧还蛋白相互作用蛋白(TXNIP)表达增加,其次是NLRP3炎症小体激活和IL-1β分泌增加。芒果苷处理减弱了TXNIP和NLRP3的表达,减少了IL-1β和IL-6的产生,证明了其对TXNIP/NLRP3炎症小体激活的抑制作用。NLRP3 炎症小体激活是线粒体细胞死亡的原因。芒果苷恢复了线粒体膜电位(Δψm)的丧失并抑制了caspase-3活性,从而保护细胞免受高葡萄糖诱导的凋亡。此外,芒果苷抑制了ET-1的分泌,并恢复了细胞暴露于高葡萄糖时NO产生的损失。芒果苷增强了AMPK磷酸化,而AMPK抑制剂化合物C降低了其有益作用,表明了AMPK在其作用中的潜在作用。
结论:
我们的研究揭示了芒果苷对改善内皮稳态的有益作用,并阐明了芒果苷通过的分子途径通过抑制内皮细胞中 ER 应激相关的 TXNIP/NLRP3 炎症小体激活来改善内皮功能障碍。这些发现证明了芒果苷对调节内皮稳态的有益作用,并表明其在糖尿病心血管并发症管理中的潜在应用。
J 细胞生化。2011年1月;112(1):89-97.骨质疏松症等溶骨性骨病有一个共同的病理特征,即破骨细胞骨吸收超过骨合成。破骨细胞的形成和活化受核因子κB配体受体激活剂(RANKL)的调节。RANKL 信号通路的诱导发生在 RANKL 与其同源受体 RANK 的相互作用之后。这种特异性结合驱动下游信号通路的激活;最终诱导破骨细胞的形成和活化。
方法和结果:
在这项研究中,我们发现天然免疫调节剂 Mangiferin 通过减弱 RANKL 诱导的信号传导来抑制破骨细胞形成和骨吸收。芒果苷降低了破骨细胞标记基因的表达,包括组织蛋白酶K、降钙素受体、DC-STAMP和V-ATPase d2。机理研究表明,芒果苷抑制RANKL诱导的NF-κB激活,同时抑制IκB-α降解和p65核易位。此外,芒果苷对RANKL诱导的ERK磷酸化也表现出抑制作用。
结论:
总的来说,我们的数据表明 Mangiferin 具有抗骨吸收特性,表明 Mangiferin 在治疗和预防涉及过度破骨细胞骨吸收的骨疾病方面具有潜在应用。 |
| 细胞研究 | 芒果苷通过 HL-60 白血病细胞的 ATR-Chk1 通路诱导 G2/M 期细胞周期停滞。[Pubmed:25966274]Genet Mol Res. 2015 年 5 月 12 日;14(2):4989-5002.本研究旨在探讨芒果苷对HL-60白血病细胞周期及细胞周期调控基因Wee1、Chk1和CDC25C表达的影响,并进一步探讨芒果苷抗白血病作用的分子机制。
方法和结果:
采用 MTT 法测定芒果苷对 HL-60 白血病细胞增殖的抑制作用。通过流式细胞术评估芒果苷对 HL-60 细胞周期的影响。用不同浓度的芒果苷处理细胞后,通过RT-PCR法测定Wee1、Chk1和CDC25C mRNA的表达水平,采用Western blot法评估cdc25c、cyclin B1和Akt蛋白的表达水平。芒果苷对HL-60细胞生长的抑制是剂量和时间依赖性的。处理24 h后,G2/M期细胞增多,G2/M期阻滞随Wee1、Chk1和CDC25C的mRNA表达增加而出现。Mangiferin 在高浓度下抑制 Chk1 和 cdc25c mRNA 表达,并以剂量依赖性方式诱导 Wee1 mRNA 表达。它显著抑制ATR、Chk1、Wee1、Akt和ERK1/2磷酸化,但增加cdc2和cyclin B1磷酸化。此外,芒果苷降低了 cdc25c、细胞周期蛋白 B1 和 Akt 蛋白水平,同时诱导 Wee1 蛋白表达。它还拮抗钒酸盐对ATR的磷酸化作用,以及EGF对Wee1的磷酸化作用。
结论:
这些结果表明,芒果苷通过 ATR-Chk1 应激反应 DNA 损伤途径抑制细胞周期进程,导致白血病细胞在 G2/M 期的细胞周期停滞。 |
| 动物研究 | 芒果苷治疗抑制果糖喂养的自发性高血压大鼠中酰基辅酶A:二酰基甘油酰基转移酶-2的肝脏表达:与改善脂肪肝有关。[Pubmed: 25123789]芒果苷通过下调糖尿病大鼠骨桥蛋白来减轻肾纤维化。[Pubmed:25380391]Phytother Res. 2015 年 2 月;29(2):295-302.本研究旨在研究芒果苷对糖尿病大鼠肾纤维化、骨桥蛋白产生和肾脏炎症的影响。
方法和结果:
通过单次给药链脲佐菌素 (55 mg/kg, ip) 诱导糖尿病。糖尿病大鼠用芒果苷(15、30和60mg/kg/天,i.g.)治疗9周。将肾脏固定在 10% 福尔马林中,使用 Masson 三色染色进行肾小球纤维化检查。采集肾脏和血液用于测定相关的生化参数。与糖尿病大鼠肾皮质中骨桥蛋白的mRNA和蛋白质表达以及环氧合酶2和NF-кB p65亚基的蛋白质表达减少相比,慢性Mangiferin治疗可预防肾小球纤维化,表现为肾小球染色的肾小球染色阳性区域,IV型胶原蛋白和α平滑肌肌动蛋白的减少。此外,芒果苷降低了糖尿病大鼠血清和肾脏中白细胞介素1β的水平。
结论:
我们的研究结果表明,芒果苷可预防糖尿病大鼠肾小球纤维化,这是通过抑制骨桥蛋白过量产生和可能通过灭活 NF-кB 的炎症来实现的。 毒理学应用药理学。2014年10月15日;280(2):207-15.芒果苷(一种氧杂蒽酮葡萄糖苷)及其相关的传统草药已被证明可以改善脂质代谢的异常。然而,其基本机制在很大程度上仍不清楚。
方法和结果:
本研究探讨了芒果苷在果糖喂养的自发性高血压大鼠(SHR)中具有甾醇调节元件结合蛋白(SREBP)-1突变的抗脂肪变性作用。结果表明,芒果苷(15 mg/kg,每日一次,口服强饲法)联合给药 7 周可显着减少果糖诱导的肝甘油三酯含量增加和 SHR 中油红 O 染色面积。然而,血压、果糖和食物摄入量、白色脂肪组织重量和代谢参数(葡萄糖、胰岛素、甘油三酯、总胆固醇和非酯化脂肪酸的血浆浓度)不受芒果苷治疗的影响。从机制上讲,芒果苷处理抑制了肝脏中 mRNA 和蛋白质水平的酰基辅酶 A:二酰基甘油酰基转移酶 (DGAT)-2 的表达。相比之下,芒果苷处理对肝脏mRNA和/或SREBP-1/1c、碳水化合物反应元件结合蛋白、肝丙酮酸激酶、脂肪酸合酶、乙酰辅酶A羧化酶-1、硬脂酰辅酶A去饱和酶-1、DGAT-1、单酰甘油酰基转移酶-2、微粒体甘油三酯转移蛋白、过氧化物酶体增殖物激活受体-α、肉碱棕榈酰转移酶-1和酰基辅酶A氧化酶的表达没有影响。
结论:
总的来说,我们的结果表明,Mangiferin 治疗通过抑制催化甘油三酯生物合成最后一步的肝脏 DGAT-2 来改善果糖喂养的 SHR 中的脂肪肝。芒果苷的抗脂肪变性作用可能与与从头脂肪酸合成和氧化相关的肝脏信号无关。 |
制备芒果苷的储备溶液
| 1 毫克 | 5 毫克 | 10 毫克 | 20 毫克 | 25 毫克 |
| 1毫米 | 2.368毫升 | 11.8399毫升 | 23.6798毫升 | 47.3597毫升 | 59.1996毫升 |
| 5毫米 | 0.4736毫升 | 2.368毫升 | 4.736毫升 | 9.4719毫升 | 11.8399毫升 |
| 10毫米 | 0.2368毫升 | 1.184毫升 | 2.368毫升 | 4.736毫升 | 5.92毫升 |
| 50毫米 | 0.0474毫升 | 0.2368毫升 | 0.4736毫升 | 0.9472毫升 | 1.184毫升 |
| 100毫米 | 0.0237毫升 | 0.1184毫升 | 0.2368毫升 | 0.4736毫升 | 0.592毫升 |
| *注意:如果 你正在实验过程中,有必要做出 样品的稀释率。以上稀释数据 仅供参考。通常,它可以变得更好 在较低浓度内的溶解度。 |