中文名:牛痘病毒加帽酶
英文名:Vaccinia Capping Enzyme
纯度:医药级
货号:V406454
包装:500u
存储温度:-20°C储存
产品介绍:
产品基本信息
来源:携带牛痘病毒加帽酶基因的E.coli
反应条件:1x Capping Buffer (50 mM Tnis-HC1, pH 8.0; 5 mM KC1; 1 mMMgaly; 1 mM DTT). 37℃孵有
储存缓冲液:20mM Tnis-HC1 pH8.0;100mMNaC1; 1mM DTT; 0.1mMEDIA;0.1%TritonX-100;50% (wv) Glycerol
产品描述
体外转录获得的mRNA未经细胞内一系列修饰,不具备Cap 结构与PolyA 尾,容易降解,易激活免疫反应,不能与核糖体起始蛋白结合,无法启动蛋白翻译,因而在工业化mRNA生产中,需使用牛痘病毒加帽酶对IVT 的mRNA进行加帽修饰,使mRNA的5' 端获得Cap0 结构,进一步使用2'-O- 甲基转移酶将Cap0 转化为Cap1。酶法加帽引入的帽结构与真核生物体内天然帽结构完全一致,从根本上降低外源mRNA 免疫原性的同时,保护其不被降解,并提高翻译效率,增加细胞内蛋白产量。通过酶法加帽最大可获得100%的加帽效率,而通过化学合成帽类似物结构加帽,其加帽效率相对较低,并且帽类似物结构与天然帽结构有差异。
牛痘病毒加帽酶将 7-甲基鸟苷帽结构(m7Gppp,Cap0)加到 RNA 的 5´ 末端。在真核生物中,该结构与 mRNA 的稳定、转运和翻译密切相关。通过酶促反应为 RNA 加帽是一种简单有效的方法,能显著改善用于体外转录、转染和显微注射的RNA的稳定性和翻译能力。这种酶由两个亚基(D1 和 D12)组成 (图 1a),D1 亚基执行 RNA 三磷酸酶和鸟苷转移酶的功能,D12亚基执行鸟嘌呤甲基转移酶的功能,它们对于添加一个完整的 Cap0 结构 m7Gppp5´N 都是必须的(图 1b)。
本制品可用于 T7 RNA Polymerase, GMP Grade(GMP-E121,Novoprotein)反应产生的 RNA 的加帽反应,加帽反应在一小时之内完成,效率接近 100%,并且保证正确的方向。
重组牛痘病毒加帽酶利用大肠杆菌大规模发酵表达,采用药用规格原辅料生产,并严格控制宿主蛋白质残留、核酸残留等,符合 GMP 规范的产品生产与质量管理规程保障生产过程及所有原辅料可追溯。
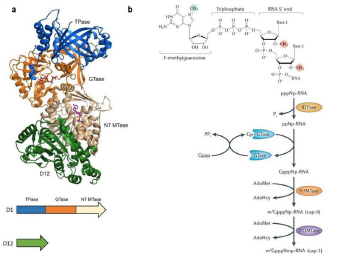
图1. 牛痘病毒加帽的结构和作用机理。a. 牛痘病毒加帽酶和 GTP(红色)、SAH(玫红)的共结晶结构 (PDB 4CKB) 。该酶由 D1 和 D12 两个亚基组成,兼具 RNA 三磷酸酶(蓝色)、鸟苷转移酶(橙色)和鸟嘌呤甲基转移酶(米黄色)的功能。本图引自 Ramanathan, A., Robb, G. B., & Chan, S. H. (2016). mRNA capping: biological functions and applications. Nucleic Acids Res 44(16), 7511–7526. b. mRNA 的帽结构是由一个7-甲基鸟苷通过一个 5′–5′三磷酸酯桥连接到 mRNA 链的 5′核苷上组成。Cap-0 结构由相邻的 RNA 链通过三种酶的依次反应形成。进一步形成 cap-1 结构需要 2-O 甲基转移酶的参与,该修饰可以降低RNA 在体内引起的细胞先天免疫反应。本图引自 Decroly, E., Ferron, F., Lescar, J. et al. (2012). Conventional and unconventional mechanisms for capping viral mRNA. Nat Rev Microbiol 10, 51–65。
质量要求
| 项目 | 标准 | 方法 | | 外观 | 澄明液体 | 目视检查 | | 可见异物 | 符合规定 | 中国药典2020版第四部第一法灯检法(通则0904) | | pH值 | 7.5-8.5 | 中国药典2020版第四部 pH值测定法(通则0631) | | 活性 | 9.8KU/ml-10.2KU/ml | 加帽修饰与效率测定法 | | 纯度 | ≥95% | 中国药典2020版第四部高效液相色谱法(通则 0512) | | 核酸内切酶残留 | 004-DNA的降解不超过10% | 10U酶与004-DNA.37℃孵育3h | | 核酸外切酶残留 | 019 Hind Ⅲ DNA 的降解不超过10% | 10U酶与019 Hind Ⅲ DNA.37℃孵育3h | | RNA酶残留 | 293-RNA的降解不超过10% | 10U酶与293-RNA,37℃孵育1h | | 细菌内毒素含量 | ≤10 EUmg | 中国药典2020版第四部凝胶限度试验法(通则1143) | | 外源性 DNA残留 | ≤100 pg/mg | 荧光定量PCR法 | | 宿主蛋白残留 | ≤50 ppm | 中国药典2020版第四部菌体蛋白残留量测定法(通则3412) | | 支原体检测 | 阴性 | 支原体检测试剂盒 | | 重金属残留 | ≤10ppm | 中国药典2020版第四部重金属检查法(通则0821) |
|
遵循以下规范生产
1. ISO 9001:2015, certified facility。
2. 《GMP 附录-细胞治疗产品》国家药品监督管理局。
3. 《人用基因治疗总论-中国药典 2020》国家药典委。
4. USP Chapter <1043>, Ancillary Materials for Cell, Gene, and Tissue-Engineered Products 用于细胞治疗,基因治疗和组织工程产品中的辅料。
5. USP Chapter <92>, Growth Factors and Cytokines Used in Cell Therapy Manufacturing 细胞治疗产品生产过程中细胞因子和生长因子。
6. Ph. Eur. General Chapter 5.2.12, Raw Materials of Biological Origin for the Production of Cell-based and Gene Therapy Medicinal Products 用于生产细胞或基因治疗药物的生物来源原料。
产品用途
体内或体外翻译前 mRNA 的加帽和 mRNA 的 5’末端标记。
应用实例

完整mRNA在细胞内表达GFP蛋白,加帽酶与帽类似物对比
注意事项
1. 用于加帽反应的 RNA 在使用之前应进行纯化并溶解于无核酸酶水。溶液中不能含有 EDTA 和盐。
2. 在配置反应体系时,可以加入 0.5 µl 的 RNase 抑制剂(GMP-E125,Novoprotein),同时去掉等体积的 RNase-free Water。
3. 在与加帽酶反应之前加热 RNA 可以消除转录产物 5´的二级结构。如果转录产物的 5´端结构复杂,可以把加热时间延长至10 分钟。
4. SAM 在 pH 7–8, 37°C 条件下不稳定,需要在反应开始之前新鲜配置。可以事先计算好 SAM 的用量,在反应开始前把分装的 32 mM 的储备液稀释成 2 mM 的工作液。为避免 SAM 降解,该工作液需要保存于冰上。
5. 如果已知转录产物的 5´端结构复杂,反应时间可延长至 60 分钟以提高加帽效率。
6. 在标记 5´端时,GTP 储备液应稀释到 mRNA 浓度的 1–3 倍。
查看阿拉丁官网此产品相关对应页面:https://www.aladdin-e.com/zh_cn/V406454.html