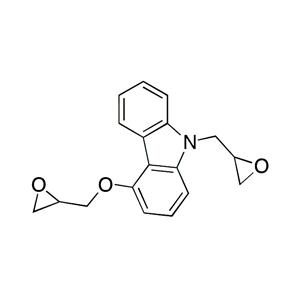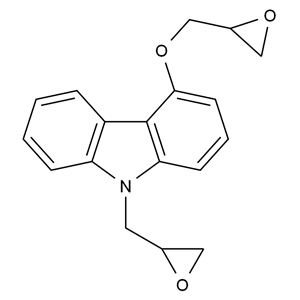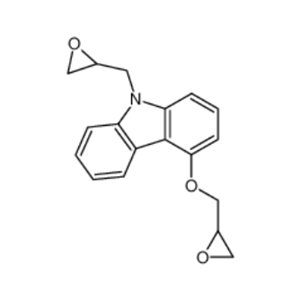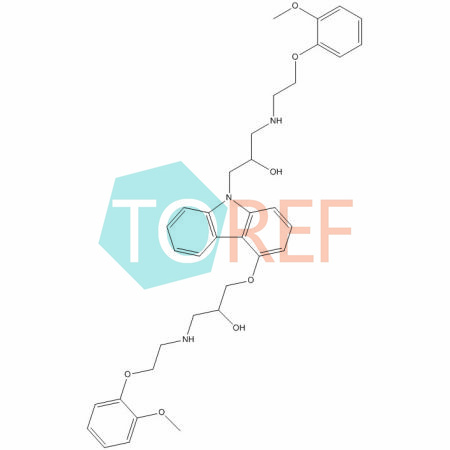

化合物简介
基本信息
化学式:C24H26N2O4
分子量:406.474
CAS号:72956-09-3
理化性质
密度:1.25g/cm3
熔点:113-117ºC
沸点:655.2ºC
闪点:350.1ºC
外观:无色结晶性粉末
溶解性:不溶于水
分子结构数据
摩尔折射率:119.59
摩尔体积(cm3/mol):325.1
等张比容(90.2K):881.0
表面张力(dyne/cm):53.9
极化率(10-24cm3):47.41
计算化学数据
疏水参数计算参考值(XlogP):无
氢键供体数量:3
氢键受体数量:5
可旋转化学键数量:10
互变异构体数量:0
拓扑分子极性表面积:75.7
重原子数量:30
表面电荷:0
复杂度:508
同位素原子数量:0
确定原子立构中心数量:0
不确定原子立构中心数量:1
确定化学键立构中心数量:0
不确定化学键立构中心数量:0
共价键单元数量:1
药品简介
适应症
适用于有症状的心力衰竭,也用于原发性高血压。
用法用量
1、治疗心力衰竭:口服:开始3.125mg/次,2次/日,若耐受良好,2周后增加到6.25mg/次,2次/日,逐渐增加;体重小于85公斤,最大剂量25mg/次,2次/日;体重大于85公斤,最大剂量50mg/次,2次/日。
2、用于高血压:口服:开始12.5mg/次,1次/日,2天后可加至25mg/次,1次/日;必要时可在2周后加至最大量50mg/日,分1~2次服用。
不良反应
1、精神神经系:统偶见轻度头晕、头痛、乏力,特别是在治疗早期;罕见抑郁、睡眠紊乱、感觉异常。
2、心血管系统:治疗早其偶见心动过缓、直立性低血压,很少引起晕厥;少见外周循环障碍(四肢发凉)、水肿和心绞痛;可使原有间歇性跛行或有雷诺现象的患者症状加重;个别患者可出现房室传导阻滞和心力衰竭加重。
3、呼吸系统:偶可诱导有哮喘或呼吸困难倾向的患者发病,罕见鼻塞。
4.消化系统:少见便秘和呕吐;偶见胃肠不适(如腹痛、腹泻、恶心等)和血清氨基转移酶升高。
5、泌尿生殖系统:罕见排尿障碍、性功能减退;有心力衰竭和弥散性血管病变和(或)肾功能不全的患者可能会进一步加重肾功能损害,个别病例可出现肾衰竭。
6、皮肤:少见变态反应性皮疹,个别患者可出现荨麻疹、瘙痒、扁平苔藓样皮肤反应。可能发生银屑样皮肤损害或使原有的病情加重。
7、眼:可引起眼干;罕见视觉障碍及眼部刺激感。
8、血液:偶见血小板减少,白细胞减少等。
9、代谢/内分泌系统:由于本药具有β肾上腺素受体阻滞药的特性,可使隐性糖尿病患者出现临床症状,或使原有糖尿病的患者病情加重,并抑制反向葡萄糖调节机制。心力衰竭患者偶见体重增加及高胆固醇血症。
10、其他:偶见四肢疼痛,罕见口干。
注意事项
NYHAⅣ级的失代偿心力衰竭、哮喘、伴有支气管痉挛的COPD、肝肾功能异常、Ⅱ~Ⅲ度房室传导阻滞、心率小于50次/分、病窦综合征等患者禁用;一般需长期应用,治疗不能骤停,需逐渐减量。
用药禁忌
慢性梗阻性肺疾患者、糖尿病患者、肝功能低下者、妊娠及哺乳期妇女禁用。
说明:上述内容仅作为介绍,药物使用必须经正规医院在医生指导下进行。
药典信息
基本信息
本品为(±)-1-(9H-4-咔唑基氧基)-3-[2-(2-甲氧基苯氧基)乙氨基]-2-丙醇,按于燥品计算,含C24H26N2O4不得少于 98.5%。
性状
本品为白色或类白色结晶性粉末,无臭。
本品在三氯甲烷中溶解,在甲醇或乙酸乙酯中略溶,在水中不溶,在冰醋酸中易溶。
熔点
本品的熔点(通则0612)为114~118℃。
鉴别
1、取本品适量,加0.06mol/L醋酸溶液溶解并稀释制成每1mL中约含20µg的溶液,照紫外-可见分光光度法(通则0401)测定,在285nm、319nm与331nm的波长处有最大吸收,在331nm与285nm波长处的吸光度比值应为0.40~0.44。
2、本品的红外光吸收图谱应与对照的图谱(光谱集714图)一致。
检查
醋酸溶液的澄清度与颜色
取本品0.10g,加6mol/L醋酸溶液10mL溶解后,溶液应澄清无色,如显色,与黄色2号标准比色液(通则0901第一法)比较,不得更深。
有关物质
照高效液相色谱法(通则0512)测定。
供试品溶液:取本品,加流动相溶解并稀释制成每1mL中约含0.5mg的溶液。
对照溶液:精密量取供试品溶液适量,用流动相定量稀释制成每1mL中约含1µg的溶液。
系统适用性溶液:取卡维地洛约12.5mg,置锥形瓶中,加5mol/L盐酸溶液5mL,于95℃水浴中加热3小时,放冷,加5mol/L氢氧化钠溶液5mL,流动相15mL,超声10分钟,摇匀,滤过。
色谱条件:用十八烷基硅烷键合硅胶为填充剂,以0.02mol/L磷酸二氢钾溶液(用磷酸调节pH值至3.5)-乙腈(65:35)为流动相,检测波长为241nm,进样体积10µL。
系统适用性要求:系统适用性溶液色谱图中,理论板数按卡维地洛峰计算不低于2000,卡维地洛峰与其后的最大降解物峰的分离度应大于6.5。
测定法:精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的3.5倍。
限度:供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液的主峰面积(0.2%),各杂质峰面积的和不得大于对照溶液主峰面积的2.5倍(0.5%)。
残留溶剂
照残留溶剂测定法(通则0861第二法)测定。
供试品溶液:取本品约0.2g,精密称定,置顶空瓶中,精密加入20%冰醋酸溶液2mL使溶解,密封。
贮备液(1):分别取甲醇、丙酮、四氢呋喃与1,4-二氧六环,精密称定,用20%冰醋酸溶液定量稀释制成每1mL中各约含3mg、5mg、0.72mg与0.38mg的溶液。
贮备液(2):分别取1,2-二氯乙烷、苯、三氯甲烷、甲苯、乙醚与乙酸乙酯,精密称定,用乙腈定量稀释制成每 1mL中各约含50µg、20µg、0.6mg、8.9mg、50mg与50mg的溶液。
对照品溶液:精密量取贮备液(1)10mL和贮备液(2)1mL,置100mL量瓶中,用20%冰醋酸溶液稀释至刻度,摇匀,精密量取2mL,置顶空瓶中,密封。
色谱条件:以聚乙二醇(或极性相近)为固定液,起始温度为40℃,维持12分钟,以每分钟40°C的速率升温至180°C,维持5分钟,进样口温度为200℃,检测器温度为230°C,顶空瓶平衡温度为90°C,平衡时间为30分钟。
系统适用性要求:对照品溶液色谱图中,各成分峰间的分离度均应符合要求。
测定法:取供试品溶液与对照品溶液,分别顶空进样,记录色谱图。
限度:按外标法以峰面积计算,甲醇、丙酮、四氢呋喃、1,4-二氧六环、1,2-二氯乙烷、苯、三氯甲烷、甲苯、乙醚与乙酸乙酯的残留盐均应符合规定。
干燥失重
取本品,以五氧化二磷为干燥剂,减压干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣
取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属
取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
含量测定
取本品约0.3g,精密称定,加冰醋酸30mL溶解后,照电位滴定法(通则0701),用高氯酸滴定液(0.1mol/L)滴定,并将滴定的结果用空白试验校正。每1mL高氯酸滴定液(0.1mol/L)相当于40.65mg的C24H26N2O4。
类别
血管舒张药,β肾上腺素受体拮抗药。
贮藏
遮光,密封保存。
制剂
1、卡维地洛片。
2、卡维地洛胶囊。
安全信息
安全术语
S26:In case of contact with eyes, rinse immediately with plenty of water and seek medical advice.
眼睛接触后,立即用大量水冲洗并征求医生意见。
S36:Wear suitable protective clothing.
穿戴适当的防护服。
S61:Avoid release to the environment. Refer to special instructions/Safety data sheets.
避免释放到环境中,参考特别指示/安全收据说明书。
风险术语
R20/21/22:Harmful by inhalation, in contact with skin and if swallowed.
吸入、与皮肤接触和吞食是有害的。
R36/37/38:Irritating to eyes, respiratory system and skin.
刺激眼睛、呼吸系统和皮肤。
R51/53:Toxic to aquatic organisms, may cause long-term adverse effects in the aquatic environment.
对水生生物有毒,可能在水生环境中造成长期不利影响。
杂质、分离纯化业务介绍
桐晖药业公司成立20多年,提供原料/参比制剂的同时,拥有一个高水平的合成定制和分离纯化团队、提供高难度定制合成和分离纯化服务,建立了完善的杂质分离技术平台,可以快速的帮您得到所需的杂质纯品,特别擅长高难度的微量杂质标样制备,比如(万分之一等极低含量,溶解度差,稳定性差,分离度差,保留弱,发酵类药物杂质),可以提供合理的监测和控制方法,分离和纯化其过程中产生的微量未知杂质。帮您轻松解决杂质研究的难题。严格把控质量关,配套资质齐全,所有杂质均可提供COA。现除自有高端定制品牌TOREF外,也代理了包括中检所、BP、USP、EP、TLC 、LGC、TRC等品牌的销售,品类齐全,价格有竞争力。
专业分离纯化制备服务(高难度项目解决方案):
1、含量低
2、分离度差
3、稳定性差
4、溶解性差
5、保留弱
6、无紫外吸收
我们的优势:
1、专业团队,完善的平台,分离纯化技术成熟,经验丰富
2、药物研发和注册过程中所需的相关杂质的定制合成
3、药物研究多成分粗品,提供分离纯化和结构解析
4、擅长分离低含量,分离度差,无紫外吸收的成分
5、多种分离技术组合,周期短,成功率高,价格优
6、毫克级,克级,公斤级纯化、技术转让
7、提供完整的资料COA等相关检测数据满足申报要求
8、快速高效交付,品质高,售后服务质量好
成功案例对卡磺钠注射液多个杂质分离纯化,确定结构,帮助客户解决生产难题
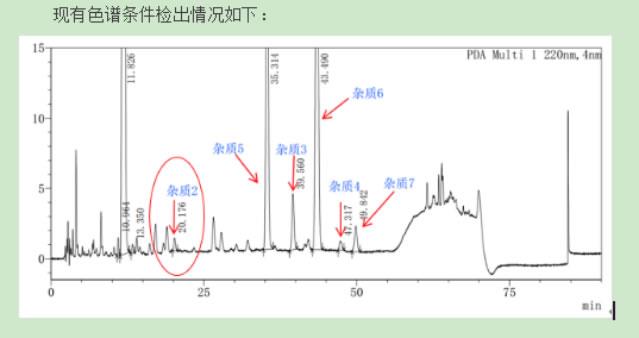
桐晖药业,基于核磁、色谱及其联用技术,在分离纯化、结构确证细分领域潜心钻研十余载,现为您提供技术专属性强、纯度高、重现性好、结构确证无误的专业解决方案,助力药品研发。