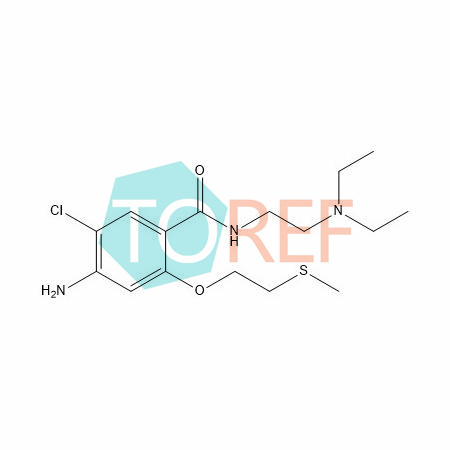
福多司坦杂质4, 1023971-10-9, 杂质、对照品 新品
Fudosteine impurity 4
1023971-10-9
1023971-10-9
询价
10mg
起订
50mg
起订
100mg
起订
广东 更新日期:2026-05-21
产品详情:
- 中文名称:
- 福多司坦杂质4
- 英文名称:
- Fudosteine impurity 4
- CAS号:
- 1023971-10-9
- 品牌:
- TOREF
- 产地:
- 国内
- 保存条件:
- 2-8℃
- 纯度规格:
- 【95.13%】
- 产品类别:
- 杂质标准品
- 货号:
- REF-F48005
- 用途:
- 未定义
- 分子式:
- C6H13NO3S
- 分子量:
- 179.2
公司简介
广州市桐晖药业有限公司成立于1999年,国家GSP认证,主要经营中西药制剂及化学原料、医药化工原料和医药中间体等产品。桐晖拥有雄厚的经济实力,是一家集市场营销、学术推广、进出口、新产品研发、合作生产为一体的现代企业。
桐晖药业是行业中的进口药专家,积极快速引进国外战略性新产品,尤其是国内紧缺或空白的新产品,已与全球各大药企建立深入的合作关系,致力于将国际上最新、最好的产品引入中国市场,打造中国医药行业排头兵。
桐晖药业是世界新产品进出口的专业平台,在国际医药界享有很高的名望和美誉。它拥有一支专业的营销部、市场部和进口注册团队,具有专业的产品打造力,高度准确的终端占有力,打造同类产品中的优秀品
| 成立日期 | (27年) |
| 注册资本 | 1000万 |
| 员工人数 | 100-500人 |
| 年营业额 | ¥ 1亿以上 |
| 经营模式 | 贸易,定制,服务 |
| 主营行业 | 医药中间体,原料药 |
福多司坦杂质4相关厂家报价
-

- D-福多司坦
- 深圳菲斯生物科技有限公司 VIP
- 2026-06-11
- 询价
-
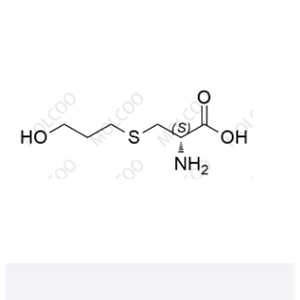
- 福多司坦右旋异构体
- 深圳摩科生化科技有限公司 VIP
- 2026-06-10
- 询价
-

- 福多司坦杂质21
- 深圳振强生物技术有限公司 VIP
- 2026-06-05
- 询价
-
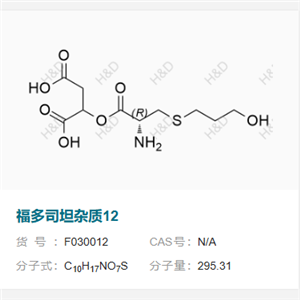
- 福多司坦杂质12
- 深圳市恒丰万达医药科技有限公司 VIP
- 2026-05-22
- 询价
-
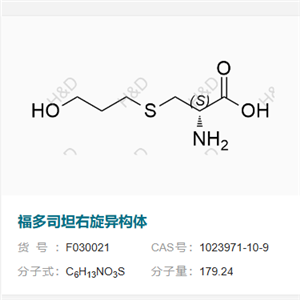
- 福多司坦右旋异构体 1023971-10-9
- 深圳市恒丰万达医药科技有限公司 VIP
- 2026-05-22
- 询价