
2YR企业会员
发布人:普健生物(武汉)科技有限公司
发布日期:2026/2/25 10:02:50
巨噬细胞(macrophage)是机体内广泛分布的重要免疫细胞。传统观点将其视为单一的“清道夫”,负责吞噬病原体与清除细胞碎片。然而,随着研究不断深入,发现巨噬细胞的起源、定植、活化状态、功能与表型均高度可塑并具有异质性。理解其多样性,对于揭示免疫机制、疾病发生以及开发干预策略具有重要意义。
在早期免疫学研究中,人们普遍认为巨噬细胞来源于骨髓造血干细胞,经由血液中的单核细胞进入组织,并逐渐分化成熟。然而,随着命运追踪(fate-mapping)技术的发展,这一传统观点被重新审视。研究者陆续发现,许多组织中的巨噬细胞在成年后几乎不依赖循环单核细胞补充,而是能够通过自身增殖长期维持。这一现象引发了对巨噬细胞发育来源的重新思考。
随着来自胚胎发育阶段的证据逐渐清晰:在卵黄囊和胎肝时期就已经出现了早期巨噬细胞前体,它们会在胎儿发育阶段迁入不同组织并完成定植,形成了多个主要的组织常驻巨噬细胞群体。例如,中枢神经系统中的小胶质细胞、肝脏的Kupffer细胞以及皮肤的朗格汉斯细胞,都是在胚胎期就已经进入组织,并在成年后通过自我增殖维持。
因此,现代免疫学对巨噬细胞的发育来源形成了更精确的认识:巨噬细胞的来源并非单一路径,而是由胚胎来源与成年骨髓来源共同构成。胚胎来源巨噬细胞主要承担长期的组织稳态功能,而成年期由单核细胞迁入组织形成的巨噬细胞,则更多参与炎症和组织修复等动态过程。
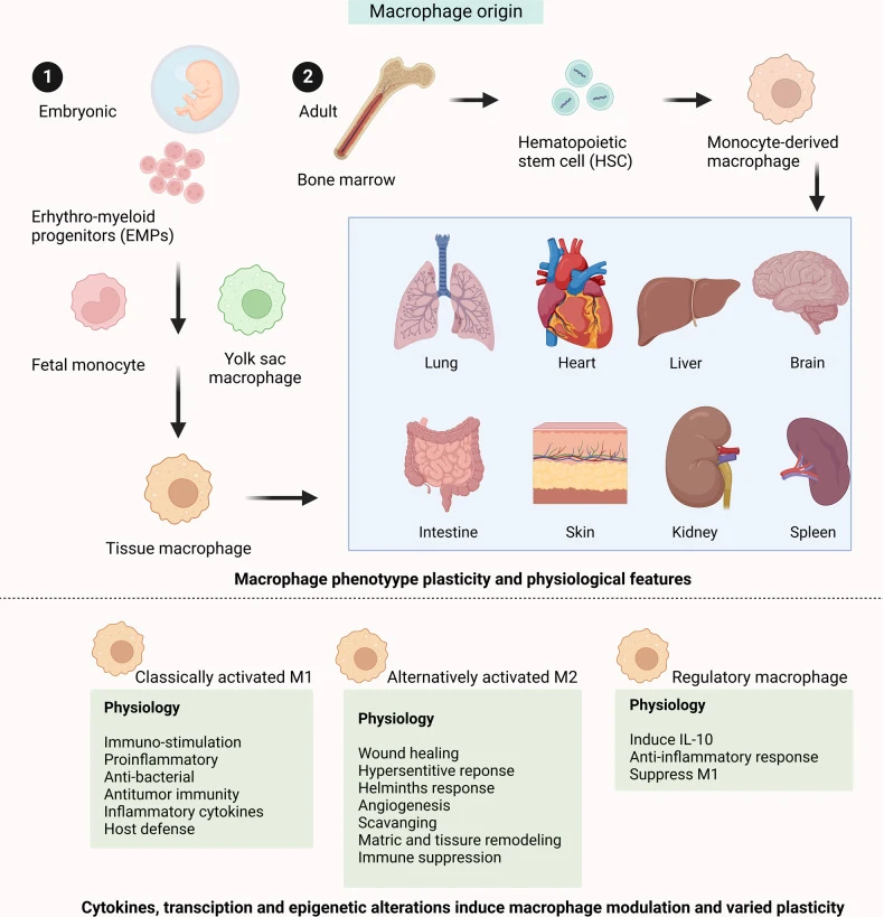
图1. 巨噬细胞的起源与发育(DOI: 10.1038/s41392-023-01452-1)
巨噬细胞一旦定植到特定组织,其表型和功能会在局部微环境的影响下发生深度改变,从而呈现高度专化的状态。这些细胞被称为组织常驻巨噬细胞。它们的多样性并非来自不同的发育路径,而是在独特组织环境的信号塑造下逐渐形成。例如,小胶质细胞在中枢神经系统中响应神经元和胶质细胞提供的信号,形成独特的免疫稳态功能;Kupffer细胞在肝脏中长期暴露于肠源代谢物,使其具备强大的耐受性与清除能力;肺泡巨噬细胞则适应富含表面活性物质的肺泡环境,形成高效的吞噬功能。每种组织常驻巨噬细胞都深刻体现了“组织决定命运”的原则。
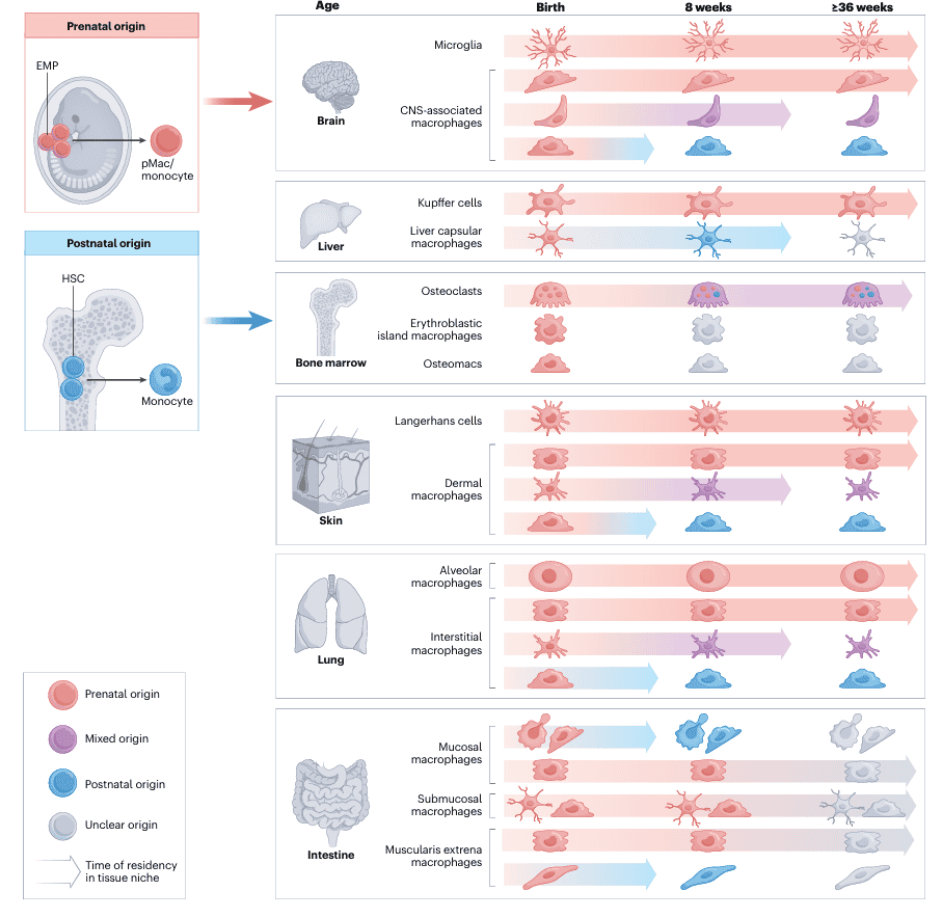
图2. 组织常驻巨噬细胞类型(DOI: 10.1038/s41577-023-00848-y)
巨噬细胞的分类仍然是一个非常有争议的话题,不同的因素会导致不同的表型和巨噬细胞活化状态,包括信号分子、生长因子、转录因子、表观遗传和转录后机制和变化,以及小生境信号,如细胞因子、细胞间接触物和代谢物。一般来说,巨噬细胞可以根据其功能和活化作用分为两种亚型:经典活化的M1巨噬细胞和替代活化的M2巨噬细胞。
M1表型体现为一类以促炎与免疫效应为主的巨噬细胞群体。实验与组织学上常见的M1相关特征包括高表达或强功能性显示的促炎介质与分子,如TNF-α、IL-1β、IL-12,以及与杀菌/溶菌相关的分子产物(例如ROS、NO)。在流式或转录组层面,M1相关标志通常伴随较高的MHC II、共刺激分子(如CD80/CD86)表达,这与其较强的抗原呈递和激活适应性免疫的能力相一致。临床或病理情境中,M1巨噬细胞常在急性感染、某些炎症性病变以及某些肿瘤的免疫活性区域中被观察到,其主要功能可概括为清除病原、限制病灶扩散并启动或维持强度较高的免疫应答。
M2表型代表一类以免疫抑制、修复与组织重塑为主的巨噬细胞群体。在分子与功能层面,M2相关巨噬细胞倾向于分泌抗炎或修复性因子(如IL-10、TGF-β等),并在清除凋亡细胞(efferocytosis)、促进间质重建与血管生成等过程中发挥重要作用。常见的表面或代谢相关标志包括CD206(甘露糖受体)、某些精氨酸代谢相关酶(如Arg1)等。M2-样表型在组织修复期、寄生虫感染后期以及许多慢性病理或肿瘤微环境中较为常见,其生物学作用更偏向于限制过度炎症、恢复组织稳态与支持修复过程。
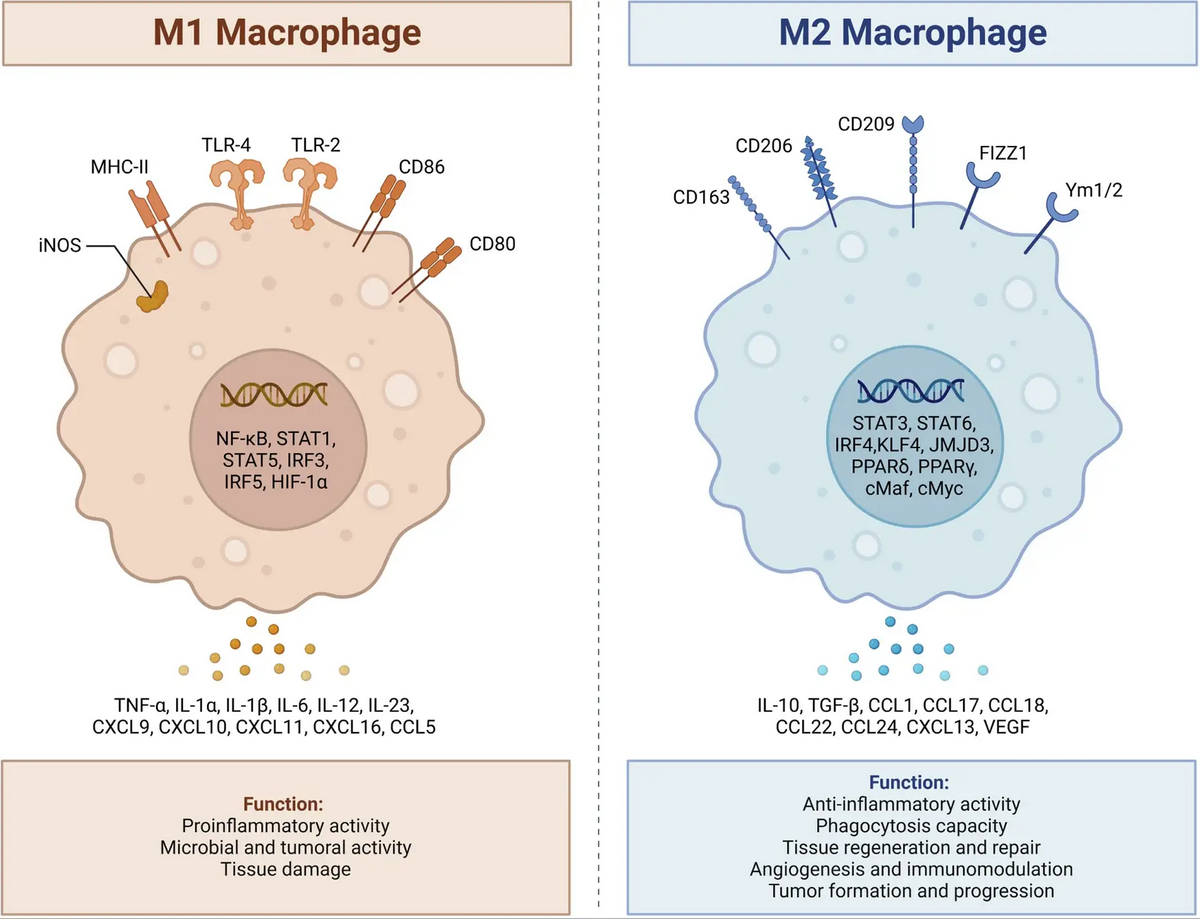
图3. 巨噬细胞的两种表型(DOI:10.1038/s41419-024-06888-z)
近年来,单细胞组学、空间转录组和命运追踪技术不断推动我们认识到:在特定疾病背景或组织微环境中,常驻与非定居民群之外,还会出现一系列高度特化的巨噬细胞亚型。这些亚群通常在某些病理状态中显著积累,具有独特的功能和标志物,对疾病进程具有重要影响。
在肿瘤组织中,肿瘤相关巨噬细胞(TAMs)是数量最多、功能最复杂的免疫成分之一。长期暴露于肿瘤分泌的细胞因子、乳酸积累和缺氧环境,使它们呈现出高度适应性的免疫抑制与组织重塑特征。TAMs能产生大量具有免疫抑制功能的因子,削弱效应T细胞对肿瘤的识别能力;同时,它们分泌的MMPs和VEGF可促进肿瘤血管形成与基质重塑,为肿瘤生长和转移提供更有利的生存条件。值得注意的是,TAMs并非单一群体,而是包含多个功能取向不同的子集,如富含抗原呈递基因的区域性TAM、邻近血管的血管生成型TAM,以及长期处于代谢压力下的炎性TAM。它们共同构成了肿瘤生态的重要组成部分,也是近年肿瘤免疫治疗的重要切入点。
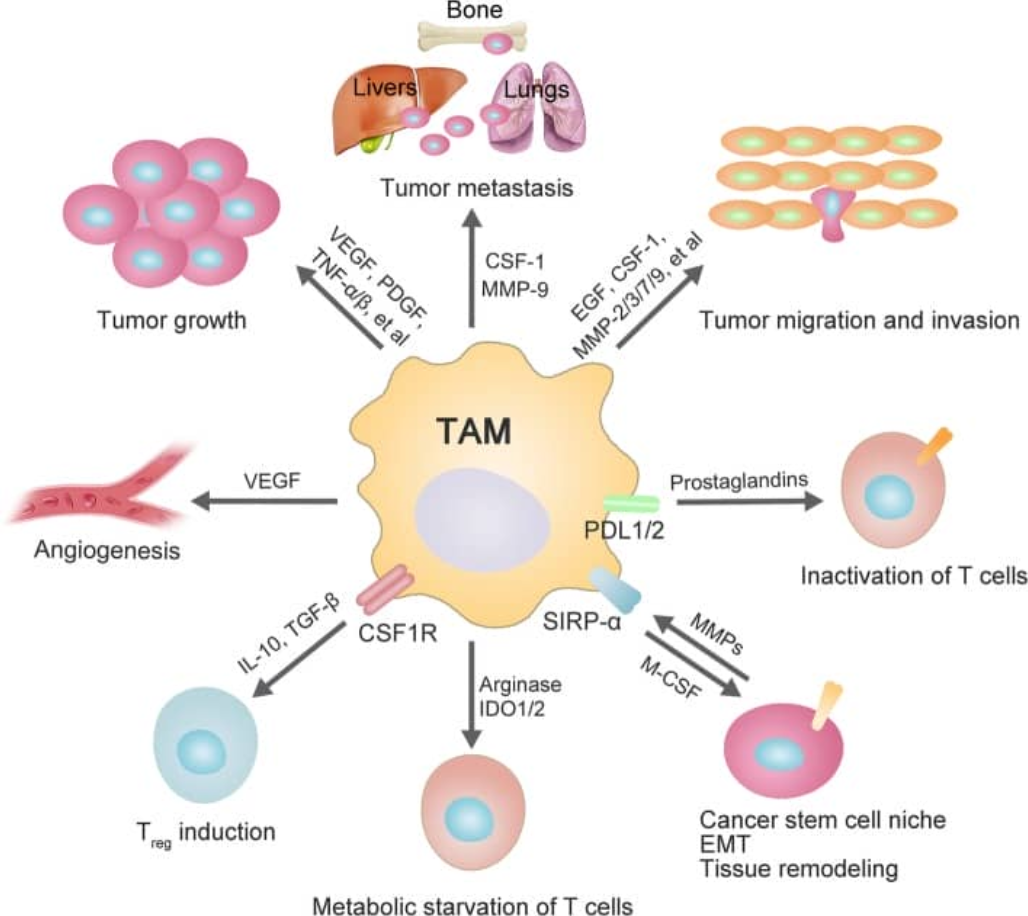
图4. TAMs在肿瘤发生过程中的作用(DOI:10.1186/s12929-019-0568-z)
与肿瘤环境中的TAMs不同,CD169+巨噬细胞主要分布在淋巴结皮质下窦、脾脏边缘区等承担抗原引流任务的解剖结构,是机体识别血液或淋巴系统中入侵病原的重要哨兵。这类巨噬细胞能够高效捕获通过体液循环到达免疫器官的抗原,并与树突状细胞协作,参与初始CD8+T细胞的激活,因此在抗病毒免疫和疫苗反应形成中占据关键地位。近年来针对急性病毒感染和疫苗应答的研究表明,CD169+巨噬细胞对早期免疫反应的影响远超传统认识,其状态甚至可能决定免疫应答的速度与质量,是连接先天免疫与适应性免疫的重要枢纽。
相比前两类亚群,TCR+巨噬细胞是更“新颖”的发现。它们在多个慢性疾病模型、肿瘤组织以及长期炎症环境中被反复观察到。其最令人关注的特征,是表达传统上属于T细胞的TCR/CD3复合体。这一现象提示这些巨噬细胞可能具备特殊的信号识别与调控能力,能够通过非典型通路与周围细胞交流。虽然其具体功能仍在研究中,但现有证据显示,它们可能参与局部免疫平衡的维持、炎症调控以及组织微环境的重塑。随着空间组学和配体互作分析工具的不断发展,TCR+巨噬细胞很可能成为未来研究中揭示新型免疫调节机制的重要线索。
巨噬细胞远不只是简单的“清道夫”,它们是机体免疫系统中高度可塑的多功能细胞。从胚胎期就定植于组织的常驻巨噬细胞,到成年期由单核细胞补充的炎症相关巨噬细胞,再到特定疾病环境下出现的TAMs、CD169+巨噬细胞或TCR+巨噬细胞,每一类巨噬细胞都在特定微环境中承担独特功能,调节免疫反应、组织稳态与修复过程。
[1] Mass E, Nimmerjahn F, Kierdorf K, Schlitzer A. Tissue-specific macrophages: how they develop and choreograph tissue biology. Nat Rev Immunol. 2023 Sep;23(9):563-579.
[2] Chen S, Saeed AFUH, Liu Q, Jiang Q, Xu H, Xiao GG, Rao L, Duo Y. Macrophages in immunoregulation and therapeutics. Signal Transduct Target Ther. 2023 May 22;8(1):207.
[3] Li D, Zhang T, Guo Y, Bi C, Liu M, Wang G. Biological impact and therapeutic implication of tumor-associated macrophages in hepatocellular carcinoma. Cell Death Dis. 2024 Jul 12;15(7):498.
[4] Chen Y, Song Y, Du W, Gong L, Chang H, Zou Z. Tumor-associated macrophages: an accomplice in solid tumor progression. J Biomed Sci. 2019 Oct 20;26(1):78.
[5] Jin R, Neufeld L, McGaha TL. Linking macrophage metabolism to function in the tumor microenvironment. Nat Cancer. 2025 Feb;6(2):239-252.
abinScience提供一系列巨噬细胞研究相关的抗体和重组蛋白,广泛应用于ELISA、Western Blot、免疫组化、FCM等实验,帮助科研人员深入研究巨噬细胞的极化、激活、蛋白质表达、功能、表型等。更多巨噬细胞相关产品请访问abinScience官网:www.abinscience.cn或扫码咨询。
相关新闻资讯