
2YR企业会员
发布人:普健生物(武汉)科技有限公司
发布日期:2026/1/12 10:41:51
在流式细胞术实验中,非特异性染色引发的高背景荧光,是制约数据精准性的高频痛点。它不仅会模糊阳性与阴性群体的界限,降低信噪比,更可能导致实验结论误判,使科研人员在反复调试中耗费大量时间与精力。
这类看似复杂的高背景问题,往往并非由单一因素导致,而是实验场景、样本特性与操作细节共同作用的结果。想要高效解决这一问题,关键在于厘清实验核心逻辑,识别易被忽视的隐性干扰因素,并结合针对性的定位方法与实操策略,才能建立清晰、可复现的优化路径。
在非特异性染色导致的高背景问题中,许多干扰源自看似合理的“常规操作”。精准识别并解析这些误区,是高背景排查的首要环节,有助于避免盲目调参,快速锁定问题本质。
![]()
Fc阻断剂的核心作用,是抑制抗体Fc段与细胞表面Fc受体之间的特异性结合。但这一策略并非对所有非特异性染色均有效,尤其在髓系细胞样本中,常可观察到Fc阻断后背景信号仍然显著存在的情况。
花青素类染料(如Cy5及其串联染料)在单核细胞、巨噬细胞和树突状细胞中,常表现出Fc非依赖性的背景信号升高。该现象在Fc受体充分阻断后仍可观察到,提示其并非典型的Fc介导结合过程。
目前,该现象的具体分子机制尚未完全阐明。既往研究中有推测认为,花青素荧光团可能与髓系细胞表面高度表达的Fcγ受体(如CD64)或其他膜相关结构发生Fc非依赖性的相互作用。然而,更广泛的实验观察表明,这类背景信号具有显著的染料依赖性:在相同抗体、相同细胞条件下,更换为非花青素类荧光素(如APC、Alexa Fluor 647)后,背景可明显降低。
这一结果提示,该现象更可能反映的是花青素类荧光团自身理化特性(如较强疏水性)与髓系细胞膜结构之间的非特异性相互作用,而非由单一受体分子主导。
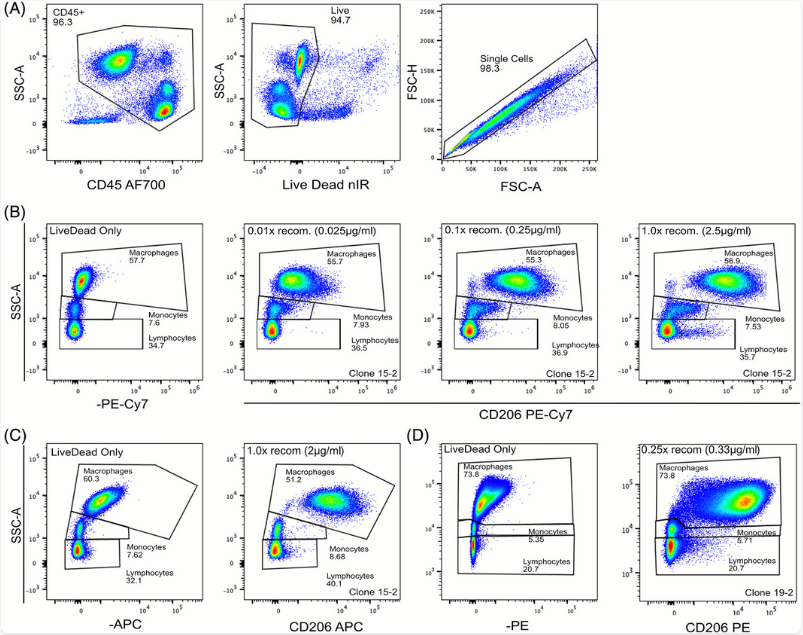
图1. Fc受体阻断后,PE-Cy7标记的CD206在淋巴细胞与单核细胞中仍出现明显非特异性染色(图B);更换为APC或PE标记后,背景显著降低(图C)。(图片来源:DOI: 10.1002/cyto.a.24273)
针对髓系细胞样本,优先避免使用花青素类染料(如Cy5、PE-Cy5、PE-Cy7);
若实验设计必须使用,可在染色缓冲液中加入1–2 %BSA或血清蛋白,以竞争性方式减少花青素荧光团与细胞膜的非特异性相互作用;
在部分体系中,可在充分验证前提下加入低浓度非离子型表面活性剂以降低疏水性吸附,但需谨慎评估其对膜完整性和抗体结合的影响;
也可尝试使用Cy系列染料专用的封闭剂:True-Stain Monocyte Blocker(BioLegend)及磷硫化寡脱氧核苷酸Oligo-Block(Sigma-Aldrich)。
注:Fc阻断仍属必要步骤,但需明确其作用边界,避免过度依赖。
![]()
同型对照的核心价值在于评估抗体Fc段介导的非特异性结合及部分胞内交叉反应。然而,在多色实验中,过度依赖同型对照不仅增加操作复杂度,还可能因关键参数不匹配而误导结果判断。
关键问题
不同厂家、不同批次抗体的荧光素–蛋白(F:P)比例差异显著。例如,A公司CD4-PE抗体的F:P为2:1,而B公司同型对照抗体的F:P为4:1,即便使用相同抗体量,同型对照的荧光强度也可能显著偏高,从而被误判为“目标抗体背景过高”。
优化方案
在多色实验中,优先使用FMO对照(荧光减一对照)评估实际实验条件下的背景分布;
若必须使用同型对照,需严格遵循“同一厂家、同一荧光素、同一用量”的原则,确保对照具有可比性。
![]()
误区解析
电压调节的核心目标,是在保证动态范围的前提下最大化群体分辨率,而非单纯压低背景。电压设置过低,往往会压缩低表达抗原的信号分布,使阳性群体与背景界限反而更加模糊。
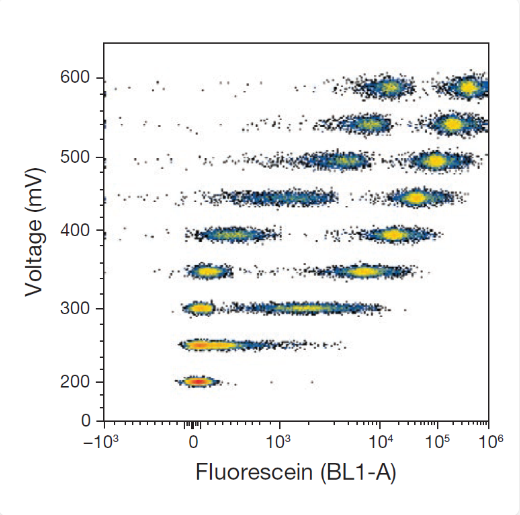
图2. 电压对荧光素分辨率的影响
以空白对照与阳性对照为双重参考,确保自发荧光峰位于检测线性范围内;
调整电压,使阳性峰与背景峰之间形成清晰分离,兼顾信噪比与动态范围。
在排除常见操作误区后,若背景荧光仍未显著改善,需进入进阶排查阶段,重点关注在特定样本或实验条件下高频出现的隐性成因。
![]()
在PMA活化PBMC或细胞因子刺激实验中,常可观察到多个通道背景同步升高。这一现象通常并非抗体或染料质量问题,而是细胞代谢状态变化的结果。
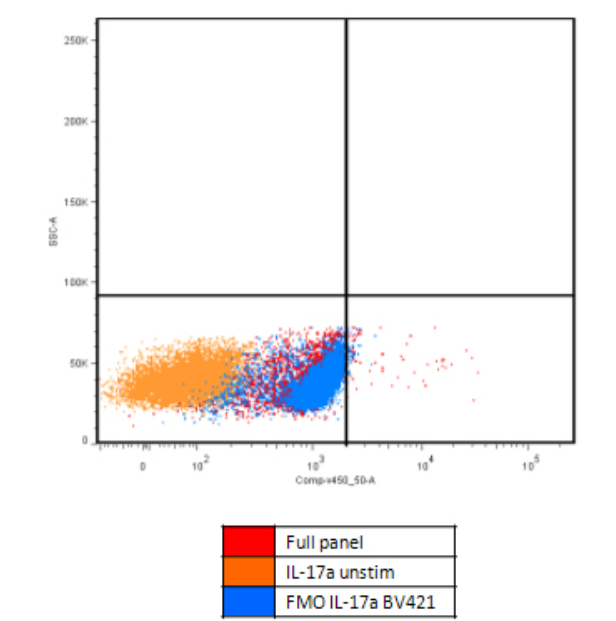
图3. PMA活化的PBMC中检测IL-17A,从FMO对照中明显看出BV421通道基线的上升(图片来源:流式中文网)
细胞代谢活化后,胞内NADH、黄素辅酶等内源性荧光分子水平升高,自发荧光增强;同时细胞膜通透性增加,放大荧光渗漏效应,导致整体基线抬高。
活化后样本增加洗涤步骤,降低胞内代谢产物残留;
下调抗体使用浓度;
优先选择长波长荧光素,减少与内源性荧光的光谱重叠。
![]()
胞内染色背景升高,常源于固定与破膜条件不匹配,而非抗体特异性不足。
固定剂浓度或时间失衡,导致蛋白过度交联或固定不足;
有机溶剂固定引发表位构象破坏;
固定后洗涤不充分,残留醛基与抗体发生非特异性反应。
固定剂与破膜剂需根据抗原类型匹配选择,细胞因子检测与转录因子检测用到的固定剂破膜剂是不同的;
严格控制固定时间与温度,固定时间应控制在15-30 min,温度保持在室温(20-25°C),以避免过度交联。对于转录因子实验,温度可适当降低至4°C,减少抗原降解;
破膜后可以增加蛋白封闭步骤,减少胞内非特异性结合位点。
——从“现象判断”回到“机制定位”的实操闭环
在完成前述误区排查与隐性成因分析后,高背景问题的处理应回归到一个核心原则:先判断背景信号的来源属性,再选择对应的干预手段,而非直接进行经验性调整。
基于非特异性染色最常见的发生机制,可将高背景问题拆解为以下四类来源,并据此构建一条由浅入深、可快速定位的问题排查路径。
1. 高背景快速排查路径(机制导向型)
(1)判断背景是否与死细胞/碎片相关(样本状态层面)
观察背景信号是否与DAPI、7-AAD等死活染料阳性群体高度重叠;
同时检查FSC/SSC是否存在大量低散射碎片或异常群体。
判定逻辑
若高背景主要集中于死细胞或碎片区域,则其本质通常为:抗体或荧光素在膜完整性受损细胞中的非特异性渗透或吸附,而非抗原特异性问题。
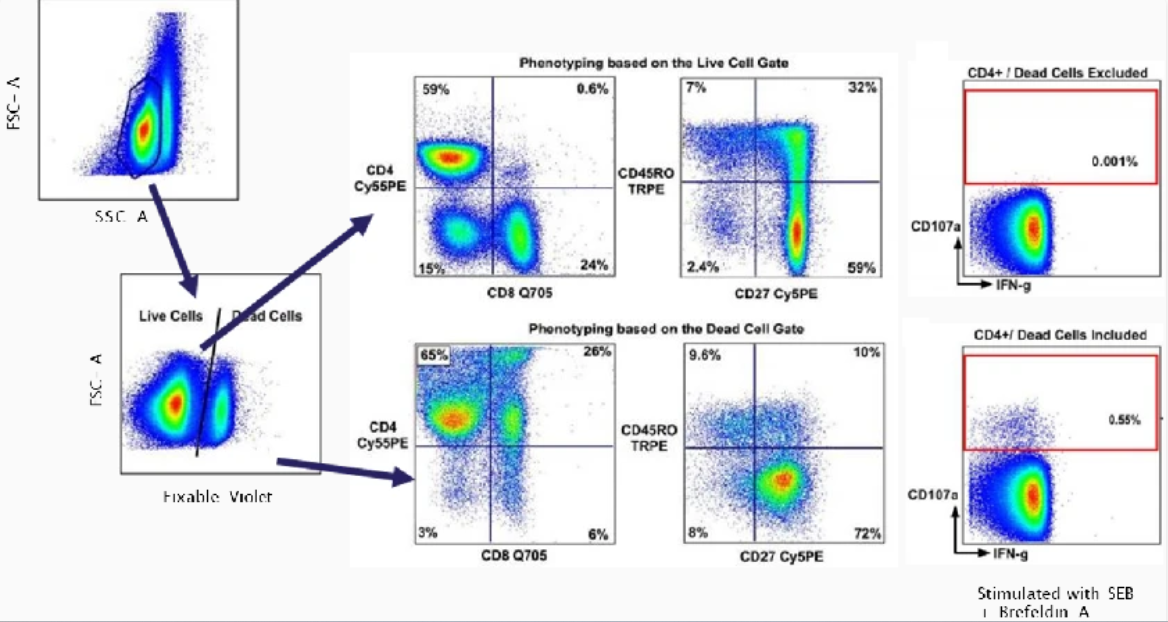
图4. 死细胞的非特异性染色结果
优先从样本质量与死细胞排除入手,而非调整抗体或补偿参数。
(2)核查FMO对照,定位是否为荧光素相关背景
在目标亚群内(而非全细胞)观察FMO对照;
判断是否存在某一通道整体基线抬高。
若FMO对照中某通道背景显著升高,提示问题更可能来源于:荧光素自身特性(如光谱渗漏、染料-细胞非特异性相互作用),而非抗体特异性。
聚焦于荧光素选择、电压设置及染色条件优化,而非简单降低抗体用量。
(3)进行“荧光素替换验证”,区分抗体问题与染料问题
在保持抗体克隆、用量、样本条件不变的前提下,仅更换荧光素;
比较背景信号变化。
若更换为非花青素类染料(如APC、Alexa Fluor 647)后背景显著下降,则可基本确认问题源于染料–细胞非特异性相互作用,在髓系细胞样本中尤为常见。
(4)复盘固定/破膜流程(胞内染色专属)
判断高背景是否仅出现在胞内染色实验;
对比表面染色与胞内染色结果。
若仅胞内染色背景升高,且FMO同样抬高,问题多与固定/破膜条件不匹配有关,而非抗体特异性不足。
![]()
流式高背景问题的解决,核心在于建立“误区排查—成因定位—实操优化”的完整逻辑链。非特异性染色引发的背景升高,并非偶发异常,而是可被系统识别和有效控制的实验变量。
通过对常见误区、隐性成因及分场景策略的系统梳理,可显著提升高背景问题的定位效率与优化成功率,为流式数据的可靠性提供坚实保障。
abinScience创立于法国,专注于高质量生命科学试剂的开发与生产,立足法国斯特拉斯堡创新科技中心,以“Empowering Bioscience Discovery”为愿景。
abinScience流式抗体产品覆盖常用检测指标,品类丰富,可满足多物种(Human/Mouse/Rat/Dog/Hamster/Monkey等)科研实验需求,为科研提供稳定可靠的支持。
相关新闻资讯