
5YR企业会员
发布人:上海优宁维生物科技股份有限公司
发布日期:2024/12/18 16:44:05
嗨,小优又来介绍Navinci公司的Naveni® PLA技术啦!前面为大家介绍了:Naveni® PLA技术&现有文献部分解析;Navinci部分产品效果展示等内容,可点击进入查看Navinci基本介绍呦~®
一、Detection of HER2(精确特异地检测 HER2)
HER2 的表达在各种癌症中起着关键作用,其过度表达与细胞失控生长和转移有关,同时也有可能成为治疗靶点。Navinci 先进的原位邻近连接技术(Naveni® PLA技术)可以准确检测 HER2,从而帮助医生做出预后和治疗决定。
细胞信号转导复杂性中的 ErbB/HER 受体
人类表皮生长因子受体(ErbB/HER)由四种细胞表面糖蛋白组成,分别称为 ErbB1/HER1、ErbB2/Neu/HER2、ErbB3/HER3 和 ErbB4/HER4(1,2)。 ErbB 受体在上皮、间充质和神经元来源的各种组织中均有表达,它们通过多种信号转导在发育、增殖和分化过程中发挥着重要作用。 配体与其同源的 ErbB 受体结合会诱导形成同源或异源二聚体复合物,从而激活受体酪氨酸激酶活性,导致下游 RAS/MAPK、PI3K/AKT 和 JAK/STAT 信号转导增加(1)。
HER2 在多种癌症中的作用
人类表皮生长因子受体家族在几种人类癌症的发病机制中起着核心作用,它们能促进细胞失控生长和肿瘤发生。 Erb/Her家族受体的过表达、扩增和激活点突变会促进肿瘤发生(1)。 HER2 的致瘤作用并不局限于潜在的增殖效应,因为 HER2 已被证明是一种转移促进因子(3-5)。
在发现 HER2 可在体外和体内诱导乳腺癌发生后,大多数有关 HER2 的研究都是在乳腺癌中进行的(6,7)。 在 25-30% 的乳腺癌中观察到 HER2 过表达,并与侵袭性临床表型相关(1)。 然而,HER2 过表达也发生在其他形式的癌症中,如胃癌、卵巢癌、子宫浆液性子宫内膜癌、结肠癌、膀胱癌、肺癌、子宫颈癌、头颈癌和食道癌(8,9)。
除了在各种癌症的发展过程中发挥作用外,它还被作为治疗靶点进行了深入评估。它还是乳腺癌和胃癌/胃食管癌的预后和预测生物标志物,改善了临床结果,针对 HER2 的疗法彻底改变了 HER2 过度表达的乳腺癌和胃癌的治疗方法(5)。
 图注:使用 NaveniBright™ HRP 原位检测恶性乳腺癌组织中的 HER2
图注:使用 NaveniBright™ HRP 原位检测恶性乳腺癌组织中的 HER2

图 1. 在 Her2 上应用靶向特异性 Naveni® 原位邻近连接试验。只有当 Navenibodies 非常接近时,它们才会产生滚圆扩增反应,从而产生强烈而明显的信号
卓越的 HER2 检测
目前获准用于临床检测 HER2 的两种方法是免疫组化(IHC)和荧光原位杂交(FISH)(10),其中 HER2 表达的评分方法是基于细胞膜染色模式。我们已开发出一种卓越的靶点特异性原位近接检测法,用于检测组织中的 HER2。与传统技术相比,该检测方法针对单个蛋白检测进行了优化,灵敏度和效率都有所提高。信号的产生是由于双抗体与同一分子上的两个不同表位结合,随后纳文抗体与之结合,从而消除了脱靶效应,与标准免疫组化(IHC)相比,大大提高了信噪比(见下文应用示例)。这使得Navinci公司的 HER2 检测优化试剂盒成为基础研究的重要工具,也是临床测试的额外验证方法,有可能成为新的标准。
应用实例 - 检测 HER2,比较 Naveni® PLA技术与 IHC
准确检测 HER2 至关重要。下面的应用实例比较了采用双抗体识别方法的 Naveni 技术和基于单抗体的传统 IHC。
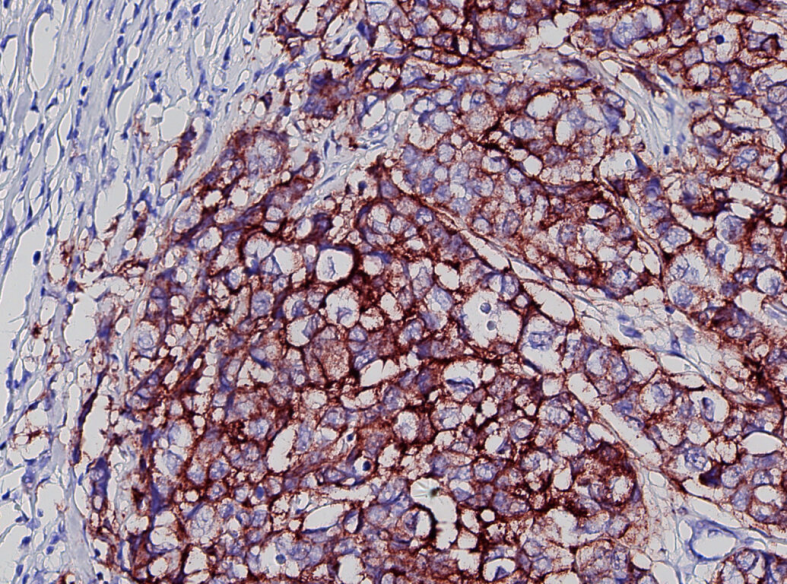
原位近接检测乳腺组织中的 HER2,显示恶性组织中的阳性染色。使用 NaveniBright 对信号进行可视化。
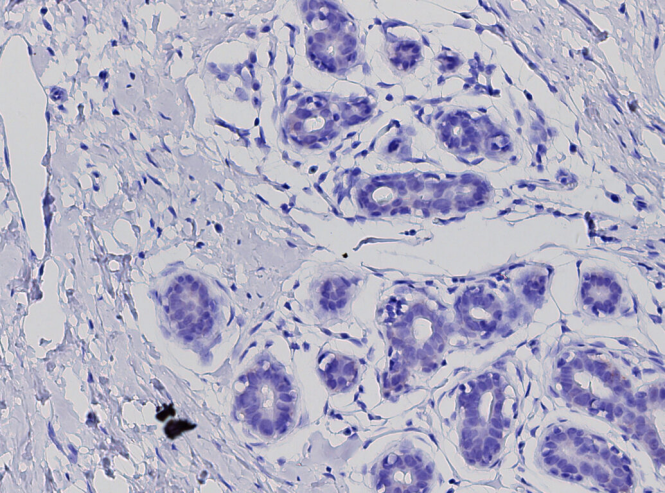 原位近接检测乳腺组织中的 HER2,显示健康组织中的阴性染色。使用 NaveniBright 对信号进行可视化。
原位近接检测乳腺组织中的 HER2,显示健康组织中的阴性染色。使用 NaveniBright 对信号进行可视化。
 乳腺组织中 HER2 的 IHC 检测,显示恶性组织中的阳性染色,A 使用兔 mAb,B 使用鼠 mAb。
乳腺组织中 HER2 的 IHC 检测,显示恶性组织中的阳性染色,A 使用兔 mAb,B 使用鼠 mAb。
 乳腺组织中 HER2 的 IHC 检测,由于乳腺组织不表达 HER2,因此显示 HER2 的非特异性染色。
乳腺组织中 HER2 的 IHC 检测,由于乳腺组织不表达 HER2,因此显示 HER2 的非特异性染色。
如何精确检测 HER2
推荐使用Navinci的NaveniBright HRP 或 NaveniFlex Tissue产品。
References
1.Olayioye, M. A., Neve, R. M., Lane, H. A., & Hynes, N. E. (2000). The ErbB signaling network: receptor heterodimerization in development and cancer. The EMBO journal, 19(13), 3159–3167. DOI: 10.1093/emboj/19.13.3159
2.Roskoski R., Jr (2019). Small molecule inhibitors targeting the EGFR/ErbB family of protein-tyrosine kinases in human cancers. Pharmacological research, 139, 395–411. DOI: 10.1016/j.phrs.2018.11.014
3.Olayioye M. A. (2001). Update on HER-2 as a target for cancer therapy: intracellular signaling pathways of ErbB2/HER-2 and family members. Breast cancer research : BCR, 3(6), 385–389. DOI: 10.1186/bcr327
4.Neve, R. M., Lane, H. A., & Hynes, N. E. (2001). The role of overexpressed HER2 in transformation. Annals of Oncology, 12, S9–S13. DOI: 10.1093/annonc/12.suppl_1.S9
5.Ménard, S., Pupa, S. M., Campiglio, M., & Tagliabue, E. (2003). Biologic and therapeutic role of HER2 in cancer. Oncogene, 22(42), 6570–6578. DOI: 10.1038/sj.onc.1206779
6.Di Fiore, P. P., Pierce, J. H., Kraus, M. H., Segatto, O., King, C. R., & Aaronson, S. A. (1987). Erb B-2 Is a Potent Oncogene When Overexpressed in NIH/3T3 Cells. Science, 237(4811), 178–182. DOI: 10.1126/science.2885917
7.Muller, W. J., Sinn, E., Pattengale, P. K., Wallace, R., & Leder, P. (1988). Single-step induction of mammary adenocarcinoma in transgenic mice bearing the activated c-neu oncogene. Cell, 54(1), 105–115. DOI: 10.1016/0092-8674(88)90184-5
8.Fukushige, S., Matsubara, K., Yoshida, M., Sasaki, M., Suzuki, T., Semba, K., Toyoshima, K., & Yamamoto, T. (1986). Localization of a novel v-erbB-related gene, c-erbB-2, on human chromosome 17 and its amplification in a gastric cancer cell line. Molecular and Cellular Biology, 6(3), 955–958. DOI: 10.1128/MCB.6.3.955
9.Reichelt, U., Duesedau, P., Tsourlakis, M. C., Quaas, A., Link, B. C., Schurr, P. G., Kaifi, J. T., Gros, S. J., Yekebas, E. F., Marx, A., Simon, R., Izbicki, J. R., & Sauter, G. (2007). Frequent homogeneous HER-2 amplification in primary and metastatic adenocarcinoma of the esophagus. Modern Pathology, 20(1), 120–129. https://doi.org/10.1038/modpathol.3800712
10.Wolff, A. C., Hammond, M. E. H., Hicks, D. G., Dowsett, M., McShane, L. M., Allison, K. H., Allred, D. C., Bartlett, J. M. S., Bilous, M., Fitzgibbons, P., Hanna, W., Jenkins, R. B., Mangu, P. B., Paik, S., Perez, E. A., Press, M. F., Spears, P. A., Vance, G. H., Viale, G., & Hayes, D. F. (2013). Recommendations for Human Epidermal Growth Factor Receptor 2 Testing in Breast Cancer: American Society of Clinical Oncology/College of American Pathologists Clinical Practice Guideline Update. Journal of Clinical Oncology, 31(31), 3997–4013. DOI: 10.1200/JCO.2013.50.9984
二、Histone H3 and lamin B1(组蛋白 H3 和层粘蛋白 B1)
探索细胞核和染色质动力学:组蛋白H3和层粘蛋白B1的蛋白质相互作用
利用 Navinci 的原位近接技术对组蛋白 H3 和层粘蛋白 B1 之间的相互作用进行可视化,加强了我们对人类细胞中染色质结构和动态完整性的了解,尤其是在癌症进展和细胞命运的背景下。
细胞核结构
细胞核是一个与膜结合的细胞器,其中包含 DNA 和 DNA 相关蛋白(染色质)。染色质是将DNA及其相关蛋白质(组蛋白)组织成紧密结构的一种秩序。DNA 被八聚体包裹,八聚体由组蛋白 H2A、H2B、H3 和 H4 各两份组成(10),从而形成核小体--染色质的基本亚基。核小体在组蛋白 H1 的帮助下进一步压缩成高阶结构,而组蛋白 H1 又被固定在片段蛋白上 (6,7,8,9)。
核膜由内外核膜(INM)、核孔复合体(NPC)和核薄层组成,核薄层是INM下面的蛋白质网状结构,与NPC相连(1)。这种内部核骨架形成了一个参与染色质组织的支架,确保了 DNA 复制和转录等核过程在空间和时间上的正确进行(2、3、4)。层粘连蛋白是支架的主要结构成分,它们位于核外围,有助于核骨架的形状和刚性,并将核骨架与细胞骨架连接起来(5)。层粘连蛋白 B1 的结构域可直接与 DNA 或组蛋白结合,也可通过 LEM 蛋白[LAP2(层粘连多肽 2)-emerin-MAN1]间接与染色质相互作用(9)。因此,层粘连蛋白 B1 可为染色质提供锚,以调节染色质的位置、高阶结构和动态。
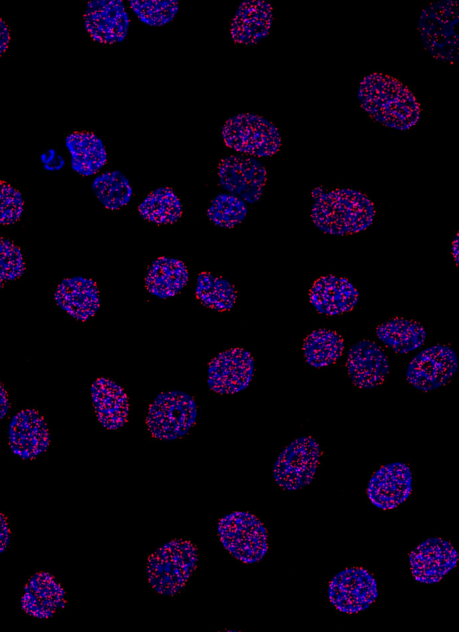 使用 NaveniFlex™ 细胞红检测 MCF7 细胞中组蛋白 H3 和层粘连 B1 的相互作用
使用 NaveniFlex™ 细胞红检测 MCF7 细胞中组蛋白 H3 和层粘连 B1 的相互作用

图 1. 组蛋白 H3 和层粘连 B1 相互作用的Naveni®原位近接试验模型。
只有当Navenibodies靠近时,它们才会产生滚圆放大反应,从而产生强烈而明显的信号。
组蛋白 H3 和层粘连 B1 相互作用的可视化
核形态在癌症进展过程中对细胞命运起着至关重要的作用。随着完整性的丧失,癌细胞的侵袭性也会增加(11)。我们已证明,使用经典的 Naveni® 原位近接检测法,可在细胞系和 FFPE 组织中观察组蛋白 H3 和层粘连 B1 之间的相互作用(图 1)。此外,我们还利用 Naveni TriFlex Cell 同时展示了组蛋白 H3 和层粘连 B1 的单独表达及其在细胞周期不同阶段的相互作用。层粘连 B1 和组蛋白 H3 的相互作用是研究人类细胞染色质结构和动态完整性的有用工具。
应用实例 - 揭开细胞戏剧的神秘面纱
通过 Naveni TriFlex Cell 见证细胞传奇,揭示组蛋白 H3 和层粘连 B1 在关键细胞事件中的动态相互作用。
Birth: 有丝分裂细胞在核膜破裂过程中显示出弥散的层粘连 B1 信号(黄色),而组蛋白 H3(洋红色)则保持在移行板附近。组蛋白 H3 和层粘连 B1 复合物(青色)解体。
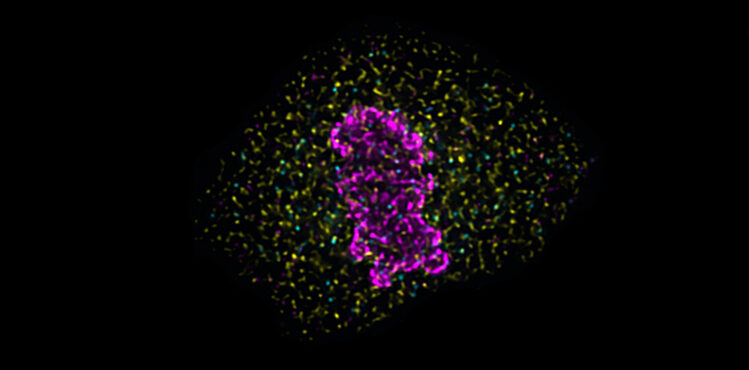 Life:在非分裂细胞中,游离的层粘连 B1 定位于核膜中,多种组蛋白 H3 和层粘连 B1 相互作用,与染色质结合的组蛋白 H3 一起出现在核质中。
Life:在非分裂细胞中,游离的层粘连 B1 定位于核膜中,多种组蛋白 H3 和层粘连 B1 相互作用,与染色质结合的组蛋白 H3 一起出现在核质中。
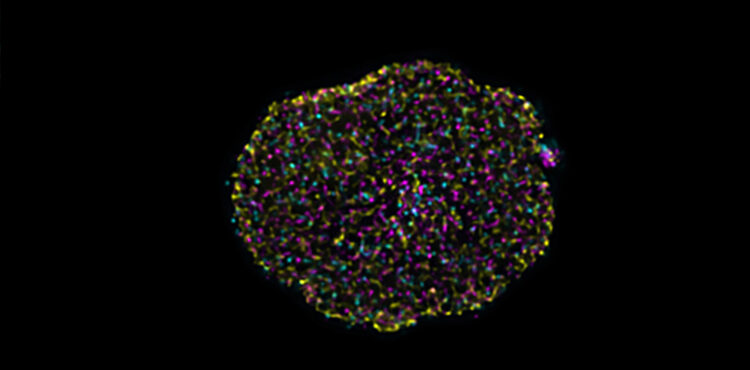
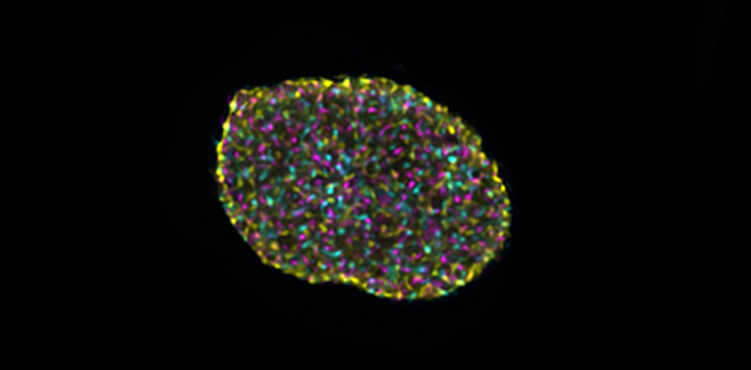 Death: 癌变早期,细胞核肿胀,核质中的复合体密度降低,组蛋白 H3 和层粘连 B1 未结合。
Death: 癌变早期,细胞核肿胀,核质中的复合体密度降低,组蛋白 H3 和层粘连 B1 未结合。
如何检测组蛋白 H3 和层粘连 B1
推荐使用Naveni TriFlex Cell 或 NaveniFlex Cell产品。
References
1.Aaronson, R. P., & Blobel, G. (1975). Isolation of nuclear pore complexes in association with a lamina. Proceedings of the National Academy of Sciences, 72(3), 1007–1011. DOI: 10.1073/pnas.72.3.1007
2.Bridger, J. M., Foeger, N., Kill, I. R., & Herrmann, H. (2007). The nuclear lamina. Both a structural framework and a platform for genome organization. The FEBS journal, 274(6), 1354–1361. DOI: 10.1111/j.1742-4658.2007.05694.x
3.Dechat, T., Pfleghaar, K., Sengupta, K., Shimi, T., Shumaker, D. K., Solimando, L., & Goldman, R. D. (2008). Nuclear lamins: major factors in the structural organization and function of the nucleus and chromatin. Genes & development, 22(7), 832–853. DOI: 10.1101/gad.1652708
4.Dorner, D., Gotzmann, J., & Foisner, R. (2007). Nucleoplasmic lamins and their interaction partners, LAP2alpha, Rb, and BAF, in transcriptional regulation. The FEBS journal, 274(6), 1362–1373. DOI: 10.1111/j.1742-4658.2007.05695.x
5.Crisp, M., & Burke, B. (2008). The nuclear envelope as an integrator of nuclear and cytoplasmic architecture. FEBS Letters, 582(14), 2023–2032. DOI: 10.1016/j.febslet.2008.05.001
6.Shumaker, D. K., Kuczmarski, E. R., & Goldman, R. D. (2003). The nucleoskeleton: lamins and actin are major players in essential nuclear functions. Current opinion in cell biology, 15(3), 358–366. DOI: 10.1016/s0955-0674(03)00050-4
7.Chang, L., Li, M., Shao, S., Li, C., Ai, S., Xue, B., Hou, Y., Zhang, Y., Li, R., Fan, X., He, A., Li, C., & Sun, Y. (2022). Nuclear peripheral chromatin-lamin B1 interaction is required for global integrity of chromatin architecture and dynamics in human cells. Protein & Cell, 13(4), 258–280. DOI: 10.1007/s13238-020-00794-8
8.Robinson, P. J., & Rhodes, D. (2006). Structure of the ’30 nm’ chromatin fibre: a key role for the linker histone. Current opinion in structural biology, 16(3), 336–343. DOI: 10.1016/j.sbi.2006.05.007
9.Barton, L. J., Soshnev, A. A., & Geyer, P. K. (2015). Networking in the nucleus: a spotlight on LEM-domain proteins. Current opinion in cell biology, 34, 1–8. DOI: 10.1016/j.ceb.2015.03.005
10.Mariño-Ramírez, L., Kann, M. G., Shoemaker, B. A., & Landsman, D. (2005). Histone structure and nucleosome stability. Expert review of proteomics, 2(5), 719–729. DOI: 10.1586/14789450.2.5.719
11.Fischer, E. G. (2020). Nuclear Morphology and the Biology of Cancer Cells. Acta Cytologica, 64(6), 511–519. DOI: 10.1159/000508780
三、Mesothelin and mucin interactions(间皮素和粘蛋白的相互作用)
可视化间皮素和粘蛋白的相互作用: 洞察癌症动态
间皮素和粘蛋白的共同表达与癌症的不良预后密切相关,在癌症中这些特定蛋白高度表达。Navinci 的原位邻近连接试验揭示了这种相互作用,为潜在的肿瘤迁移和侵袭性控制提供了早期启示。
间皮素和粘蛋白--肿瘤发生过程中的两种重要蛋白质
间皮素是一种糖基磷脂酰肌醇(GPI)锚定的细胞表面糖蛋白,在许多癌症中过度表达。间皮素在许多实体瘤中都有表达,其中以间皮瘤、上皮性卵巢癌和胰腺腺癌中的表达最为活跃,肺部和子宫恶性肿瘤以及胆管癌中也有表达(1,2,3,4,5)。粘蛋白 16(MUC16)是一种细胞表面糖蛋白,在卵巢癌中起到促进癌细胞生长的作用。 它是粘蛋白家族中的一种糖蛋白。研究表明,MUC16 在多种肿瘤类型中过表达,包括恶性间皮瘤、卵巢癌、乳腺癌、胰腺癌和结直肠癌。 MUC16 与其各种受体之间的蛋白质相互作用可能会影响细胞与细胞之间的相互作用,从而使癌细胞逃避凋亡(6、7、8、9)。第一个确定的粘蛋白结合位点位于间皮细胞上检测到的间皮素上。
许多上皮源性肿瘤中 MUC16 的过表达表明,粘蛋白在肿瘤发生中扮演着重要角色。间皮素细胞外结构域的 N 端与 MUC16 具有特异性亲和力,通过这种亲和力介导癌细胞粘附,并可能在肿瘤的种植和转移扩散中发挥作用(6、7、10)。这两种糖蛋白之间的高亲和力相互作用使这两种分子成为预防和控制转移的极佳治疗目标(6)。
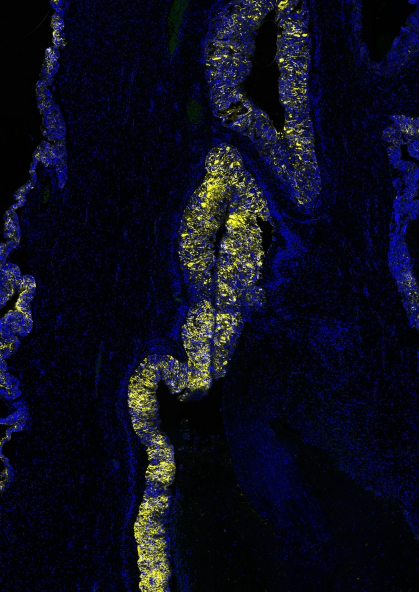
使用 NaveniFlex™ MR Atto647N 检测恶性卵巢透明细胞癌组织中间皮素和粘蛋白的相互作用。
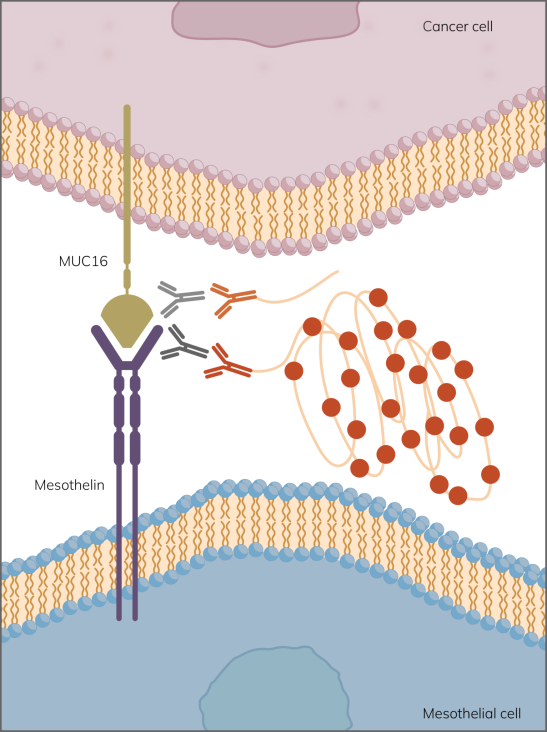 图 1. Navinci 的间皮素和粘蛋白相互作用原位近接试验模型。
图 1. Navinci 的间皮素和粘蛋白相互作用原位近接试验模型。
只有当 Navenibodies 靠近时,它们才会产生滚圆放大反应,从而产生强烈而明显的信号
Naveni® PLA技术: 阐明间皮素-粘蛋白的动态变化
间皮素和 MUC16 在多种肿瘤类型(如上皮性卵巢肿瘤和胰腺癌)中高度表达和上调。相反,它们在正常组织中的表达却很有限。我们已经展示了使用经典的Naveni® PLA试验来观察间皮素和 MUC16 在 FFPE 组织中的相互作用(图 1)。鉴于MUC16和间皮素的共同表达与预后不良和患者预后不佳密切相关(11,12),这种检测方法有利于在早期观察两者之间的相互作用,这可能有助于预防和控制肿瘤细胞的迁移和侵袭性。
应用示例--卵巢亮场读数中间皮素和粘蛋白的相互作用
 使用 NaveniBright AP 检测恶性卵巢透明细胞癌组织核心中间皮素和粘蛋白的相互作用
使用 NaveniBright AP 检测恶性卵巢透明细胞癌组织核心中间皮素和粘蛋白的相互作用
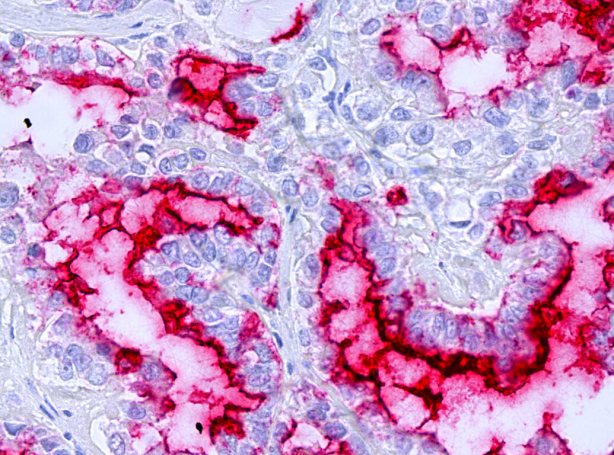 使用 NaveniBright AP 检测恶性卵巢透明细胞癌组织核心中间皮素和粘蛋白的相互作用
使用 NaveniBright AP 检测恶性卵巢透明细胞癌组织核心中间皮素和粘蛋白的相互作用
应用实例--卵巢荧光读数中间皮素和粘蛋白的相互作用
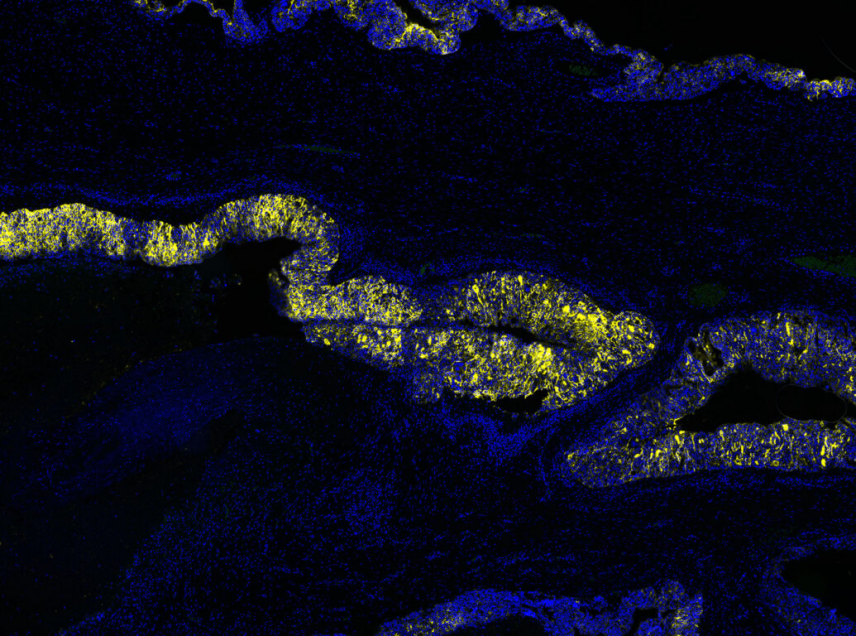 使用 NaveniFlex MR Atto647N 检测恶性卵巢透明细胞癌组织中间皮素和粘蛋白的相互作用
使用 NaveniFlex MR Atto647N 检测恶性卵巢透明细胞癌组织中间皮素和粘蛋白的相互作用
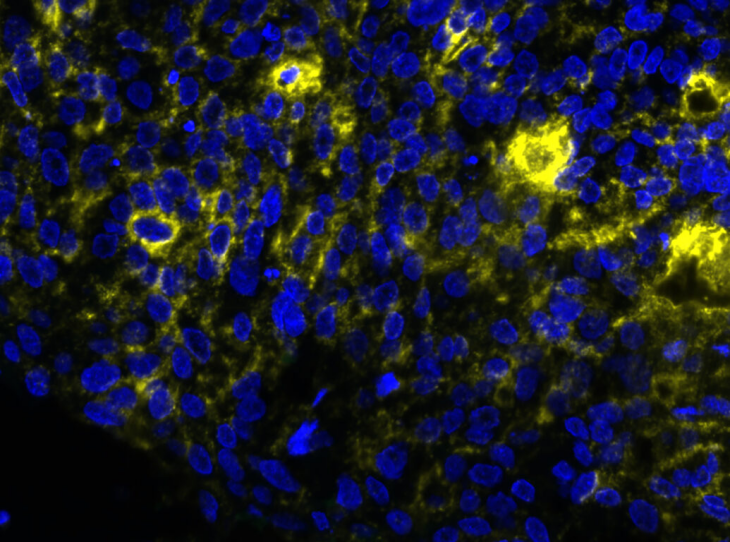 使用 NaveniFlex MR Atto647N 检测恶性卵巢透明细胞癌组织中间皮素和粘蛋白的相互作用
使用 NaveniFlex MR Atto647N 检测恶性卵巢透明细胞癌组织中间皮素和粘蛋白的相互作用
如何检测间皮素和粘蛋白的相互作用
推荐使用NaveniBright AP 和 NaveinFlex Tissue MR Atto647N。
References
1.Dainty, L. A., Risinger, J. I., Morrison, C., Chandramouli, G. V., Bidus, M. A., Zahn, C., Rose, G. S., Fowler, J., Berchuck, A., & Maxwell, G. L. (2007). Overexpression of folate binding protein and mesothelin are associated with uterine serous carcinoma. Gynecologic oncology, 105(3), 563–570. DOI: 10.1016/j.ygyno.2006.10.063
2.Galloway M.L., et al. Histopathology.2006;48:767–769.
3.Ho, M., Bera, T. K., Willingham, M. C., Onda, M., Hassan, R., FitzGerald, D., & Pastan, I. (2007). Mesothelin expression in human lung cancer. Clinical cancer research : an official journal of the American Association for Cancer Research, 13(5), 1571–1575. DOI: 10.1158/1078-0432.CCR-06-2161
4.Ordóñez N. G. (2003). Application of mesothelin immunostaining in tumor diagnosis. The American journal of surgical pathology, 27(11), 1418–1428. DOI: 10.1097/00000478-200311000-00003
5.Yu, L., Feng, M., Kim, H., Phung, Y., Kleiner, D.E., Gores, G.J., Qian, M., Wang, X.W., Ho, M. (2010). Mesothelin as a Potential Therapeutic Target in Human Cholangiocarcinoma. Journal of Cancer, 1, 141-149. DOI: 10.7150/jca.1.141
6.Gubbels, J. A., Belisle, J., Onda, M., Rancourt, C., Migneault, M., Ho, M., Bera, T. K., Connor, J., Sathyanarayana, B. K., Lee, B., Pastan, I., & Patankar, M. S. (2006). Mesothelin-MUC16 binding is a high affinity, N-glycan dependent interaction that facilitates peritoneal metastasis of ovarian tumors. Molecular cancer, 5(1), 50. DOI: 10.1186/1476-4598-5-50
7.Rump, A., Morikawa, Y., Tanaka, M., Minami, S., Umesaki, N., Takeuchi, M., & Miyajima, A. (2004). Binding of ovarian cancer antigen CA125/MUC16 to mesothelin mediates cell adhesion. The Journal of biological chemistry, 279(10), 9190–9198. DOI: 10.1074/jbc.M312372200
8.Streppel, M. M., Vincent, A., Mukherjee, R., Campbell, N. R., Chen, S. H., Konstantopoulos, K., Goggins, M. G., Van Seuningen, I., Maitra, A., & Montgomery, E. A. (2012). Mucin 16 (cancer antigen 125) expression in human tissues and cell lines and correlation with clinical outcome in adenocarcinomas of the pancreas, esophagus, stomach, and colon. Human pathology, 43(10), 1755–1763. DOI: 10.1016/j.humpath.2012.01.005
9.Shimizu, A., Hirono, S., Tani, M., Kawai, M., Okada, K., Miyazawa, M., Kitahata, Y., Nakamura, Y., Noda, T., Yokoyama, S., & Yamaue, H. (2012). Coexpression of MUC16 and mesothelin is related to the invasion process in pancreatic ductal adenocarcinoma. Cancer science, 103(4), 739–746. DOI: 10.1111/j.1349-7006.2012.02214.x
10.Kaneko, O., Gong, L., Zhang, J., Hansen, J. K., Hassan, R., Lee, B., & Ho, M. (2009). A binding domain on mesothelin for CA125/MUC16. The Journal of biological chemistry, 284(6), 3739–3749. DOI: 10.1074/jbc.M806776200
11.Belisle, J. A., Horibata, S., Jennifer, G. A., Petrie, S., Kapur, A., André, S., Gabius, H. J., Rancourt, C., Connor, J., Paulson, J. C., & Patankar, M. S. (2010). Identification of Siglec-9 as the receptor for MUC16 on human NK cells, B cells, and monocytes. Molecular cancer, 9, 118. DOI: 10.1186/1476-4598-9-118
今天学习到此为止吧!敬请期待下周的:小优进修班∣Naveni® PLA技术产品应用现状2,届时小优会为大家介绍PD1/SHP-2 、E-cadherin 和 β-catenin 之间的相互作用,不见不散呦~
应用推荐好物
上海优宁维生物科技股份有限公司
试剂 | 耗材 | 仪器 | 软件 | 定制 | 实验服务 | 供应链
免费热线:4008-168-068
咨询邮箱:info@univ-bio.com
订购商城:www.univ-bio.com
微信公众平台:优宁维抗体专家,欢迎关注!
小优博士(小程序):5大课堂, 让你的科研不再难!


相关新闻资讯