ChemicalBook CAS数据库列表 过氧化氢酶
过氧化氢酶
- CAS号:9001-05-2
- 英文名:CATALASE
- 中文名:过氧化氢酶
- CBNumber:CB9273573
- 分子式:C9H10O3
- 分子量:166.1739
- MOL File:9001-05-2.mol
过氧化氢酶化学性质
- 密度 :1.06 g/mL at 20 °C
- 蒸气压 :0Pa at 25℃
- 闪点 :41 °C
- 储存条件 :-20°C
- 溶解度 :50 mM potassium phosphate buffer, pH 7.0: soluble 2.0mg/mL
- 形态 :suspension
- 颜色 :deep brown
- PH值 :5.4(isoelectric point)
- 生物来源 :human erythrocytes
- 水溶解性 :125g/L at 25℃
- 敏感性 :Hygroscopic
- Merck :13,1910
- Specific Activity :65,000-150,000U/mL
- 稳定性 :Air and moisture sensitive. Incompatible with strong oxidizing agents. Refrigerate.
- LogP :-1.3 at 20℃
- EPA化学物质信息 :Catalase (9001-05-2)
安全信息
- 危险品标志 :B
- 危险类别码 :10
- 安全说明 :23-24/25-22
- 危险品运输编号 :UN 1993 3/PG 3
- WGK Germany :1
- RTECS号 :FI4378000
- F :10-21
- TSCA :Yes
- 海关编码 :35079090
过氧化氢酶性质、用途与生产工艺
-
背景及概述
过氧化氢酶是一种催化过氧化氢分子分解的酶。 2H2O2—→2H2O+O2 系统名为H2O2; H2O2氧化还原酶(E、C、1、11、1、6),它的辅基为血红素,分子量为250,000,以四聚体存在。几乎所有动物细胞中都存在过氧化氢酶,除真性厌氧菌外,在植物中及所有微生物中广泛存在这种酶。动物肝脏、红细胞、肾脏含有特别丰富的过氧化氢酶,主要存在于细胞的微体(又叫过氧化酶体)中。
在线粒体的呼吸链,黄素酶反应及其他氧化反应中的电子传递中,都会或可能会生成一部分有毒性的氧化还原反应产物,最主要的是超氧离子O2-及H2O2,它们在化学性质上都非常活泼,可能不可逆地损害某些生物分子,超氧化离子在细胞内的超氧物歧化酶的作用下,变成过氧化氢和氧。过氧过氢酶最主要的作用,就是分解过氧化氢,防止过氧化氢的蓄积,使细胞免受过氧化氢之害,过氧化氢酶催化过氧化氢分解速度十分迅速,比过氧化物酶快104倍,每分子酶每秒钟能催化分解44000分子的过氧化氢。
由于我国境内分布着各种类型的天然极端环境,拥有丰富的极端微生物资源, 加大力度开发各类极端微生物的过氧化氢酶,并不断提高产酶水平,有望改变我国对过氧化氢酶依赖进口的局面。
随着现代生物技术以及生物信息学的不断发展,将使得在体外对极端酶进行修饰和改造成为可能,极端微生物产CAT的开发和应用必将呈现更加诱人的前景。 -
药品概况
通用名称:过氧化氢酶
英文名称:CATALASE FROM MICROCOCCUS
别名:自溶血性链球菌分离的过氧化氢酶
Cas No:9001-05-2
结构式: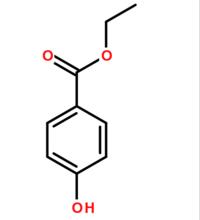
-
临床意义
CAT具有各种生理功能,它既可调节体内H2O2水平,又可充当Hb和其他含巯基蛋白质的保 护剂。血清CAT活性改变可见于下列疾病:
CAT增高主要见于肝硬化、伤寒、发热等。
CAT减低主要见于各类癌症、心肌炎、肺炎、急性胆囊炎、急性胰腺炎等。饥饿、风湿热、 外伤、局部化脓性感染、贫血等血清CAT也可呈不同程度地减低。 -
来源
几乎所有的生物机体都存在过氧化氢酶。其普遍存在于能呼吸的生物体内,主要存在于植物的叶绿体、线粒体、内质网、动物的肝和红细胞中,其酶促活性为机体提供了抗氧化防御机理。
CAT是红血素酶,不同的来源有不同的结构。在不同的组织中其活性水平高低不同。过氧化氢在肝脏中分解速度比在脑或心脏等器官快,就是因为肝中的CAT含量水平高。 -
反应机制
虽然过氧化氢酶完整的催化机制还没有完全被了解,但其催化过程被认为分为两步:
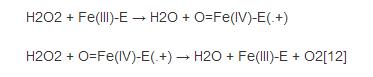
其中,“Fe()-E”表示结合在酶上的血红素基团(E)的中心铁原子(Fe)。Fe(IV)-E(.+)为Fe(V)-E的一种共振形式,即铁原子并没有完全氧化到+V价,而是从血红素上接受了一些“支持电子”。因而,反应式中的血红素也就表示为自由基阳离子(.+).
过氧化氢进入活性位点并与酶147位上的天冬酰胺残基(Asn147)和74位上的组氨酸残基(His74)相互作用,使得一个质子在氧原子间互相传递。自由的氧原子配位结合,生成水分子和Fe(IV)=O。Fe(IV)=O与第二个过氧化氢分子反应重新形成Fe(III)-E,并生成水分子和氧气。[12]活性中心铁原子的反应活性可能由于357位上酪氨酸残基(Tyr357)的苯酚基侧链的存在(帮助Fe(III)氧化为Fe(IV))而得以提高。反应的效率可能是通过His74和Asn147与反应中间体作用而得以提高。[12]该反应的速率通常可以通过米氏方程来确定。
过氧化氢酶也能够氧化其他一些细胞毒性物质,如甲醛、甲酸、苯酚和乙醇。这些氧化过程需要利用过氧化氢通过以下反应来完成: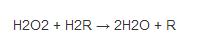
同样,具体的反应机制还不清楚。
任何重金属离子(如硫酸铜中的铜离子)可以作为过氧化氢酶的非竞争性抑制剂。另外,剧毒性的氰化物是过氧化氢酶的竞争性抑制剂,可以紧密地结合到酶中的血红素上,阻止酶的催化反应。
处于过氧化状态的过氧化氢酶中间体的三维结构已经获得解析,可以在蛋白质数据库中检索到。 -
检测
进行中的过氧化氢酶检测,可以观察到气泡。
过氧化氢酶检测是微生物学家鉴定细菌种类的主要的三种检测手段之一,即用过氧化氢来检测过氧化氢酶是否存在。假如细菌中含有过氧化氢酶,则在过氧化氢溶液中加入少量细菌提取物就能观察到氧气气泡生成。
有气泡生成,则该菌被认为是呈“过氧化氢酶阳性”。如staphylococcus和micrococcus。没有,则该菌被认为是呈“过氧化氢酶阴性”。如streptococcus和enterococcus。 虽然过氧化氢酶检测无法鉴定特定生物体,但与其他检测方法结合,它可以有效地帮助诊断。
此外细菌中是否存在过氧化氢酶,还取决于细胞生长条件和所使用的培养基。 -
应用
过氧化氢酶在食品工业中被用于除去用于制造奶酪的牛奶中的过氧化氢。过氧化氢酶也被用于食品包装,防止食物被氧化。在纺织工业中,过氧化氢酶被用于除去纺织物上的过氧化氢,以保证成品是不含过氧化物的。它还被用在隐形眼镜的清洁上:眼镜在含有过氧化氢的清洁剂中浸泡后,使用前再用过氧化氢酶除去残留的过氧化氢。过氧化氢酶在美容业中的使用:一些面部护理中加入了该酶和过氧化氢,目的是增加表皮上层的细胞氧量。
过氧化氢酶在实验室中还常常被用作了解酶对反应速率影响的工具。 -
功能概述
过氧化氢是一种代谢过程中产生的废物,它能够对机体造成损害。为了避免这种损害,过氧化氢必须被快速地转化为其他无害或毒性较小的物质。而过氧化氢酶就是常常被细胞用来催化过氧化氢分解的工具。
但过氧化氢酶真正的生物学重要性并不是如此简单:研究者发现基因工程改造后的过氧化氢酶缺失的小鼠依然为正常表现型,这就表明过氧化氢酶只是在一些特定条件下才对动物是必不可少的。
一些人群体内的过氧化氢酶水平非常低,但也不显示出明显的病理反应。这很有可能是因为正常哺乳动物细胞内主要的过氧化氢清除剂是过氧化物还原酶(peroxiredoxin),而不是过氧化氢酶。
过氧化氢酶通常定位于一种被称为过氧化物酶体的细胞器中。植物细胞中的过氧化物酶体参与了光呼吸(利用氧气并生成二氧化碳)和共生性氮固定(将氮气(N2)解离为活性氮原子)。
但细胞被病原体感染时,过氧化氢可以被用作一种有效的抗微生物试剂。部分病原体,如结核杆菌、嗜肺军团菌和空肠弯曲菌,能够生产过氧化氢酶以降解过氧化氢,使得它们能在宿主体内存活。
漂白作用
要说明的是用酶可促进漂白的进行,羊毛在含有蛋白酶Bactosol ST的过氧化氢漂液中漂白,可显著提高羊毛的白度和亲水性。这是由于酶促进羊毛纤维初始受到快速的浸蚀,致使羊毛漂白较易进行。从此原理出发,将蛋白酶对羊毛先预处理,使纤维表面裸露,再进行漂白,显然效果更好,且纤维损伤也易控制。 -
分布
过氧化氢酶存在于所有已知的动物的各个组织中,特别在肝脏中以高浓度存在。在投弹手甲虫(bombardier beetle)中,过氧化氢酶具有独特用途。这种甲虫具有两套分开储存于腺体中的化学物。大的腺体中储存着对苯二酚和过氧化氢,而小的腺体中储存着过氧化氢酶和辣根过氧化物酶。当甲虫将两个腺体中的化学物质混合在一起时,就会释放出氧气,而氧气既可以氧化对苯二酚又可以作为助推剂。
过氧化氢酶也普遍存在于植物中,但不包括真菌,虽然有些真菌被发现在低pH值和温暖的环境下能够产生该酶。
绝大多数需氧微生物都含有过氧化氢酶[4]。例外包括Streptococcus,一种没有过氧化氢酶的需氧细菌。部分厌氧微生物,如Methanosarcina barkeri,也含有过氧化氢酶。 - 毒性 FAO/WHO 2001年规定由牛肝制得者,ADI不作限制性规定;溶纤维蛋白小球菌和黑曲霉制得者,ADI延期决定;由青霉制得者未作规定;由李氏木霉(Trichoderma reesei)制得者不作特殊规定。
- 使用限量 适度为限(FDA,§173.135,2000)。
-
食品添加剂最大允许使用量最大允许残留量标准
▼▲添加剂中文名称允许使用该种添加剂的食品中文名称添加剂功能最大允许使用量(g/kg)最大允许残留量(g/kg)过氧化氢酶食品酶制剂按生产需要适量使用(有特别规定的除外)
-
主要参考资料
[1] 化工空间-过氧化氢酶的物化性质
[2] 杨玉林,贺志安 主编.临床肝病实验诊断学.北京:中国中医药出版社.2007.第8 -
化学性质
近乎白色至浅棕黄色的无定形粉末或液体。分子量约24万。溶于水,水溶液一般呈浅棕黄色至棕色,几乎不溶于乙醇、氯仿和乙醚。最适pH值7.0,在稀酸中作用受阻。最适温度0~10℃,温度过高或过氧化氢浓度过大均能破坏其活性。1分子的过氧化氢酶在1min内约可使500万个过氧化氢分子破坏。主要作用原理为:
由肝脏所得者的最适pH值为7.0左右,在5.3~8.0之间活性都很高,5.0以下则很快下降。由黑曲菌所得者pH值在2~7之间均很活跃,而由小球菌制得者的最适pH值为7~9。
天然品存在于好气性微生物、哺乳动物的红血球、肝脏(极丰富)等中。 - 用途 酶制剂。主要用于干酪、牛奶和蛋制品等的生产,以消除由紫外线照射时产生过氧化氢而造成的特异臭味;亦可用作面包制造时的疏松剂。在牛奶中的最高用量为20mg/kg。
- 用途 常用诊断用酶。配合偶联反应,测定葡萄糖等。食物防腐、分解过氧化氢。生化试剂。
- 用途 一种氧化还原酶,可将过氧化氢氧化为氧,与此同时将另一分子过氧化氢还原为水。作为天然抗氧化剂,可用于研究活性氧物质对基因表达和凋亡的作用。它还被用于保护蛋白质、脂质和核酸免受氧化损伤。
- 用途 用于生化研究、食物防腐,牛奶的杀菌脱糖等。临床上常用作诊断酶,测定葡萄糖含量。
-
生产方法
由牛肝抽提物经纯化而得。
由黑曲霉变种(Aspergillus niger var.)在通风搅拌等控制条件下培养而得。
由溶纤维蛋白小球菌(Micrococcus lysodeikticus)的深层发酵液提取精制而成。 - 生产方法 以牛肝为原料,在35%二氧六环中匀浆,过滤后用二氧六环沉淀,饱和硫酸铵结晶得产品。
- 类别 有毒物质
- 可燃性危险特性 热分解排出辛辣刺激烟雾
- 储运特性 库房低温通风干燥
- 灭火剂 水,二氧化碳, 泡沫, 干粉
过氧化氢酶上下游产品信息
上游原料
下游产品
过氧化氢酶 试剂级价格
- 更新日期:2025/02/08
- 产品编号:HY-135849
- 产品名称:过氧化氢酶 Catalase
- CAS编号:9001-05-2
- 包装:100mg
- 价格:500元
- 更新日期:2025/02/05
- 产品编号:C0052
- 产品名称:过氧化氢酶,从牛肝所得 Catalase from Bovine Liver
- CAS编号:9001-05-2
- 包装:1G
- 价格:1090元
过氧化氢酶生产厂家
- 公司名称:上海阿拉丁生化科技股份有限公司
- 联系电话:400-6206333 18021050169
- 电子邮件:market@aladdin-e.com
- 国家:中国
- 产品数:48459
- 优势度:58
- 公司名称:山东丰泰生物科技有限公司
- 联系电话:0531-0531-82066716 15662658391
- 电子邮件:528732991@qq.com
- 国家:中国
- 产品数:1024
- 优势度:58
- 公司名称:南京罗迈美生物科技有限公司
- 联系电话:
- 电子邮件:sales@njromanme.com
- 国家:中国
- 产品数:4529
- 优势度:58
- 公司名称:上海鼓臣生物技术有限公司
- 联系电话:021-34675735 19147740836
- 电子邮件:1986399151@qq.com
- 国家:中国
- 产品数:9844
- 优势度:58
- 公司名称:金华市佰康生物工程有限公司
- 联系电话:0573-15557365800 15557365800
- 电子邮件:78117547@qq.com
- 国家:中国
- 产品数:476
- 优势度:58
- 公司名称:广东迈科百胜生物技术有限公司
- 联系电话:153-0048-7802 15300487802
- 电子邮件:jlin@microbiosyn.com
- 国家:中国
- 产品数:186
- 优势度:58
- 公司名称:伊势久(江苏连云港)生物科技有限责任公司
- 联系电话: 18082049515
- 电子邮件:2757382053@qq.com
- 国家:中国
- 产品数:2150
- 优势度:58
- 公司名称:湖北魏氏化学试剂股份有限公司
- 联系电话:027-59102966 18717199209
- 电子邮件:2853877583@QQ.com
- 国家:中国
- 产品数:7890
- 优势度:58
- 公司名称:北京百灵威科技有限公司
- 联系电话:010-82848833 400-666-7788
- 电子邮件:jkinfo@jkchemical.com
- 国家:中国
- 产品数:94657
- 优势度:76
- 公司名称:上海迈瑞尔生化科技有限公司
- 联系电话:021-61259108 18621169109
- 电子邮件:market03@meryer.com
- 国家:中国
- 产品数:40228
- 优势度:62
9001-05-2, 过氧化氢酶相关搜索: