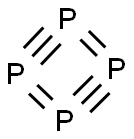
白磷
- CAS号:12185-10-3
- 英文名:White phosphorus
- 中文名:白磷
- CBNumber:CB82131283
- 分子式:P4
- 分子量:123.896
- MOL File:12185-10-3.mol
白磷化学性质
- 熔点 :44.1 (0.181mm) [MER06]
- 沸点 :277℃ [CRC10]
- 密度 :α: 1.83; β. 1.88 [MER06]
- 水溶解性 :1 part/300,000 parts H2O; 1g/400mL absolute alcohol; 1 g/200mL CHCl2; 1g/40mL benzene [MER06]
- NIST化学物质信息 :Phosphorus tetramer(12185-10-3)
- EPA化学物质信息 :Phosphorus (white or yellow) (12185-10-3)
白磷性质、用途与生产工艺
- 理化性质 黄磷,分子式P4,又称白磷。磷的同素异形体之一。黄磷有α-黄磷和β-黄磷。一般所谓黄磷是指α-黄磷而言,β-黄磷是将α-黄磷冷却到-77K以下才得到的。白磷在400℃密闭加热数小时会转化为红磷: 白磷⇌红磷+16.7kJ。纯品为黄色或白色蜡状立方晶体或透明结晶性固体,有亚臭蒜气味,剧毒。见光颜色变暗,在暗处能发磷光。相对密度 1.82(20℃),熔点44.1℃,沸点280℃。在空气中34℃时能自燃并冒白烟。不溶于冷水和醇,微溶于热水,易溶于二硫化碳,溶于苯、氨、强碱、乙醚、三氯 甲烷、甲苯、丙酮和四氯化碳。与卤族元素激烈反应,在氯气中自行起火,遇液体氯或溴可爆炸,与冷浓硝酸激烈反应生成磷酸,与碱(苛性碱)溶液共热放出磷化氢,须保存在水中。黄磷可由磷灰石、硅石和焦炭按一定配比混合, 在电炉中熔融得黄磷蒸气, 再经迅速冷却而制得。其反应式如下: 4Ca5F(PO4)3+21SiO2+30C→ 3P4+30CO+SiF4+20CaSiO3。
-
磷的同素异形体
磷的同素异形体有白磷、红磷、黑磷、紫磷,它们拥有不同的分子结构,从而晶体构型也不同,最终表现为物理化学性质差异。
白磷是磷氏家族中最活泼、脾气也最火爆的小弟,这是因为其分子结构中的四个磷原子构成了一个正四面体,理论键角为60°,但实际上其分子中的P-P键98%是P原子间分别用3p轨道“肩靠肩”重叠形成的共价键,而p轨道成键的键角一般是90°,为了努力向60°靠近,P-P键受到了很大应力而弯曲,非常不稳定,因而具有很高的化学活性,着火点只有40 ℃,在空间中就会自燃生成大量浓烟。也是因为这种属性,没法儿在室温下用X射线衍射去探测它的实际晶体结构。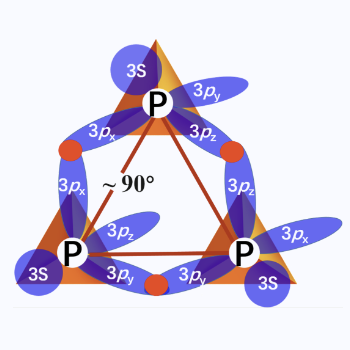
黑磷是这个家中最稳重的大哥,脾气最好最冷静,它是具有金属光泽的黑色晶体,能导电,着火点为490 ℃,通常难以发生化学反应。1914年美国物理学家Bridgman首次在高压高温条件下用白磷合成了黑磷这种同素异构体。同红磷一样,它有着极为复杂的空间结构,因而也只能以P作为其化学式。
紫磷是目前已知最稳定的磷的同素异形体。
红磷又名赤磷,为紫红色或略带棕色的无定形粉末,有光泽,无毒。红磷要在240℃左右才能燃烧。红磷以P4四面体的单键形成链或环的高聚合结构,具有较高的稳定性。若不加压则不熔化而升华,汽化后再冷凝则得白磷。1845年,奥地利化学家施勒特尔发现了红磷,确定它与白磷是同素异形体。但和白磷的简单结构相比,红磷的结构更为复杂,且至今尚未有明确结论,因此它还未有具体分子式,一般以P作为其化学式。1947年,Roth等人报道了红磷至少存在五种不同同素异形体I~V。 - 毒性 参见黄磷。
-
毒性
对皮肤有烧伤作用。急性中毒时会出现腹痛、腹泻,吐出物有大蒜味,在暗处能发光。
皮肤被黄磷烧伤时,立即用大量的水冲洗,并在水洗下用木刮片将黄磷除净。如溅入眼内,应立即用大量水冲洗后,送医院治疗。被黄磷烧着的衣服须用水浇灭,并用水浇时立即脱下。误服黄磷引起急性中毒时,用0.2%高锰酸钾或1%硫酸铜溶液反复洗胃,至洗出液中黄磷的气味消失为止。成人误服50 mg/kg可致死。
最高容许浓度为0.03 mg/kg。
操作时要穿工作服、戴防毒口罩等劳保用品。严禁在车间吃东西、吸烟;下班后淋浴。生产过程应密闭、通风良好。生产工人每半年体检一次,应给予保健饮食。 - 注意事项 黄磷可用铁桶盛装,桶内盛水,将黄磷浸没于水中。包装上应有明显的 “自燃物品”及“剧毒品”标志。应贮存于较阴凉的库房内,与爆炸品、氧化剂、卤素、强酸和氧气隔离存放,远离热源与火种。操作时应戴防护用具,防止与皮肤接触,切勿入口。
- 化学性质 白磷是一种磷的单质,化学式为P4。外观为白色或黄色蜡状固体,质软,可用刀切割。不溶于水,微溶于醇,溶于液碱、苯、乙醚、氯仿、甲苯,易溶于二硫化碳。燃点低,所以大部分白磷都储存在水中,在空气中很短时间就会冒烟继而燃烧。人的手温更容易使它燃烧,所以取用白磷时必须用镊子去取,绝对不能用手指去接触,否则手就会被灼烧,造成疼痛难愈的灼伤。白磷还是一种剧毒的物质。人的中毒剂量为15mg,致死量为50mg。
- 用途 黄磷主要用于生产赤磷、磷酸和磷化物,也用于制造农药和灭鼠药,在国防上可用于生产燃烧弹、烟幕弹和信号弹。
-
生产方法
1.将磷矿石在高温下,用碳还原生成磷蒸气,经冷凝后制得黄磷。还原反应在高炉内进行时称为高炉法;在电炉内进行时称为电炉法。用电炉法生产黄磷有产品质量好,劳动生产率高,生产成本低的优点,目前国内外普遍采用电炉法生产,而且电炉向大型化发展。
2.电炉法将磷矿石、焦炭和硅石分别破碎至规定粒度,然后按规定比例混合,混合料在密闭的三相电炉中于1400~1500℃高温下熔融进行还原反应,生成的磷蒸气经冷凝塔冷却,凝聚成液滴,与机械杂质一起进入塔底集磷槽中,即得粗磷。将粗磷在精制锅中用蒸汽加热、搅拌、澄清后,纯磷沉积在锅底。放入黄磷池,冷却成型后,制得黄磷成品。集磷槽底的磷泥定期取出,作回收磷用。从冷凝塔出来的尾气含一氧化碳80%~90%,可用作燃料,也可供制甲酸或草酸用。炉渣定期排出,供制水泥、砖和矿渣棉等建筑材料。磷铁(含21%~22%P,63%~73%%Fe)定期排出,供冶金工业用。
白磷上下游产品信息
上游原料
下游产品
白磷生产厂家
- 公司名称:Protheragen-ING
- 联系电话: +16313385890
- 电子邮件:info@protheragen-ing.com
- 国家:美国
- 产品数:3868
- 优势度:58
- 公司名称:Wonda Science
- 联系电话:--
- 电子邮件:wonda@wondascience.com
- 国家:美国
- 产品数:2192
- 优势度:50
12185-10-3, 白磷相关搜索: